Fármacos para la diabetes mellitus
El páncreas desarrolla funciones únicas y vitales proporcionando enzimas digestivas esenciales y secretando hormonas responsables del equilibrio de la glucosa. Desde el punto de vista farmacológico la enfermedad pancreática más importante es la diabetes mellitus. Millones de personas padecen diabetes, una enfermedad causada por factores genéticos y ambientales que afecta a la utilización celular de la glucosa. Como la glucosa es esencial para todas las células, los efectos de la diabetes se manifiestan a nivel global. La diabetes merece una consideración particular en farmacología porque el personal de enfermería encontrará muchos pacientes con esta enfermedad.
Conceptos clave
Los conceptos clave numerados proporcionan un breve resumen de los aspectos más importantes de cada uno de los apartados correspondientes dentro del capítulo. Si alguno de estos puntos no está claro, acuda al apartado correspondiente para su revisión.
El páncreas es una glándula endocrina y exocrina. La insulina se libera cuando aumenta la glucemia y el glucagón cuando ésta disminuye.
La DM tipo 1 está causada por la absoluta ausencia de secreción de insulina debido a una destrucción autoinmune de las células de los islotes pancreáticos. Si no se trata, da lugar a afectación grave de los sistemas cardiovascular y nervioso.
La DM tipo 1 se trata mediante restricciones dietéticas, ejercicio y terapia con insulina. Los distintos tipos de preparados de insulina varían en su inicio de acción, pico de acción y duración total de su efecto.
La DM tipo 2 está causada por una ausencia de sensibilidad de los receptores de la insulina en las células diana así como una disminución de la secreción de insulina. Si no se trata aparecen las mismas complicaciones que en la DM tipo 1.
La DM tipo 2 se controla a través de modificaciones en el estilo de vida y fármacos antidiabéticos orales. Existen al menos cinco tipos distintos de esta clase de fármacos disponibles para el tratamiento de la DM tipo 2.
Funciones pancreáticas normales
Localizado detrás del estómago y entre el duodeno y el bazo, el páncreas es un órgano esencial para los sistemas digestivo y endocrino. Es responsable de la secreción al duodeno de varias enzimas que contribuyen a la digestión química de los nutrientes. Esta es su función exocrina. Determinados grupos de células pancreáticas denominadas islotes de Langerhans son las responsables de su función endocrina: la secreción de glucagón e insulina. Las células alfa secretan glucagón, mientras que las células beta secretan insulina (figura 44.1). Al igual que otros órganos endocrinos, el páncreas secreta estas hormonas directamente en los capilares sanguíneos donde son transportados hacia los tejidos corporales. Tanto la insulina como el glucagón juegan un papel clave en el mantenimiento normal de la glucemia.
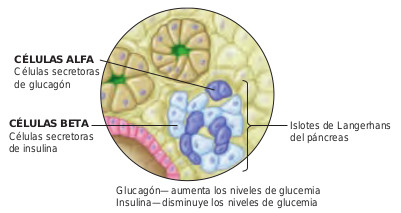
La secreción de insulina está regulada por factores químicos, hormonales y neurológicos. El factor regulador más importante son las concentraciones de glucosa en sangre o glucemia. Después de la ingesta, cuando las concentraciones de glucosa aumentan, los islotes de Langerhans secretan insulina, que se encarga de que la glucosa abandone el torrente sanguíneo y penetre al interior celular. Una concentración alta de insulina y una glucemia baja proporcionan un sistema de retroalimentación negativa hacia el páncreas que detiene la secreción de insulina.
La insulina afecta al metabolismo de los carbohidratos, lípidos y proteínas en la mayoría de las células corporales. Su acción primordial es ayudar en el transporte de glucosa; sin insulina la glucosa no puede penetrar en las células. Una célula puede estar literalmente nadando en glucosa, que si no existe insulina no puede servir como fuente de energía celular. Por tanto la insulina tiene un efecto hipoglucémico ya que su presencia condiciona que la glucosa disminuya en el torrente sanguíneo y suero. El encéfalo constituye una importante excepción, ya que no requiere insulina para el transporte de glucosa.
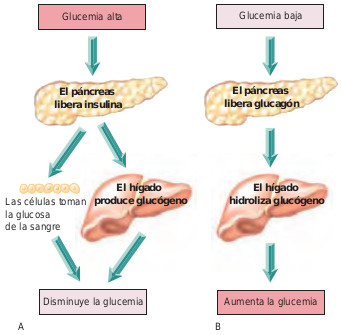
Las células de los islotes pancreáticos también secretan glucagón, un antagonista de la insulina con acciones opuestas a la misma. Cuando la glucemia es baja, se secreta glucagón. Su función primordial es mantener una glucemia sérica adecuada entre las comidas. Por tanto el glucagón tiene un efecto hiperglucémico, ya que su presencia causa el aumento de la glucosa sanguínea. La figura 44.2 ilustra las relaciones entre la glucemia sanguínea, la insulina y el glucagón.
Los niveles de glucemia se mantienen en condiciones normales en un rango normal gracias al efecto de la insulina y el glucagón; sin embargo otras hormonas y fármacos pueden afectar al metabolismo de la glucosa. Otras hormonas hiperglucémicas son epinefrina, hormonas tiroideas, hormona de crecimiento y corticoesteroides. Algunos fármacos de uso común que pueden provocar hiperglucemia son la fenitoína, AINEs y diuréticos. En cambio, el alcohol, litio, fármacos inhibidores de la enzima convertidora de la angiotensina (ECA) y bloqueantes beta-adrenérgicos tienen un efecto hipoglucémico. La glucemia debe ser controlada periódicamente en pacientes sometidos a tratamiento con los fármacos anteriormente mencionados.
Diabetes Mellitus
Se cree que aproximadamente 135 millones de personas padecen diabetes mellitus (DM) en todo el mundo en el momento actual y hasta 300 millones podrían padecerla hacia el año 2025.
La etiología de la DM incluye una combinación de factores genéticos y ambientales. El reciente aumento de la frecuencia de la enfermedad está probablemente relacionado con el aumento de hábitos sedentarios, y el estilo de vida estresante con el aumento del consumo de alimentos hipercalóricos, que dan como resultado obesidad, y la mayor longevidad.
La DM está formada por un grupo de enfermedades metabólicas en las cuales existe una secreción deficitaria de insulina o una sensibilidad disminuida de los receptores de insulina o de las células diana, que se traduce en hiperglucemia. La DM incluye la diabetes tipo 1, tipo 2, diabetes gestacional y otros tipos específicos, como la diabetes asociada al síndrome de Cushing o la diabetes químicamente inducida. En este capítulo se tratarán solamente la DM tipo 1 y tipo 2.
Etiología y características de la diabetes mellitus tipo 1
La diabetes mellitus tipo 1 supone el 10% de todos los casos de DM y es una de las enfermedades más frecuentes en la infancia.
La DM tipo 1 se denominó diabetes de inicio juvenil ya que su diagnóstico se realiza con frecuencia entre los 11 y 13 años. Sin embargo, debido a que aproximadamente el 25% de los casos es diagnosticado en la edad adulta, esta denominación no se considera la más precisa. Este tipo de diabetes corresponde a la diabetes mellitus insulinodependiente.
La DM tipo 1 se produce como resultado de una destrucción autoinmunitaria de las células beta pancreáticas, que condiciona la ausencia de la secreción de insulina. Se piensa que la enfermedad se debe a un conjunto de factores genéticos, inmunológicos y ambientales. De entre ellos el factor genético parece obvio, ya que la enfermedad se detecta en los hijos y hermanos de los pacientes con DM.
Los signos y síntomas de la DM tipo 1 se repiten en todos los pacientes siendo el signo diagnóstico más frecuente la hiperglucemia sostenida. Se enumeran a continuación los signos y síntomas típicos de esta enfermedad:
- Hiperglucemia: glucemia en ayunas mayor de 126 mg/dL en al menos dos extracciones distintas
- Poliuria: diuresis excesiva
- Polifagia: aumento del apetito
- Polidipsia: aumento de la sed
- Glucosuria: concentraciones aumentadas de glucosa en orina
- Pérdida de peso
- Fatiga
La DM no tratada produce afectación a largo plazo de las arterias condicionando alteraciones cardíacas, ictus, enfermedad renal y ceguera. La ausencia de una adecuada circulación en los pies puede causar gangrena de los dedos de los pies y requerir amputación. La degeneración nerviosa es frecuente con síntomas que van desde hormigueos en los dedos de las manos o de los pies hasta pérdida completa de la sensibilidad en la extremidad afectada. Como la glucosa no puede penetrar en las células, los lípidos se utilizan como fuente de energía produciéndose y acumulándose cuerpos cetónicos. Estas sustancias producen en el paciente un olor del aliento afrutado a acetona característico, y disminuyen el pH sanguíneo causando cetoacidosis diabética (CAD) que puede producir coma y la muerte en caso de no ser tratada.
Farmacoterapia con insulina
La insulina estuvo disponible como medicación por primera vez en 1922. Antes de esta fecha los enfermos de diabetes tipo 1 no podían mantener glucemias normales, por lo que sufrían numerosas complicaciones y normalmente morían jóvenes. El aumento de la disponibilidad de la insulina y las mejoras en los productos derivados de la misma, la mejora de los dispositivos personales de monitorización de la glucosa y la bomba de insulina han hecho posible que estos pacientes mantengan un control de su glucemia más exacto.
Como los pacientes con DM carecen por completo de la secreción de insulina, el objetivo terapéutico es administrar insulina como tratamiento sustitutivo en cantidades similares a las fisiológicas. Ya que la secreción normal de insulina varía ampliamente como respuesta a las actividades de la vida diaria como la ingesta o la realización de ejercicio, la terapia con insulina debe planificarse cuidadosamente y ser coordinado con una planificación correcta de la dieta y de los hábitos de vida. El resultado deseable del tratamiento con insulina es prevenir las consecuencias a largo plazo de la enfermedad mediante el mantenimiento estricto de las glucemia dentro del rango normal.
El principio fundamental que debe recordarse sobre el tratamiento con insulina es que la cantidad correcta de insulina debe estar disponible para las células cuando la glucosa está disponible en la sangre. La administración de insulina cuando la glucosa no está disponible en la sangre, puede llevar al paciente a una hipoglucemia severa y coma. Esta situación ocurre cuando el paciente se administra insulina correctamente, pero se salta una comida; por tanto la insulina está disponible para las células, pero la glucosa no. Otro ejemplo sería cuando el paciente realiza ejercicio intenso. En este caso la insulina puede haberse administrado a su hora y se puede haber comido correctamente; sin embargo, la actividad muscular rápida consume la glucosa de la sangre y el paciente sufre hipoglucemia. Los pacientes diabéticos que practican deportes de competición, necesitan consumir alimentos y bebidas deportivas justo antes o durante la actividad para mantener la glucemia dentro de niveles normales.
Los pacientes con diabetes que se saltan u olvidan su dosis de insulina pueden enfrentarse también a serias consecuencias.
Una vez más, hay que recordar el principio fundamental de la terapia con insulina: la cantidad correcta de insulina debe estar disponible para las células cuando la glucosa está disponible en la sangre. Sin insulina, la glucosa en sangre procedente de la ingesta puede incrementarse a niveles elevados causando hiperglucemia y posible coma. Una correcta planificación y asesoramiento por parte del personal de enfermería es esencial para unos resultados satisfactorios del tratamiento y un cumplimiento correcto por parte del paciente.
Están disponibles distintos tipos de insulina según sea su procedencia, comienzo y duración de su efecto. Hasta 1980, la insulina procedía de páncreas de ternera o cerdo. Casi todas las insulinas actuales son humanas y se obtienen mediante la tecnología de ADN recombinante, ya que es más eficaz, causa menos alergias y tiene menos incidencia de resistencia. Los farmacólogos han modificado la insulina humana para mejorar su farmacocinética consiguiendo una mayor rapidez de acción o un efecto más prolongado. Estas formas de insulina modificadas se denominan análogos de insulina.
Las dosis de insulina deben ser altamente individualizadas para cada paciente para conseguir un control preciso de la glucemia. Algunos pacientes pueden requerir dos o más inyecciones diarias de insulina. En algunas ocasiones se recurre a combinar dos tipos distintos pero compatibles de insulina utilizando un método estándar para obtener los efectos terapéuticos deseados. Estos tratamientos se administran mediante cartuchos que se comercializan con soluciones previamente mezcladas listas para su uso.
La vía de administración más frecuente de la insulina es la subcutánea, sin embargo se está investigando en este aspecto para intentar conseguir preparados con otras vías de administración más cómodas como la vía intranasal. En el año 2006, una forma inhalada de insulina fue aprobada por la FDA. Esta insulina está preparada en forma de polvo seco en un dispositivo para su inhalación a través de la boca (figura 44.3A). Esta forma presenta una mayor rapidez en su acción hipoglucemiante y consigue un efecto de la misma duración que las formas habituales de insulina subcutánea. Además tiene un efecto más largo que las insulinas de rápida acción.
Algunos pacientes utilizan una bomba de insulina (figura 44.3B). Esta bomba habitualmente se fija al abdomen y está programada para administrar pequeñas dosis de insulina subcutánea a intervalos de tiempo determinados. Esta forma de tratamiento puede complementarse con bolos subcutáneos de insulina después de las comidas si es necesario. La mayoría de las bombas disponen de un sistema de alarma que suena para recordar a los pacientes que tienen que inyectarse su dosis de insulina. La figura 44.3B muestra una bomba de insulina.
La reacción adversa principal del tratamiento con insulina es la hipoglucemia. Esta entidad se produce cuando el paciente con DM tipo 1 tiene más insulina en su sangre de la necesaria para la cantidad de glucosa circulante. La hipoglucemia puede ocurrir durante el nivel máximo de insulina, durante el ejercicio, cuando el paciente recibe demasiada insulina por un error de la medicación o cuando el paciente se salta una comida.
Algunos de los síntomas de la hipoglucemia son los mismos que los de la cetoacidosis. Los que diferencian las dos entidades son palidez, frialdad y sudoración con glucemia por debajo de 50 mg/dL y aparición rápida de los síntomas. Si no se trata, la hipoglucemia grave puede desencadenar la muerte.
Otras reacciones adversas de la insulina incluyen alergia localizada en el lugar de la inyección, urticaria generalizada y adenopatías. Algunos pacientes experimentan el llamado fenómeno de Somogyi, que consiste en una disminución rápida de la glucemia habitualmente durante la noche, que estimula la liberación de hormonas que elevan la glucemia como la adrenalina, el cortisol y el glucagón con la consiguiente elevación de la glucemia por la mañana. La administración adicional de insulina en este momento puede producir una hipoglucemia de re bote de instauración rápida.
La hormona glucagón puede administrarse en algunos pacientes diabéticos con alteración de su secreción, como tratamiento sustitutivo durante los estados hipoglucémicos.
La inyección de 1 mg de glucagón intravenoso, intramuscular o subcutáneo, revierte los síntomas de la hipoglucemia en 20 minutos o menos, dependiendo de su vía de administración.


Consideraciones de enfermería
El papel del profesional de enfermería en el tratamiento con insulina incluye una monitorización estrecha del estado del paciente así como facilitar asesoramiento respecto al tratamiento farmacológico prescrito. En concreto el paciente debe familiarizarse con información respecto al comienzo, pico y duración de la acción de la insulina utilizada.
Valore en el paciente la existencia de signos o síntomas de hipoglucemia, así como la necesidad de monitorización de glucosa. Es más frecuente que la hipoglucemia aparezca cuando la insulina alcanza su pico de efecto, durante el ejercicio o durante una enfermedad aguda. Compruebe que el paciente está preparado para comer antes de recibir la insulina. Valore el nivel de entendimiento por parte del paciente de los posibles síntomas asociados a la administración de insulina de hipoglucemia y cetoacidosis diabética. Enseñe al paciente a reconocer estos síntomas y a actuar en consecuencia como respuesta a los mismos. Las contraindicaciones de la insulina incluyen hipersensibilidad a alguno de los componentes del fármaco, y en este caso la hipoglucemia puede empeorar por la administración de insulina. Utilice la insulina con precaución en mujeres embarazadas y en pacientes con estrés grave. Estos pacientes necesitan con frecuencia mayor cantidad de insulina y necesitan monitorización más estrecha.
Dos de los tipos de insulina más frecuentemente utilizados son la insulina NPH isofano y la insulina regular. La insulina de acción intermedia o NPH se utiliza para conseguir un efecto más prolongado que la insulina regular y otras insulinas de acción rápida. Su comienzo de acción es entre 1 y 4 horas mientras que alcanza su pico de efecto entre 18 y 24 horas. Normalmente se administra 30 minutos antes de la primera comida del día y en algunas ocasiones debe inyectarse una dosis adicional, más pequeña a la hora de la cena o al acostarse. En algunos pacientes está indicado el uso de insulinas premezcladas que contienen NPH (70%) e insulina regular de acción rápida (30%). Si se utilizan insulinas premezcladas alternándose con otros tipos de insulina, la información sobre su uso al paciente debe ser aún más cuidadosa.
En algunas circunstancias la insulina regular se administra por vía intravenosa; los demás tipos de insulina se administran siempre por vía subcutánea.
La insulina de acción rápida lispro ha sido utilizada con más frecuencia. Su comienzo de acción es de 10 a 15 minutos, que es más rápida que el inicio de 30-60 minutos de la insulina regular. El pico de efecto de la insulina de acción rápida lispro ocurre en 30 a 60 minutos y su duración se extiende hasta 5 horas o menos. Con frecuencia se utiliza con bombas de infusión de insulina.
La insulina glargina es una nuevo agente análogo recombinante de la insulina humana. No debe ser mezclado en la jeringa con ningún otro tipo de insulina y su administración es siempre subcutánea. La insulina glargina tiene un efecto hipoglucémico de larga duración sin un pico de acción definido. Se prescribe una vez al día al acostarse.
La insulina de acción prolongada se prescribe a algunos pacientes. La insulina protamina cinc tiene un comienzo de acción a las 4 a 8 horas, un pico de efecto de entre 14 y 24 horas y una duración total de 36 horas. La suspensión de insulina extendida de cinc tiene un comienzo de acción a las 4 a 8 horas, un pico de efecto de entre 10 y 30 horas y una duración total de 36 horas. Se comercializa una insulina premezclada (70% N y 30% R) con un comienzo de acción a las 4 a 8 horas, un pico de efecto de entre 16 y 18 horas y una duración total mayor de 36 horas. En 2005 ha sido aprobada una nueva insulina de larga duración llamada insulina detemir.
Cuando se administra insulina se debe asegurar de que las unidades que marca la jeringa coinciden con las del vial. Por ejemplo, cuando se pauta insulina U100 (100 unidades en cada mL de líquido) el vial debe marcar U100 y la jeringa debe estar igualmente calibrada. A pesar de que las concentraciones de insulina más utilizadas son U100 y U50 también está disponible U500 para los pacientes que han desarrollado resistencia a la insulina y necesitan dosis mayores para controlar su glucemia. Cuando se administra U500 es necesaria una jeringa calibrada para U500. Es también imperativo entender que no todos los tipos de insulina son compatibles entre sí y pueden no poderse mezclar en una misma jeringa. La insulina regular debe ser clara y a la hora de preparar las mezclas debe ser tomada antes que las insulinas en suspensión (turbias) para evitar contaminación.
Consideraciones por edades
La diabetes mellitus gestacional (DMG) es una entidad que se diagnostica durante el embarazo y comúnmente desaparece unas seis semanas después del posparto. El lactógeno placentario y la destrucción de la insulina materna en la placenta contribuyen a la enfermedad aumentando la resistencia a la insulina en la embarazada. La incidencia de la DMG ha ido en aumento desde mediados de los años noventa, y actualmente se recomienda la monitorización de pruebas de glucosa a las embarazadas entre las semanas 24 y 28 de gestación para descartarla. Cuando se diagnostica la DMG deben implementarse cambios dietéticos y en la realización de ejercicio. Si con estas medidas no se controla la glucemia debe entonces prescribirse tratamiento con insulina.
Debe informarse de los potenciales riesgos para el feto y para la propia gestante durante el embarazo, el parto y posparto si no se realiza correctamente el tratamiento. Un hijo de madre diagnosticada de DMG tiene un 40% más de probabilidades de ser obeso y de desarrollar diabetes mellitus tipo 2 a lo largo de su vida. La madre tiene mayor riesgo de desarrollar DMG en futuros embarazos. Los antidiabéticos orales están contraindicados en el embarazo por su potencial efecto teratógeno sobre el feto.
La población geriátrica también se enfrenta a problemas específicos relacionados con el metabolismo de la glucosa. Si los pacientes ancianos ya han padecido diabetes a lo largo de su vida, pueden decidir ignorar el régimen terapéutico recomendado porque consideran que a esas edades ya no encontrarán mejoras de su calidad de vida. Además las personas ancianas a menudo presentan alteraciones cognitivas que impiden su correcto juicio a la hora de decidir si deciden seguir las recomendaciones dietéticas. Estos pacientes deben ser controlados estrechamente, ya que la dieta es fundamental para disminuir la glucemia.
Educación del paciente
Dentro de los objetivos del tratamiento, es importante incluir la educación de los pacientes y la obtención de datos basales, como constantes vitales y la existencia de enfermedades que producen hipoglucemia como enfermedad de base. Igualmente deben tenerse en cuenta las reacciones adversas. Cuando asesore a los pacientes en relación al tratamiento con insulina incluya los siguientes aspectos:
- Monitorizar estrechamente la glucemia antes de cada comida y antes de la administración de insulina tal y como se indique por el médico.
- Llevar siempre encima azúcar para poder ser utilizado en caso de hipoglucemia.
- Cuando dude de si los síntomas corresponden a hipoglucemia o hiperglucemia, tratarlos con azúcar como si fuesen hipoglucemia, ya que la hipoglucemia progresa rápidamente y la hiperglucemia de forma más lenta.
- Alternar los lugares de inyección de la insulina para prevenir la aparición de lipodistrofia.
- No inyectar insulina en lugares que aparezcan elevados, hinchados, hundidos o en los que sienta prurito.
- Mantener los viales de insulina que tenga en uso a temperatura ambiente, porque a esa temperatura la insulina es menos irritante para la piel.
- Cuando no se necesite, refrigerar la insulina para mantener su estabilidad.
- Seguir estrictamente la dieta prescrita hasta que se le comunique lo contrario.
- Llevar puesto un brazalete de alerta médica para que el personal que pudiera atenderle conozca inmediatamente que es diabético. Indíqueselo al personal que lo asista, compañeros de trabajo y otros que pudieran prestarle ayuda en caso necesario.
- Utilizar solamente una jeringa correctamente calibrada a la misma concentración que la insulina.
- Utilizar solamente el tipo de insulina prescrito por su médico.
Etiología y características de la diabetes mellitus tipo 2
Podemos distinguir una serie de diferencias entre la diabetes tipo 1 y tipo 2. La diabetes mellitus tipo 2 suele aparecer en las personas de edad media, por lo que también se denomina diabetes relacionada con la edad madura. Este es un término poco preciso, ya que cada vez es más frecuente su diagnóstico en niños. Aproximadamente el 90% de todos los pacientes diabéticos son tipo 2.
Al contrario que los pacientes con diabetes tipo 1, aquellos que padecen tipo 2 son capaces de secretar insulina, sin embargo lo hacen en cantidades deficientes. El problema fundamental en la DM tipo 2 es que los receptores para la insulina en los tejidos diana, se han vuelto insensibles para la hormona.
Este fenómeno se denomina resistencia a la insulina y consiste en que las pequeñas cantidades de insulina secretadas no pueden unirse a los receptores celulares con suficiente eficiencia y por tanto consiguen un menor efecto. Los pacientes permanecen con frecuencia asintomáticos durante muchos años, desconociendo que padecen la enfermedad.
Otra diferencia importante es que el mantenimiento de una dieta correcta y ejercicio pueden conseguir aumentar la sensibilidad de los receptores, hasta hacer innecesario el uso de fármacos. Muchos pacientes con DM tipo 2 son obesos, tienen dislipemias y necesitan un plan de estrecha vigilancia para conseguir perder peso y realizar ejercicio con seguridad. Este es un cambio en los hábitos de vida importante para estos pacientes que necesitarán mantenerlos el resto de su vida. Los pacientes con DM tipo 2 mal controlados sufren a menudo las mismas complicaciones que los de tipo 1 (ej. retinopatía, neuropatía y nefropatía).
Farmacoterapia con antidiabéticos orales
La diabetes tipo 2 habitualmente puede controlarse con antidiabéticos orales, que se prescriben como segunda alternativa cuando fallan las medidas dietéticas y el ejercicio. En casos graves, que no responden a la medicación oral o temporalmente en caso de estrés o enfermedad aguda, puede ser necesario el uso de insulina.
Todos los antidiabéticos orales son capaces de disminuir los niveles de glucosa utilizados regularmente. Muchos de ellos pueden potencialmente causar hipoglucemia; por tanto debe realizarse monitorización frecuente de la glucemia. Los antidiabéticos orales no son eficaces para el control de la diabetes tipo 1.
La clasificación de los antidiabéticos orales se basa en su estructura química y en su mecanismo de acción. Los cinco grupos son sulfonilureas, biguanidas, tiazolidinedionas, inhibidores de la alfa glucosidasa y meglitinidas. En el 2006 fue aprobado para su uso un nuevo tipo de fármaco: los inhibidores de la dipeptidil peptidasa-4 (DPP-4). El tratamiento comienza habitualmente con un solo fármaco. Si con la monoterapia no se alcanzan los objetivos propuestos, entonces se utilizan dos fármacos en combinación. Cuando esta alternativa terapéutica también falla, normalmente es necesario el uso de insulina.
Sulfonilureas
Las sulfonilureas fueron los primeros fármacos hipoglucemiantes disponibles. Se dividen en sulfonilureas de primera y de segunda generación. Ambos grupos tienen la misma capacidad hipoglucemiante, pero los de segunda generación presentan menos interacciones con otros fármacos. Su mecanismo de acción consiste en facilitar la liberación de insulina de los islotes pancreáticos y aumentar la sensibilidad de los receptores de la insulina de las células diana. El efecto adverso más frecuente de este grupo de fármacos es la hipoglucemia por tomar medicación en exceso o por no comer adecuadamente. La hipoglucemia producida en este caso puede ser persistente y necesitar la administración de dextrosa para recuperar los niveles normales de glucosa. Otras reacciones adversas incluyen aumento de peso, reacciones de hipersensibilidad, alteraciones gastrointestinales y hepatotoxicidad. Cuando se ingiere alcohol cuando se está con este tratamiento puede aparecer una reacción tipo disulfiram, con enrojecimiento, palpitaciones y náuseas.
Biguanidas
La metformina es el único compuesto de este grupo y su mecanismo de acción consiste en la disminución de la producción hepática de glucosa (gluconeogénesis) y disminución de la resistencia a la insulina. No promueve la liberación de insulina pancreática. Los principales efectos adversos son leves molestias gastrointestinales como anorexia, náusea y diarrea.
Al contrario que las sulfonilureas, la metformina no causa hipoglucemia o aumento de peso. En casos raros se ha comunicado la aparición de acidosis láctica en pacientes con alteración de la función hepática. Una nueva formulación de este compuesto de liberación lenta aprobado en el 2005 permite tomar una única dosis diaria.
Inhibidores de la alfa glucosidasa
Los inhibidores de la alfa glucosidasa, como la acarbosa, bloquean las enzimas a nivel del intestino delgado responsables de la hidrólisis de los carbohidratos complejos en monosacáridos. Puesto que la glucosa debe estar en forma monosacárida para ser absorbida se retrasa su digestión. Estos agentes son bien tolerados y con mínimos efectos secundarios, los más frecuentes leves molestias digestivas, como dolores cólicos abdominales, diarrea o flatulencia. Debe monitorizarse la función hepática ya que se ha comunicado la posible aparición de alteraciones hepáticas. Por sí mismos estos fármacos no producen hipoglucemia, pero sí si se utilizan en combinación con insulina o sulfonilurea o se toma concomitantemente ajo o ginseng.
Tiozolidinedionas
Estos fármacos también llamados glitazonas reducen la glucemia mediante la disminución de la resistencia a la insulina y la inhibición de la gluconeogénesis hepática. Su efecto óptimo se consigue tras 3 o 4 meses de tratamiento.
Los efectos adversos más comunes son retención de líquidos, dolor de cabeza y aumento de peso. No producen hipoglucemia aunque sí pueden tener cierta hepatotoxicidad por lo que debe controlarse la función hepática. En el año 2000 la troglitazona fue retirada del mercado por varias muertes por insuficiencia hepática al parecer relacionadas con su consumo. Estos medicamentos están contraindicados en pacientes con insuficiencia cardíaca o edema pulmonar por su tendencia a la retención de líquidos.
Meglitinidas
Las meglitinidas son una nueva clase de antidiabéticos orales que actúan, de manera similar a las sulfonilureas, estimulando la liberación de insulina desde los islotes pancreáticos. Su acción es corta duración (entre 2 y 4 horas) y su eficacia es similar a las de las sulfonilureas. Son fármacos bien tolerados y su efecto adverso principal es la hipoglucemia.
Nuevos agentes
Se han aprobado algunos fármacos nuevos que actúan sobre el mecanismo de control de la glucosa-incretina.
Las incretinas son hormonas secretadas en el intestino después de las comidas, cuando la glucosa en sangre está elevada. Estas hormonas indican al páncreas que es necesario aumentar la producción de insulina y al hígado que es necesario interrumpir la producción de glucagón. Estas dos acciones producen la disminución de la glucemia. Los pacientes diabéticos son incapaces de producir incretinas en cantidades suficientes, por lo que falla este importante mecanismo de control. Pueden utilizarse compuestos para modificar el sistema de la incretina que actúen a dos niveles: bien simulando su efecto, o bien disminuyendo su destrucción.
La exenatida es un fármaco inyectable que simula el efecto de las incretinas por lo que aumenta la secreción de insulina y en consecuencia retrasa la absorción de glucosa y disminuye la acción del glucagón. Fue aprobada en el 2005 como una alternativa a la metformina en pacientes que no conseguían un control de la glucemia con metformina o sulfonilurea en monoterapia. Debe administrarse por vía subcutánea habitualmente dos veces al día. Entre sus efectos adversos destacan náuseas, vómitos y diarrea en algunos pacientes.
En el 2006 la FDA aprobó el fosfato de sitagliptina, el primer fármaco del grupo de los inhibidores de la dipeptidil peptidasa-4 (DPP-4). Esta enzima actúa destruyendo las incretinas, por lo que su inhibición retrasa esta destrucción. Los niveles de incretinas aumentan y por tanto disminuye la glucemia en pacientes con diabetes tipo 2. Otros compuestos de este grupo se encuentran actualmente en avanzadas fases de ensayos clínicos y pueden ser aprobados en un futuro próximo (entre ellos, vildagliptón, denagliptón, alogliptón y saxagliptón).
La pramlintida es un nuevo fármaco inyectable para el tratamiento de la diabetes tipo 1 y tipo 2 cuya acción se basa en su similitud con la amilina, una hormona pancreática que se secreta después de las comidas y ayuda a regular la glucemia. La pramlintida retrasa la absorción de la glucosa e inhibe la acción del glucagón por los que disminuye la glucemia y favorece la pérdida de peso.
Debido a que los distintos antidiabéticos orales actúan a distintos niveles para conseguir la disminución de la glucemia, y a que tienen distintas propiedades farmacocinéticas, su combinación consigue mejorar los efectos terapéuticos y disminuir los efectos secundarios. Una combinación muy popular es la que mezcla gliburida con metformina en distintas proporciones (1,25/250, 2,5/500 y 5/500).
La American Diabetes Association y la American Association of Clinical Endocrinologists recomiendan que en los pacientes con diabetes tipo 2 mantengan una glucemia preprandial por debajo de 110 mg/dL. En las personas sanas, las células beta secretan insulina en respuesta a los ligeros aumentos de glucosa en la sangre, lo que se denomina una respuesta insulínica aguda. Esta respuesta disminuye a partir de 115 mg/dL y a medida que aumenta la glucemia es menos probable que las células beta respondan con secreción de insulina. Como los pacientes con diabetes tipo 2 necesitan secretar algo de insulina, el mantenimiento de la glucosa por debajo del nivel de 110 mg/dL antes de las comidas optimiza la secreción de insulina.
Los pacientes con DM tipo 2 necesitan reconocer los síntomas del coma hiperosmolar no cetósico (CHNC), que es una urgencia que puede comprometer la vida. Al igual que al comienzo de la cetoacidosis diabética en los pacientes con DM tipo 1, la CHNC se desarrolla lentamente y está ocasionada por la insuficiente insulina circulante. Aparece con más frecuencia en pacientes mayores. La piel aparece enrojecida, seca y caliente, como en la cetoacidosis diabética. Por el contrario, la CHNC no afecta a la respiración. Los niveles de glucosa en sangre pueden superar los 600 mg/dL e incluso alcanzar los 1.000 o 2.000 mg/dL. La CHNC tiene mayor mortalidad que la cetoacidosis diabética.
Consideraciones de enfermería
El papel del personal de enfermería en el manejo del tratamiento con antidiabéticos orales incluye una valoración cuidadosa y una monitorización del estado del paciente así como proporcionar al enfermo toda la información relativa al uso de la medicación prescrita. En la valoración debe incluirse una exploración física, anamnesis médica y psicosocial e información sobre el estilo de vida del paciente. Una valoración exhaustiva es necesaria debido a que la diabetes puede afectar a distintos sistemas del cuerpo. Los factores psicosociales y el estilo de vida, así como el conocimiento de base en relación a la diabetes, puede afectar a la capacidad del paciente de mantener su nivel de glucemia dentro del rango normal. El estilo de vida del paciente y los antecedentes médicos ayudan a determinar qué fármacos utilizar.
Proporcione al paciente información respecto a la importancia de mantener los niveles de glucemia dentro de la normalidad. La glucemia debe monitorizarse diariamente; la excreción urinaria de cuerpos cetónicos debe comprobarse si la glucemia supera los 300 mg/dL. Deben asimismo monitorizarse los aportes y las pérdidas y revisar las pruebas de laboratorio de función hepática. Monitorice a los pacientes en busca de signos y síntomas de infección, ya que las enfermedades pueden cambiar las necesidades de fármacos de los pacientes. Utilice la medicación con precaución en pacientes con alteración de la función renal y hepática así como en los que presentan malnutrición, ya que estos problemas pueden interferir con la absorción y metabolismo de los antidiabéticos orales. Deben también utilizarse con precaución en pacientes con trastornos adrenales o hipofisarios, puesto que las hormonas que segregan afectan al metabolismo de la glucosa. Los antidiabéticos orales están contraindicados si existe hipersensibilidad, cetoacidosis o coma diabético.
También están contraindicados en las mujeres embarazadas o durante el período de lactancia ya que su seguridad en estos casos no ha sido establecida y se sabe que se eliminan por la leche materna.
Administre los antidiabéticos orales tal y como sean prescritos. Algunos de estos fármacos se dan 30 minutos antes del desayuno para que el compuesto alcance el plasma cuando el paciente comience a comer. Otros, como la acarbosa y el miglitol, se administran en cada comida.
Consideraciones por edades
El rápido aumento de la incidencia de la diabetes tipo 2 en niños está convirtiéndose en un motivo de preocupación para las autoridades sanitarias. La enfermedad está alcanzando proporciones epidémicas especialmente en ciertos grupos étnicos como los afroamericanos, los nativos americanos, hispanos, asiáticos y personas oriundas de las islas del pacífico. Los niños que desarrollan diabetes tipo 2 son con frecuencia sedentarios y padecen sobrepeso.
Aunque los dos únicos fármacos aprobados por la FDA para tratar la forma pediátrica de diabetes tipo 2 son insulina y metformina, algunas veces se prescriben otros. La insulina, es el compuesto más eficaz a pesar de que a menudo los niños responden mal al tratamiento diario con insulina. La metformina ha resultado segura y eficaz en niños, aunque a lo largo del tratamiento se deben añadir fármacos de otras clases. Las recomendaciones del tratamiento farmacológico en los niños con diabetes tipo 2 cambian con rapidez como respuesta a los estudios en marcha respecto a las distintas alternativas de tratamiento.
Educación del paciente
La educación de los pacientes en relación con el uso de los antidiabéticos orales debe incluir los objetivos del tratamiento, las razones por las cuales se deben obtener datos basales de constantes vitales y de la posible existencia de alteraciones cardíacas o renales y la posibilidad de aparición de reacciones adversas. Incluya los siguientes aspectos:
- Llevar consigo cualquier tipo de azúcar para tomarlo en caso de hipoglucemia.
- Llevar un brazalete médico de emergencia para alertar al personal de urgencias de que es diabético. Informe a los cuidadores, compañeros de trabajo y otros que pudiera necesitar su asistencia.
- Evitar el consumo de alcohol.
- Monitorizar estrechamente la glucemia tal y como le indique el médico.
- Seguir estrictamente la dieta prescrita a menos que se le indique lo contrario.
- Tragar los comprimidos enteros y no fragmentar los de liberación lenta.
- Tomar la medicación 30 minutos antes del desayuno o tal como se indique por su médico.
- Comunicar a su médico inmediatamente la aparición de nerviosismo, confusión, sudoración excesiva, aumento del pulso o temblores, ya que estos son signos de sobredosis de fármacos e hipoglucemia.
- Comunicar a su médico inmediatamente la aparición de sed excesiva, aumento de la eliminación urinaria, disminución del apetito o fatiga excesiva, ya que estos son signos de dosis insuficiente de fármacos e hiperglucemia.