04. Control de la respiración
Control de la respiración
La ventilación es el movimiento de aire entre la atmósfera y los pulmones; la perfusión es el flujo de sangre hacia dentro y fuera de las porciones de intercambio de gas del pulmón. La ventilación pulmonar se refiere al intercambio total de gases entre la atmósfera y los pulmones, y la alveolar a la ventilación en la porción de intercambio de gas de los pulmones. La distribución de la ventilación alveolar y el flujo de sangre capilar pulmonar varían con el volumen pulmonar y la posición del cuerpo. En la posición recta y a volúmenes pulmonares altos, la ventilación es mayor en las partes más bajas de los pulmones. En esta posición se produce también una disminución del flujo sanguíneo hacia las partes superiores del pulmón, que resulta de la distancia arriba del nivel del corazón y la presión arterial media baja en la circulación pulmonar. La eficiencia del intercambio de gas requiere comparar la ventilación y la perfusión, de modo que entren a los pulmones cantidades iguales de aire y sangre a la porción respiratoria de los pulmones. Dos condiciones interfieren con la comparación de la ventilación y la perfusión: el espacio de aire muerto, en el que las áreas de los pulmones son ventiladas pero no perfundidas y la derivación, en la que las áreas de los pulmones son perfundidas pero no ventiladas.
La difusión de gases en los pulmones se ve afectada por 4 factores: el área superficial disponible para difusión; el espesor de la membrana alveolar-capilar, por la que se difunden los gases; las diferencias en la presión parcial del gas en cualquier lado de la membrana y las características de difusión del gas.
La sangre transporta oxígeno a las células y devuelve dióxido de carbono a los pulmones. El oxígeno se transporta de 2 maneras: en combinación química con hemoglobina y físicamente disuelto en plasma (PO2). La hemoglobina, un portador ciente de oxígeno, participa en el transporte de entre el 98% y el 99% del oxígeno. La relación entre el oxígeno transportado en combinación con hemoglobina y la curva de disociación oxígeno-hemoglobina describe la PO2 de la sangre. El dióxido de carbono es llevado en 3 formas: unido a hemoglobina (30%), dióxido de carbono disuelto (10%) y bicarbonato (60%).
A diferencia del corazón, que tiene propiedades rítmicas inherentes y puede latir de modo independiente del sistema nervioso, los músculos que controlan la respiración requieren entrada continua desde el sistema nervioso. El movimiento del diafragma, músculos intercostales, esternocleidomastoideos y otros músculos accesorios que controlan la ventilación está integrado por neuronas localizadas en el puente de Varolio y la médula. En conjunto, estas neuronas se denominan centro respiratorio (figura 35-23).
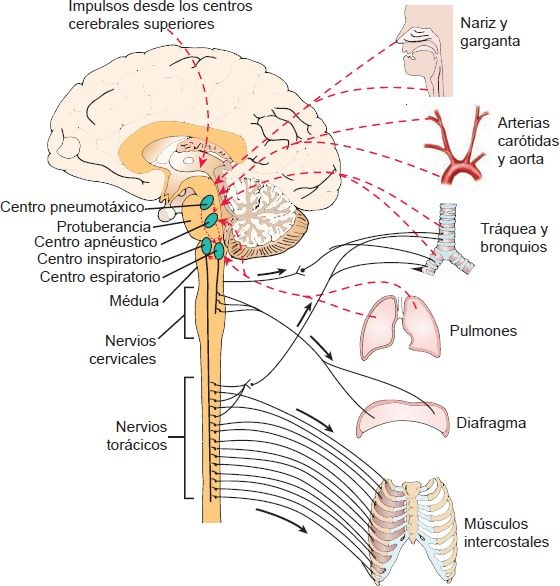
Centro respiratorio
Consiste en 2 agregados bilaterales, densos, de neuronas respiratorias. En el inicio de la inspiración y expiración estas neuronas incorporan impulsos aferentes a las respuestas motoras de los músculos respiratorios. El primer grupo, o dorsal, de neuronas en el centro respiratorio tiene que ver sobre todo con la inspiración. Estas neuronas controlan la actividad de los nervios frénicos que inervan el diafragma e impulsan al segundo grupo, o ventral, de neuronas respiratorias. Se cree que integran la entrada sensorial de los pulmones y las vías respiratorias a la respuesta ventilatoria. El segundo grupo de neuronas, que contiene neuronas inspiratorias y espiratorias, controla las neuronas motoras espinales de los músculos intercostales y abdominales.
Las propiedades de marcapasos del centro respiratorio resultan del ciclo de los 2 grupos de neuronas respiratorias: el centro neumotáxico en la protuberancia (puente de Varolio) superior y el centro apnéustico en la protuberancia inferior (figura 35-23). Estos 2 grupos de neuronas contribuyen a la función del centro respiratorio en la médula. El centro apnéustico tiene un efecto excitatorio en la inspiración y tiende a una inspiración prolongada. El centro penumotáxico desactiva la inspiración y ayuda en el control de la frecuencia respiratoria y el volumen inspiratorio. Las lesiones cerebrales que dañan la conexión entre ambos centros derivan en un patrón de respiración irregular, que consiste en jadeos inspiratorios prolongados interrumpidos por esfuerzos espiratorios.
En el centro respiratorio los axones de las neuronas cruzan en la línea media y descienden en las columnas ventrolaterales de la médula espinal. Las vías que controlan la espiración y la inspiración están separadas espacialmente en la médula, igual que las vías que transmiten reflejos especializados (es decir, tos e hipo) y el control voluntario de la ventilación. Sólo en el nivel de la médula espinal se encuentran los impulsos ventilatorios integrados para producir una respuesta refleja.
Regulación de la respiración
El control de la respiración tiene componentes automáticos y voluntarios. La regulación automática de la ventilación se controla mediante la entrada de 2 tipos de sensores o receptores: quimiorreceptores y receptores pulmonares. Los primeros monitorean los niveles sanguíneos de oxígeno, dióxido de carbono y pH, y ajustan la ventilación para cumplir con las necesidades metabólicas cambiantes del cuerpo. Los receptores pulmonares monitorean los patrones de respiración y la función pulmonar.
La regulación voluntaria de la ventilación integra la respiración con los actos voluntarios como hablar, soplar y cantar. Estos actos, que son iniciados por la corteza motora y premotora, causan una suspensión temporal de la respiración automática. Los componentes automático y voluntario de la respiración son regulados por impulsos aferentes transmitidos al centro respiratorio desde varias fuentes. La entrada aferente desde los centros cerebrales superiores se pone en evidencia por el hecho de que una persona puede alterar de manera consciente la profundidad y frecuencia de respiración. La fiebre, el dolor y la emoción ejercen su influencia a través de los centros cerebrales inferiores. Los aferentes vagales de los receptores sensoriales en los pulmones y las vías respiratorias se integran en el área dorsal del centro respiratorio.
Quimiorreceptores
Las necesidades tisulares de oxígeno y la remoción de dióxido de carbono se regulan mediante quimiorreceptores que monitorean los niveles sanguíneos de estos gases. La entrada desde estos sensores se transmite al centro respiratorio y la ventilación se ajusta para mantener los GSA dentro de un rango normal.
Existen 2 tipos de quimiorreceptores: centrales y periféricos. Los quimiorreceptores más importantes para detectar cambios en la PCO2 de la sangre son los quimiorreceptores centrales, que se localizan en las regiones quimiosensibles, cerca del centro respiratorio, en la médula. Están rodeados de líquido extracelular cerebral y responden a cambios en su concentración de iones hidrógeno (H+). Esta composición del líquido extracelular está gobernada por el líquido cerebroespinal (LCE), el flujo sanguíneo local y el metabolismo tisular. De éstos, el LCE es en apariencia el más importante; está separado de la sangre por la barrera hematoencefálica, la que permite la libre difusión de dióxido de carbono pero no de bicarbonato (HCO 3-) o H+. Con rapidez, el dióxido de carbono se combina con agua para formar ácido carbónico (H2CO3), que se disocia en H+ y HCO-3. Cuando sube la PCO2, el dióxido de carbono de la sangre se difunde hacia el LCE, liberando H+, que luego estimula los quimiorreceptores. Los quimiorreceptores centrales son en extremo sensibles a cambios de corto plazo en la PCO2. Un incremento en los niveles de PCO2 produce un aumento de la ventilación, que alcanza su máximo más o menos en un minuto y luego disminuye si el nivel de PCO2 permanece elevado. Así, las personas que de manera crónica presentan niveles elevados de PCO2 ya no responden a este estímulo para ventilación incrementada, sino que dependen del estímulo proporcionado por una disminución en los niveles de PO2 sanguíneo. En general, esto se presenta en personas que tienen EPOC, y se denomina narcosis por CO.
Los quimiorreceptores periféricos se localizan en los cuerpos carotídeo y aórtico, que se encuentran en la bifurcación de las arterias carótidas comunes y en el arco de la aorta, respectivamente (figura 35-23). Estos quimiorreceptores monitorean los niveles de oxígeno sanguíneo arterial. Aunque los quimiorreceptores periféricos monitorean también el dióxido de carbono, desempeñan un papel mucho más importante en el monitoreo de niveles de oxígeno. Estos receptores ejercen poco control sobre la ventilación hasta que la PO2 cae por debajo de 60 mm Hg.
Así, la hipoxia es el estímulo principal para la ventilación en quienes presentan niveles crónicos elevados de dióxido de carbono. Si a estas personas se les administra el tratamiento de oxígeno a un nivel suficiente para incrementar la PO2 arriba de la necesaria para estimular los quimiorreceptores periféricos, su ventilación podría sufrir una reducción grave.
Receptores pulmonares
Los receptores de la pared pulmonar y torácica monitorean el estado de respiración en términos de la resistencia de vías respiratorias y la expansión pulmonar. Existen 3 tipos de receptores pulmonares: receptores de estiramiento, irritación y yuxtacapilares.
Los receptores de estiramiento se localizan en las capas de músculo liso de las vías respiratorias conductoras. Responden a cambios de presión en las paredes de las vías respiratorias. Cuando se inflan los pulmones, estos receptores inhiben la inspiración y promueven la espiración. Son importantes para establecer los patrones de respiración y minimizar el trabajo de respirar ajustando la frecuencia respiratoria y VT para acomodar cambios en la distensibilidad pulmonar y la resistencia de las vías respiratorias.
Los receptores de irritación se localizan entre las células epiteliales de las vías respiratorias. Son estimulados por gases nocivos, humo de cigarro, polvo inhalado y aire frío. La estimulación de estos receptores origina la restricción de vías respiratorias y un patrón de respiración rápida, poco profunda. Es probable que este patrón de respiración proteja los tejidos respiratorios de efectos dañinos de inhalantes tóxicos. Se considera también que la estimulación mecánica de estos receptores podría asegurar expansión pulmonar más uniforme al iniciar suspiros y bostezos periódicos. También es posible que estén relacionados con la respuesta de broncoconstricción que se presenta en algunas personas con asma bronquial.
Los receptores yuxtacapilares o J se localizan en la pared alveolar, cerca de los capilares pulmonares. Se piensa que detectan la congestión pulmonar. Podrían ser responsables de la respiración rápida, poco profunda, que tiene lugar en el edema pulmonar, embolismo pulmonar y neumonía.
Reflejo tusígeno
La tos es un reflejo mediado neuralmente que protege los pulmones de acumulación de secreciones y de la entrada de sustancias irritantes y destructivas. Es uno de los mecanismos de defensa primarios del tracto respiratorio. El reflejo tusígeno se inicia mediante receptores localizados en la pared bronquial que son muy sensibles a sustancias irritantes y a la presencia de secreciones en exceso. Los impulsos aferentes de estos receptores se transmiten por el nervio vago al centro medular, que integra la respuesta de tos.
El acto de toser requiere por sí mismo inspiración rápida de un gran volumen de aire (por lo general, cerca de 2,5 l), seguida del cierre rápido de la glotis y la contracción forzada de los músculos abdominales y espiratorios. Cuando estos músculos se contraen, las presiones intratorácicas se elevan a niveles de 100 mm Hg o más. En este punto, la apertura rápida de la glotis origina una expulsión explosiva de aire.
Muchas condiciones pueden interferir con el reflejo tusígeno y su función protectora. El reflejo se deteriora en personas cuyos músculos abdominales o respiratorios son débiles, problema que puede ser causado por enfermedades que provocan debilidad o parálisis muscular, por inactividad prolongada o como resultado de intervención quirúrgica relacionada con estos músculos. El descanso en la cama interfiere con la expansión del tórax y limita la cantidad de aire que puede introducirse a los pulmones en la preparación para toser, lo que hace que la tos sea débil e ineficaz.
Las enfermedades que evitan el cierre efectivo de la glotis y los músculos laríngeos interfieren con la producción de un marcado incremento en la presión intratorácica que se requiere para la tos efectiva.
La presencia de un tubo nasogástrico, por ejemplo, podría evitar el cierre de la estructura del vía respiratoria superior y podría fatigar a los receptores para el reflejo tusígeno que se localizan en el área. El reflejo tusígeno se afecta también cuando existe función reducida de los centros medulares que, en el cerebro, integran este reflejo. La interrupción del aspecto de integración central del reflejo tusígeno puede surgir como resultado de enfermedad de esta parte del cerebro o la acción de fármacos que reducen la actividad del centro de la tos.
Disnea
Es una sensación subjetiva que incluye la percepción de dificultad para respirar y la reacción a esa sensación. Con frecuencia, los términos disnea, sofocación y dificultad para respirar (DPR) se emplean de modo intercambiable. La disnea se observa en por lo menos 3 estados principales de enfermedad cardiopulmonar:
- Enfermedades pulmonares primarias, como neumonía, asma y enfisema.
- Cardiopatía caracterizada por congestión pulmonar.
- Trastornos neuromusculares, como miastenia grave y distrofia muscular, que afectan los músculos respiratorios.
Aunque la disnea suele relacionarse con la enfermedad respiratoria, en ciertas personas se presenta también sólo durante el ejercicio, lo que se denomina trastorno reactivo de vías respiratorias inducido por ejercicio o asma inducida por ejercicio.
La causa de la disnea se desconoce, pero para explicar la sensación se han propuesto 4 tipos de mecanismos:
- Estimulación de receptores pulmonares.
- Mayor sensibilidad a cambios en la ventilación percibidos a través de mecanismos del sistema nervioso central.
- Capacidad ventilatoria o reserva de respiración reducidas.
- Estimulación de receptores neurales en las fibras musculares de los intercostales y el diafragma, y de receptores en las articulaciones esqueléticas.
El primero de los mecanismos sugeridos es la estimulación de los receptores pulmonares. Estos receptores son estimulados por la contracción del músculo liso bronquial, el estiramiento de la pared bronquial, la congestión pulmonar y las condiciones que disminuyen la distensibilidad pulmonar. La segunda categoría se centra en los mecanismos del sistema nervioso central que transmiten información a la corteza en relación con la debilidad muscular respiratoria o una discrepancia entre el esfuerzo incrementado de respirar y la contracción muscular respiratoria inadecuada. El tercer tipo de mecanismos se enfoca en una reducción de la capacidad ventilatoria o reserva respiratoria. Por lo general, una reducción de la reserva respiratoria (es decir, ventilación voluntaria máxima que no se utiliza durante una determinada actividad) a menos del 65% al 75% se correlaciona bien con la disnea. El cuarto mecanismo posible es la estimulación de los receptores del músculo y la articulación en la musculatura respiratoria debido a una discrepancia en la tensión generada por estos músculos y el VT que resulta. Una vez estimulados, estos receptores transmiten señales que dan lugar a una apreciación de la discrepancia respiratoria. Al igual que otros síntomas subjetivos, como la fatiga y el dolor, la disnea es difícil de cuantificar, porque depende de la percepción que tenga una persona del problema.
El método más común para medir la disnea es una determinación retrospectiva subjetiva del nivel de actividad diaria en que una persona experimenta la enfermedad. Para este empleo están disponibles varias escalas. Una de éstas utiliza 4 grados de disnea para evaluar la discapacidad. La escala análoga visual podría emplearse para evaluar la dificultad respiratoria que se presenta con una determinada actividad, como caminar una cierta distancia. La escala análoga visual consiste en una línea continua (con frecuencia, 10 cm de longitud) con descriptores como «fácil respirar» en un extremo y «muy difícil respirar» en el otro. La persona evaluada selecciona un punto en la escala que describe la percepción de su disnea.
El tratamiento de la disnea depende de la causa. Por ejemplo, personas con deterioro de la función respiratoria podrían necesitar tratamiento de oxígeno, y aquellas con edema pulmonar podrían requerir medidas para mejorar la función cardíaca. Los métodos para disminuir la ansiedad, reentrenamiento de la respiración y medidas de conservación de la energía podrían emplearse para reducir la sensación subjetiva de disnea.