03. Intercambio y transporte de gases
Las funciones primarias de los pulmones son la oxigenación de la sangre y la remoción de dióxido de carbono. De manera convencional, el intercambio de gas pulmonar se divide en 3 procesos:
- Ventilación-flujo de gases hacia dentro y fuera de los alvéolos pulmonares.
- Perfusión-flujo de sangre en los capilares pulmonares adyacentes.
- Difusión-transferencia de gases entre los alvéolos y los capilares pulmonares.
La eficiencia del intercambio de gas requiere que la ventilación alveolar se dé de manera adyacente a los capilares pulmonares perfundidos.
Ventilación
La ventilación se refiere al intercambio de gases en el sistema respiratorio. Existen 2 tipos de ventilación: pulmonar y alveolar. La ventilación pulmonar alude al intercambio total de gases entre la atmósfera y los pulmones. La ventilación alveolar es el intercambio de gases dentro de la porción de intercambio de los pulmones. La ventilación requiere un sistema de vías respiratorias abiertas y una diferencia de presión que mueva el aire hacia dentro y hacia fuera de los pulmones. Se ve afectada por la posición corporal y el volumen pulmonar; también, por las condiciones de enfermedad relacionadas con el corazón y el sistema respiratorio.
Distribución de la ventilación
La distribución de la ventilación entre el ápice y la base del pulmón varía con la posición del cuerpo y los efectos de la gravedad sobre la presión intrapleural (figura 35-18). Cuando la persona está sentada o de pie, la gravedad ejerce un empuje hacia abajo sobre el pulmón, lo que causa que la presión intrapleural en el ápice del pulmón se vuelva más negativa que en la base del pulmón. Como resultado, los alvéolos en el ápice del pulmón están más expandidos que los de la base del mismo. Lo mismo se cumple para porciones dependientes del pulmón en la posición supina o lateral. En la primera, la ventilación en las partes más bajas (posteriores) del pulmón excede la de las partes más altas (anteriores). En la posición lateral (es decir, recostado de lado), el pulmón dependiente se ventila mejor.
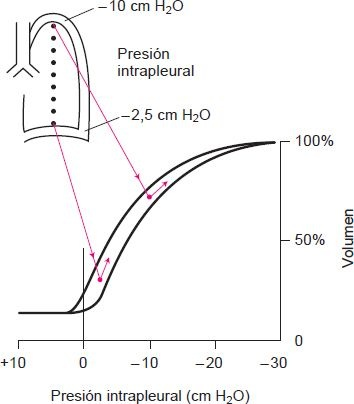
Los volúmenes pulmonares afectan también la distribución de la ventilación. La distensibilidad refleja el cambio de volumen que tiene lugar con un cambio de presión. Es menor en alvéolos completamente expandidos, que tienen dificultad de acomodar más aire y mayor en alvéolos que están menos inflados. Durante la inspiración total en la posición sentada o de pie, las vías respiratorias se abren y el aire entra a las porciones más elásticas del pulmón inferior. En volúmenes pulmonares bajos, sucede lo opuesto. En este caso, la presión pleural en la base del pulmón excede la presión de las vías respiratorias que las comprime, por lo que se reduce mucho la ventilación. Además, en la parte superior del pulmón las vías respiratorias permanecen abiertas para que esta parte se ventile mejor que el fondo.
Incluso a volúmenes pulmonares bajos cierta cantidad de aire permanece en los alvéolos de la porción inferior de los pulmones, evitando así su colapso. De acuerdo con la ley de Laplace, la presión necesaria para vencer la tensión en la pared de una esfera o un tubo elástico es inversamente proporcional a su radio. Por tanto, las vías respiratorias pequeñas cierran primero, capturando algo de gas en los alvéolos. Podría haber un aumento de captación de aire en los alvéolos de la parte inferior de los pulmones en personas mayores y en aquellas con enfermedad pulmonar (ej. enfisema). Se cree que esta afección resulta de una pérdida en las propiedades de retroceso elásticas de los pulmones, de modo que la presión intrapleural, creada por el retroceso elástico del pulmón y la pared torácica, se vuelve negativa. En estas personas, el cierre de las vías respiratorias se presenta al final de los volúmenes pulmonares normales, en vez de los volúmenes pulmonares bajos, lo que permite capturar mayores cantidades de aire, con un incremento resultante en el volumen pulmonar residual.
Espacio de aire muerto
El espacio muerto se refiere al aire que debe ser movido con cada respiración pero que no participa en el intercambio de gas. El movimiento de aire por el espacio muerto contribuye al trabajo de respirar pero no de intercambiar gas. Existen 2 tipos de espacio muerto:
- Espacio muerto anatómico, es aquel contenido en las vías respiratorias conductoras.
- Espacio muerto alveolar, es aquel contenido en la porción respiratoria del pulmón.
El volumen del espacio muerto de las vías respiratorias anatómicas se fija en cerca de 150 ml a 200 ml, según el tamaño corporal. Constituye el aire contenido en la nariz, faringe, tráquea y bronquios. La práctica de una traqueostomía (abertura quirúrgica en la tráquea) disminuye la ventilación del espacio muerto anatómico porque el aire no tiene que moverse por las vías respiratorias nasal y bucal. El espacio muerto alveolar, por lo regular 5 ml a 10 ml, constituye el aire alveolar que no participa en el intercambio de gas. Cuando los alvéolos son ventilados pero desprovistos del flujo sanguíneo, no contribuyen al intercambio de gas y, por tanto, conforman el espacio muerto alveolar.
El espacio muerto fisiológico incluye el espacio muerto anatómico, más el espacio muerto alveolar. En personas con función respiratoria normal, el espacio muerto fisiológico es casi el mismo que el espacio muerto anatómico. Sólo en la enfermedad pulmonar se incrementa el espacio muerto fisiológico. La ventilación alveolar es igual a la ventilación por minuto, menos la ventilación del espacio muerto fisiológico.
Perfusión
Las funciones primarias de la circulación pulmonar consisten en perfundir o proporcionar flujo sanguíneo a la porción de intercambio de gas del pulmón y facilitar el intercambio de gas. Además del intercambio de gas, desempeña otras funciones importantes: filtra la sangre que se mueve del lado derecho al lado izquierdo de la circulación, elimina la mayoría de los tromboémbolos que podrían formarse y sirve como un reservorio de sangre para el lado izquierdo del corazón.
La función de intercambio de gas de los pulmones requiere un flujo continuo de sangre por la porción respiratoria pulmonar. La sangre desoxigenada entra al pulmón por la arteria pulmonar, que tiene su origen en el lado derecho del corazón y entra al pulmón en el hilio, junto con el bronquio primario. Las arterias pulmonares se ramifican de una manera similar a la de las vías respiratorias.
Las arterias pulmonares pequeñas acompañan a los bronquios a medida que se mueven por los lóbulos y se ramifican para alimentar la red capilar que rodea a los alvéolos (figura 35-8). La sangre capilar oxigenada se recolecta en las pequeñas venas pulmonares de los lóbulos. Luego, se mueve alas venas más grandes para ser recolectada en las 4 venas pulmonares grandes que descargan en la aurícula izquierda.
Los vasos sanguíneos pulmonares son más delgados, más elásticos y ofrecen menor resistencia al flujo que los de la circulación sistémica. Además, las presiones en el sistema pulmonar son mucho más bajas (ej. 22/8 mm Hg contra 120/70 mm Hg de presión en la circulación sistémica). La presión y resistencia bajas de la circulación pulmonar acomodan la entrega de diversas cantidades de sangre de la circulación sistémica sin producir signos ni síntomas de congestión. En la circulación pulmonar el volumen es de aproximadamente 500 ml; cerca de 100 ml de este volumen se localiza en el lecho capilar pulmonar. Cuando la entrada de sangre del corazón derecho y la salida de sangre hacia el corazón izquierdo son iguales, el flujo de sangre pulmonar es constante. Pequeñas diferencias entre la entrada y salida pueden producir grandes cambios en el volumen pulmonar si éstas continúan durante muchos latidos. El movimiento de sangre por el lecho capilar pulmonar requiere que la presión arterial pulmonar media sea mayor que la presión venosa pulmonar media. La presión venosa pulmonar se incrementa en la insuficiencia cardíaca lateral izquierda. Esto permite que la sangre se acumule en el lecho capilar pulmonar y cause edema pulmonar.
Distribución del flujo sanguíneo
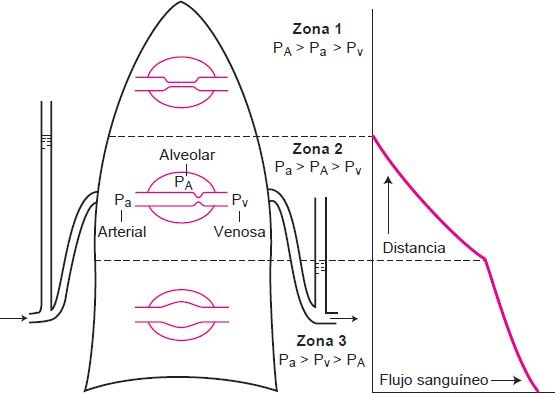
Como con la ventilación, la distribución del flujo de sangre pulmonar es afectada por la posición corporal y la gravedad. En posición recta, la distancia de los ápices superiores del pulmón arriba del nivel del corazón podría exceder las capacidades de perfusión de la presión arterial pulmonar media (cerca de 12 mm Hg). Por tanto, el flujo sanguíneo en la parte superior de los pulmones es menor que en la base o fondo de los pulmones (figura 35-19). En la posición supina, los pulmones y el corazón están al mismo nivel, y el flujo de sangre hacia los ápices y la base de los pulmones se vuelve más uniforme. En esta posición el flujo de sangre hacia las porciones posteriores o dependientes (ej. el fondo del pulmón al recostarse de lado) excede el flujo en el interior o porciones no dependientes de los pulmones.
Vasoconstricción inducida por hipoxia
En la circulación pulmonar los vasos sanguíneos son muy sensibles a los niveles de oxígeno alveolar y experimentan vasoconstricción marcada cuando se exponen a hipoxia. El mecanismo preciso para esta respuesta no está claro. Cuando los niveles de oxígeno alveolar caen abajo de 60 mm Hg, podría presentarse vasoconstricción marcada.
En niveles de oxígeno muy bajos, el flujo local podría casi abolirse. En hipoxia regional, que se presenta con atelectasia, la vasoconstricción se localiza en una región específica del pulmón. En este caso, tiene como efecto dirigir el flujo sanguíneo lejos de las regiones hipóxicas de los pulmones. Cuando la hipoxia alveolar desaparece, se restablece el flujo sanguíneo.
La hipoxia generalizada, que se presenta a gran altura y en personas con hipoxia crónica debido a enfermedad pulmonar, causa vasoconstricción en el pulmón. La hipoxia prolongada puede provocar hipertensión pulmonar y mayor carga de trabajo en el corazón derecho, lo que genera cardiopatía pulmonar. Un pH sanguíneo bajo tiene un efecto similar, en particular cuando se presenta hipoxia alveolar (ej. durante el shock circulatorio).
Derivación
El término derivación se refiere a la sangre que se mueve del lado derecho al lado izquierdo de la circulación sin ser oxigenada. Como con el espacio de aire muerto, existen 2 tipos de derivaciones: fisiológica y anatómica.
En una derivación anatómica la sangre se mueve del lado venoso al lado arterial de la circulación sin pasar por los pulmones. La derivación intracardíaca anatómica de la sangre se presenta con los defectos cardíacos congénitos.
En una derivación fisiológica hay incompatibilidad de la ventilación y la perfusión dentro del pulmón. Esto produce ventilación insuficiente para proporcionar el oxígeno necesario para oxigenar la sangre que fluye por los capilares alveolares. Por lo regular, la derivación fisiológica de sangre resulta de enfermedad pulmonar destructiva que deteriora la ventilación o de insuficiencia cardíaca que interfiere con el movimiento de sangre a través de las secciones pulmonares.
Incompatibilidad de la ventilación y la perfusión
Las propiedades del intercambio de gas del pulmón dependen de la compatibilidad de la ventilación yla perfusión, asegurando que cantidades iguales de aire y sangre entren a la porción respiratoria de los pulmones. El espacio de aire muerto y la derivación producen una incompatibilidad de la ventilación y la perfusión, como se ilustra en la figura 35-20.
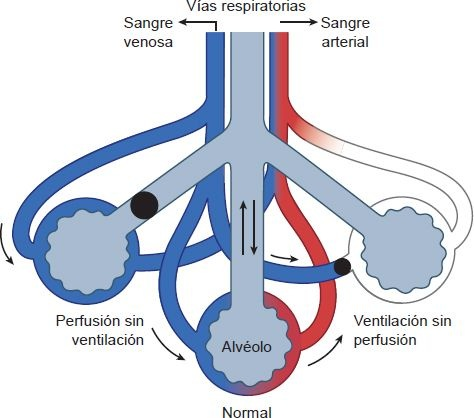
Con la derivación (ilustrada a la izquierda), hay perfusión sin ventilación, lo que da como resultado una relación de ventilación-perfusión baja. Se presenta en afecciones como atelectasia en la que existe obstrucción de las vías respiratorias. Con el espacio de aire muerto, hay ventilación sin perfusión, lo que produce una relación de ventilación-perfusión alta. Tiene lugar en afecciones como embolismo pulmonar, que afecta el flujo sanguíneo hacia una parte del pulmón. La sangre arterial que sale de la circulación pulmonar refleja la mezcla de sangre de áreas ventiladas y perfundidas del pulmón, así como de áreas que no son ventiladas (espacio de aire muerto) o perfundidas (derivación). Muchas de las afecciones que causan incompatibilidad de ventilación y perfusión tienen que ver con el espacio de aire muerto y la derivación. En la enfermedad pulmonar obstructiva crónica, por ejemplo, podría alterarse la ventilación en un área del pulmón y afectarse la perfusión en otra.
Difusión
La difusión tiene lugar en las porciones respiratorias del pulmón y se refiere al movimiento de gases en la membrana alveolar-capilar. La ley de Fick de difusión describe la difusión de gas en el pulmón. Esta ley establece que el volumen de un gas (Vgas) que se difunde a través de la membrana por unidad de tiempo es directamente proporcional a la diferencia de presión parcial del gas (P 1 – P 2), el área superficial (AS) de la membrana y el coeficiente de difusión (D), y es inversamente proporcional al espesor (E) de la membrana (figura 35-21).
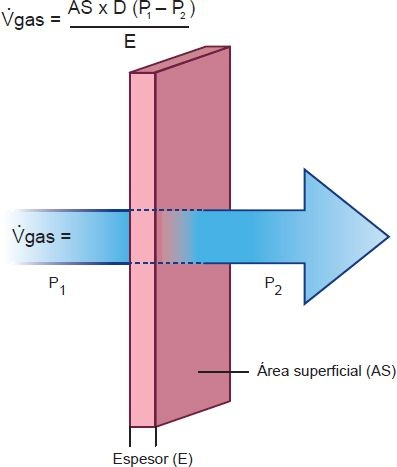
Varios factores influyen en la difusión de gases en el pulmón. La administración de concentraciones altas de oxígeno incrementa la diferencia de presión parcial entre los 2 lados de la membrana y aumenta la difusión del gas. Las enfermedades que destruyen el tejido pulmonar (es decir, el área superficial para difusión) o incrementan el espesor de la membrana alveolar-capilar afectan de modo adverso la capacidad de difusión de los pulmones.
La remoción de un pulmón, por ejemplo, reduce a la mitad la capacidad de difusión. El espesor de la membrana alveolar-capilar y la distancia para difusión se incrementan en personas con edema pulmonar o neumonía. Las características del gas y su peso molecular y solubilidad constituyen el coeficiente de difusión y determinan qué tan rápido se difunde un gas por las membranas respiratorias. Por ejemplo, el dióxido de carbono se difunde 20 veces más rápido que el oxígeno como resultado de su mayor solubilidad en las membranas respiratorias.
La capacidad de difusión proporciona una medida de la tasa de transferencia de gas en los pulmones por gradiente de presión parcial. Dado que no puede medirse la diferencia inicial alveolar-capilar para el oxígeno, se utiliza el monóxido de carbono (CO) para determinar la capacidad de difusión. Medir CO tiene varias ventajas:
- Su captación no está limitada por la difusión o el flujo sanguíneo.
- En esencia, no hay CO en la sangre venosa.
- Su afinidad hacia la hemoglobina es 210 veces la del oxígeno, lo que asegura que su presión parcial será esencialmente cero en el capilar pulmonar.
La técnica más común para realizar esta medición es la prueba de respiración simple, que consiste en respirar CO diluido una sola vez y mantener la respiración 10 segundos. La capacidad de difusión puede calcularse mediante el volumen pulmonar y el porcentaje de CO en los alvéolos al comienzo y al final de haber mantenido la respiración por 10 segundos.
Transporte de oxígeno y dióxido de carbono
Aunque los pulmones se encargan del intercambio de gases con el medio externo, es la sangre la que transporta estos gases entre los pulmones y los tejidos corporales. La sangre lleva oxígeno y dióxido de carbono en estado disuelto físicamente y en combinación con hemoglobina. El dióxido de carbono se convierte también en bicarbonato y se transporta en esa forma.
El oxígeno y dióxido de carbono disueltos ejercen una presión parcial que se designa de la misma manera que las presiones parciales en el estado gaseoso. En el entorno clínico, las mediciones de gas sanguíneo se emplean para determinar la presión parcial del oxígeno (PO2) y dióxido de carbono (PCO2)en la sangre. En general, la sangre arterial se utiliza para medir gases sanguíneos. La sangre venosa no se utiliza porque los niveles venosos de oxígeno y dióxido de carbono reflejan las demandas metabólicas de los tejidos y no la función de intercambio de gas de los pulmones. Por lo general, la PO2 de la sangre arterial está arriba de 80 mm Hg, mientas que la PCO2 está en un intervalo de 35 mm Hg a 45 mm Hg (tabla 35-3). En general, los GSA son lo mismo o casi lo mismo que la presión parcial de los gases en los alvéolos. La PO2 arterial se escribe con frecuencia como PaO 2 y la PO2 alveolar como PAO 2, con los mismos tipos de designaciones que se utilizan para PCO2. En este texto se emplean PO2 y PCO2 para designar los niveles arterial y alveolar de los gases.
Transporte de oxígeno
El oxígeno se transporta en 2 formas:
- En combinación química con hemoglobina.
- En estado disuelto.
La hemoglobina lleva cerca del 98% al 99% del oxígeno en la sangre y es el principal transportador de oxígeno. Del 1% al 2% restante del oxígeno se lleva en estado disuelto. Sólo la forma disuelta del oxígeno pasa por la pared capilar, se difunde por la membrana celular y se hace a sí mismo accesible para el empleo en el metabolismo celular. El contenido de oxígeno (medido en ml/100 ml) de sangre incluye el oxígeno llevado por la hemoglobina y el que está en estado disuelto.
Transporte de hemoglobina
La hemoglobina es un portador de oxígeno muy eficiente. La hemoglobina con oxígeno ligado se llama oxihemoglobina. Cuando se elimina el oxígeno, se llama hemoglobina desoxigenada o reducida. Cada gramo de hemoglobina lleva cerca de 1,34 ml de oxígeno cuando está saturada del todo. Ésto significa que una persona con un nivel de hemoglobina de 14 g/100 ml lleva 18,8 ml de oxígeno por 100 ml de sangre.
En los pulmones, el oxígeno se mueve por la membrana alveolar-capilar, a través del plasma y hacia los eritrocitos, en donde forma un enlace débil y reversible con la molécula de hemoglobina.
En los pulmones normales, este proceso es rápido. Por tanto, incluso con una frecuencia cardíaca rápida, la hemoglobina está casi completamente saturada con oxígeno durante el poco tiempo que pasa en los capilares pulmonares. Cuando el oxígeno sale de los capilares en respuesta a las necesidades de los tejidos, la saturación de hemoglobina disminuye. Cuando la sangre sale del lado izquierdo del corazón está saturado cerca del 95% al 97%. Luego, cuando la sangre venosa mixta regresa al lado derecho del corazón, decrece a alrededor del 75% de saturación.
Oxígeno disuelto
La presión parcial del oxígeno representa el nivel de oxígeno disuelto en el plasma. La cantidad de oxígeno disuelto depende de su presión parcial y su solubilidad en el plasma.
En el pulmón normal a 760 mm Hg de presión atmosférica, la PO2 de la sangre arterial es aproximadamente 100 mm Hg. La solubilidad del oxígeno en el plasma es fija y muy pequeña. Por cada 1 mm Hg de PO2 presente, 0,003 ml de oxígeno se disuelven en 100 ml de plasma. Esto significa que a una PO2 arterial normal de 100 mm Hg, la sangre lleva sólo 0,3 ml de oxígeno disuelto en cada 100 ml de plasma. Esta cantidad (cerca del 1%) es muy pequeña, comparada con la que puede llevarse en una cantidad igual de sangre cuando el oxígeno se une a hemoglobina.
Sin embargo, esta pequeña cantidad puede volverse un modo de transporte decisivo en casos de intoxicación por CO, cuando la mayor parte de los sitios de hemoglobina están ocupados por CO y no están disponibles para transportar oxígeno. La utilización de una cámara hiperbárica, en la que el 100% de oxígeno puede administrarse a presiones atmosféricas altas, incrementa la cantidad de oxígeno que puede llevarse en estado disuelto y se utiliza en personas con quemaduras graves, en especial las que impactan el sistema respiratorio, y en aquellas que presentan múltiples tipos de heridas, como las inmunodeprimidas o que tienen diabetes con problemas de cicatrización.
Afinidad de enlace de la hemoglobina con el oxígeno
La eficiencia del sistema de transporte de hemoglobina depende de la capacidad de la molécula de hemoglobina para unirse al oxígeno en los pulmones y liberarlo cuando se requiera en los tejidos. El oxígeno que permanece unido a la hemoglobina no participa en el metabolismo tisular. El término afinidad alude a la capacidad de la hemoglobina para unirse al oxígeno. La hemoglobina se une al oxígeno con más facilidad cuando se incrementa su afinidad y se libera más fácilmente cuando disminuye su afinidad.
La molécula de hemoglobina se compone de 4 cadenas polipeptídicas con un grupo hem que contiene hierro. Dado que el oxígeno se une al átomo de hierro, cada molécula de hemoglobina puede enlazarse a 4 moléculas de oxígeno cuando se satura por completo. El oxígeno se une beneficiando a los grupos hem en la molécula de hemoglobina. Después que la primera molécula de oxígeno se une a la hemoglobina, la molécula experimenta un cambio en su forma. Como resultado, la segunda y tercera moléculas se unen más fácilmente, y el enlace de la cuarta molécula es aún más fácil. De un modo similar, la descarga de la primera molécula de oxígeno mejora la descarga de la siguiente molécula, y así sucesivamente. De este modo, la afinidad de la hemoglobina hacia el oxígeno cambia con la saturación de hemoglobina.
La afinidad de la hemoglobina hacia el oxígeno se ve afectada también por el pH, la concentración del dióxido de carbono y la temperatura corporal. Se une al oxígeno más fácilmente en condiciones de pH incrementado (alcalosis), concentración reducida de dióxido de carbono y temperatura corporal reducida, y se libera con mayor facilidad si se reduce el pH (acidosis), aumenta la concentración de dióxido de carbono y si hay fiebre. Por ejemplo, el metabolismo tisular incrementado genera dióxido de carbono y ácidos metabólicos, y por tanto, disminuye la afinidad de la hemoglobina hacia el oxígeno. El calor es también un subproducto del metabolismo tisular, lo que explica el efecto de la fiebre en el enlace de oxígeno.
Los eritrocitos contienen un intermediario metabólico llamado 2,3-difosfoglicerato (2,3-DFG) que afecta asimismo la afinidad de la hemoglobina hacia el oxígeno. Un incremento en 2,3-DFG mejora la descarga de oxígeno de la hemoglobina en el nivel tisular. Las condiciones que incrementan 2,3-DFG son el ejercicio, la hipoxia que se presenta a gran altitud y la enfermedad pulmonar crónica.
Curva de disociación del oxígeno
La relación entre el oxígeno transportado en combinación con hemoglobina y la PO2 de la sangre se describe mediante la curva de disociación oxígenohemoglobina, que se muestra en la figura 35-22. El eje de las x de la gráfica ilustra la PO2 u oxígeno disuelto.
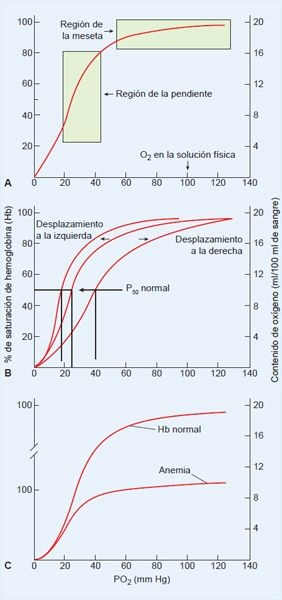
Refleja la presión parcial del oxígeno en los pulmones (es decir, la PO2 es aproximadamente 100 mm Hg cuando se respira aire ambiente, pero puede subir a 200 mm Hg o más cuando se respira aire enriquecido con oxígeno). El eje y izquierdo ilustra la saturación de hemoglobina o la cantidad de oxígeno que se lleva en la hemoglobina. El eje y derecho ilustra el contenido de oxígeno o cantidad total del contenido de oxígeno que se lleva en la sangre.
Transporte de dióxido de carbono
El dióxido de carbono se transporta en la sangre en 3 formas:
- Como dióxido de carbono disuelto (10%).
- Unido a hemoglobina (30%).
- Como bicarbonato (60%).
El equilibrio acidobásico se ve afectado por la cantidad de dióxido de carbono disuelto y el nivel de bicarbonato en la sangre.
Cuando el dióxido de carbono se forma durante el proceso metabólico, se difunde de las células hacia los espacios tisulares y luego hacia los capilares. La presión parcial del gas y su coeficiente de solubilidad (0,03 ml/100 ml/1 mm Hg de PCO2) determinan la cantidad de dióxido de carbono disuelto que puede llevarse en el plasma. El dióxido de carbono es 20 veces más soluble en plasma que el oxígeno. Así, el estado disuelto desempeña un papel mayor en el transporte de dióxido de carbono, en comparación con el oxígeno.
La mayor parte del dióxido de carbono se difunde hacia los eritrocitos, donde forma ácido carbónico o se combina con la hemoglobina. El ácido carbónico (H2CO3) se forma cuando el dióxido de carbono se combina con agua (CO2 + H2O = H+ + HCO-3). El proceso se cataliza por una enzima llamada anhidrasa carbónica, que se presenta en grandes cantidades en los eritrocitos; ésta, incrementa la tasa de la reacción entre el dióxido de carbono y el agua en casi 5.000 veces. El ácido carbónico se ioniza con facilidad para formar iones bicarbonato (HCO-) e hidrógeno (H+). El ion hidrógeno se combina con la hemoglobina, que es una poderosa solución amortiguadora acidobásico, y el ion bicarbonato se difunde hacia el plasma en intercambio por un ion cloruro. Este intercambio es posible gracias a una proteína especial portadora de bicarbonato-cloruro en la membrana del eritrocito. Como resultado del desplazamiento de bicarbonato-cloruro, el contenido de cloruro y agua del eritrocito es mayor en las sangre venosa que en la arterial.
Además de la reacción mediada por la anhidrasa carbónica con agua, el dióxido de carbono reacciona directamente con la hemoglobina para formar carbaminohemoglobina. La combinación de dióxido de carbono con hemoglobina es una reacción reversible relacionada con un enlace débil. Esto permite el transporte de dióxido de carbono de los tejidos a los pulmones, donde se libera hacia los alvéolos para intercambio con el medio externo. La liberación de oxígeno de la hemoglobina en los tejidos mejorará el enlace del dióxido de carbono a la hemoglobina. En los pulmones, la combinación de oxígeno con hemoglobina desplaza dióxido de carbono. El enlace de dióxido de carbono a hemoglobina se determina por la naturaleza ácida de esta última. El enlace con dióxido de carbono ocasiona que la hemoglobina se vuelva un ácido más fuerte. En los pulmones, la hemoglobina altamente ácida tiene una menor tendencia a formar carbaminohemoglobina y el dióxido de carbono se libera de la hemoglobina hacia los alvéolos. En los tejidos, la liberación de oxígeno de la hemoglobina provoca que la hemoglobina sea menos ácida; así, se incrementa su capacidad para combinarse con dióxido de carbono y formar carbaminohemoglobina.