Teorema del tratamiento del estrés en implantología
La odontología es una faceta singular de la medicina, que combina la ciencia con una forma de arte. Algunos aspectos en el ámbito dental hacen énfasis en esta forma de arte, como en la estética dental, que trata con el color y la forma del diente para mejorar la sonrisa del paciente y el aspecto general. En cualquier caso, la razón primaria por la que se aplica el término doctor a la profesión dentaria es debido a las ciencias dentales. Estas pueden separarse en un componente biológico y un componente biomecánico. Para los odontólogos generalistas, se hace énfasis en los aspectos biológicos de la salud oral. Las complicaciones comunes relacionadas con la dentición natural tienen primariamente orígenes biológicos, teniendo como ejemplos las enfermedades periodontales, caries, y problemas endodóncicos.
Una combinación de factores biológicos y biomecánicos es la responsable del fracaso de las prótesis fijas dentosoportadas. Las cuatro complicaciones más comunes para las prótesis fijas de tres unidades son 1) las caries, 2) los problemas endodóncicos, 3) la falta de retención protésica y 4) la fractura de la porcelana. Las complicaciones biológicas suelen producirse con mayor frecuencia (del 11 al 22 %) en comparación con las biomecánicas (del 7 al 10%), pero ambos aspectos deberían ser comprendidos por el odontólogo.
La odontología implantológica involucra siempre a la sustitución de los dientes. Cuando se informa de complicaciones con los implantes, la mayoría de los problemas se relacionan más con los aspectos científicos del propio implante que con los estéticos. Pero, a diferencia de los dientes naturales, los aspectos biológicos de la odontología implantológica presentan relativamente pocas complicaciones. Por ejemplo, el desarrollo de una interfase directa hueso-implante es en gran parte biológico. La mayoría de los informes recientes indican que la fase quirúrgica de los implantes forman una buena interfase en más del 95% de las ocasiones, independientemente del sistema de implantes empleado. De ahí que el aspecto biológico del campo sea muy predecible.
Las complicaciones más comunes relacionadas con los implantes son los problemas biomecánicos que se producen una vez cargado el implante. Un repaso a la literatura referente a los fracasos de implantes indica que estos problemas se producen primariamente durante los 18 meses posteriores a la carga inicial del implante. Estos fracasos iniciales de carga del implante se producen con más frecuencia en los de tipo de hueso más blando (fracaso del 16%) o en los implantes de menor longitud (fracaso del 17%). Estos dos grupos de fracasos están causados típicamente por factores biomecánicos. El hueso blando es demasiado débil para las fuerzas oclusales aplicadas en los implantes, o los implantes más cortos soportan demasiado estrés en la interfase hueso-implante (fig. 4-1).
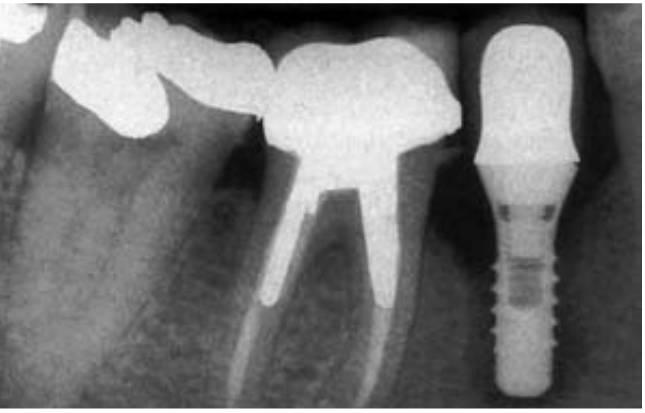
Las complicaciones más comunes que no conllevan al fracaso del implante suelen tratarse también de problemas biomecánicos. Las sobredentaduras implantológicas tienen problemas de fracturas o complicaciones en los retenedores (30 %) y fracturas de las prótesis removibles (12 %). En las prótesis fijas implantosoportadas la fractura de la carilla de resina acrílica (22 %), el aflojamiento del tornillo protésico o del pilar (7-10%), la fractura de la porcelana (7%), y la fractura del metal en la prótesis (3 %) son algunos ejemplos de complicaciones comunes. Además, los componentes implantológicos (del 2 al 4 %) e incluso el cuerpo de los implantes (del 1 al 2%) pueden fracturarse (cuadro 4-1). En otras palabras, las complicaciones mecánicas sobrepasan en número a los problemas biológicos implantológicos.
Cualquier estructura de ingeniería compleja fracasará en su «eslabón mas débil» y las estructuras implantológicas dentales no son una excepción. Un concepto general en ingeniería es determinar las causas de las complicaciones y desarrollar un sistema para reducir las condiciones que causan los problemas. Las causas más comunes de complicaciones relacionadas con implantes se centran alrededor del estrés. Así, el plan de tratamiento total debería 1) evaluar los mayores factores de fuerza en el sistema y 2) establecer mecanismos para proteger el sistema global implante-hueso-prótesis.
Fracaso quirúrgico
Existen numerosas razones para que un implante fracase en su integración inicial con el hueso. Las causas primarias del fracaso están relacionadas con un excesivo calor durante la preparación de la osteotomía o un exceso de presión en la interfase implante-hueso en el momento de la inserción del implante21 (fig. 4-2). La presión excesiva en la inserción del implante se observa con más frecuencia con los diseños del cuerpo de tipo tornillo cónico. La fuerza de inserción del torque sobre un implante de diseño de cuerpo de tornillo cónico puede aplicar fuerzas excesivas sobre el hueso, lo que conlleva a una reabsorción y fracaso del implante.
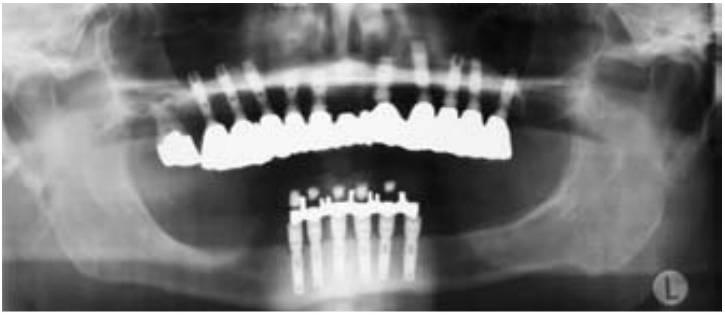
Una causa adicional del fracaso quirúrgico son los micromovimientos del implan te mientras se establece la interfase en desarrollo (fig. 4-3). Un brazo fracturado es inmovilizado para evitar movimiento en el foco de fractura para disminuir el riesgo de una falta de unión fibrosa. Se ha observado que movimientos tan pequeños como de 20 micrones pueden causar la formación de una interfase fibrosa en el foco de fractura. Brunski observó el desarrollo de una interfase de tejido fibroso cuando un implante dental se mueve más de 100 micrones durante la cicatrización inicial. El protocolo original Bránemark empleaba un enfoque quirúrgico de dos etapas. Uno de los principales motivos de este concepto era el de colocar el implante en la región de hueso de la cresta o por debajo de ella para disminuir el riesgo de movimiento del implante durante la cicatrización ósea inicial. Schroeder sugirió también un período de cicatrización sin cargas para los implantes, aunque el implante fuera colocado en los tejidos gingivales o ligeramente superior a estos.

Las fuerzas oclusales aplicadas sobre una prótesis removible sobre un implante en cicatrización pueden causar también la apertura de la línea de incisión de los tejidos blandos y retrasar la cicatrización de los mismos. Estas fuerzas oclusales pueden afectar también al hueso marginal alrededor del lecho implantológico en desarrollo. Transferir estas fuerzas a una prótesis mucosoportada situada por encima puede causar micromovimiento en la interfase implante-hueso, independientemente de que el implante esté cicatrizando por encima o por debajo de los tejidos gingivales. El estrés aplicado a un implante en fase de cicatrización aumenta el riesgo de complicaciones. Por otra parte, algunos informes clínicos multicéntricos indican que un cirujano experimentado puede obtener fijaciones rígidas tras una colocación quirúrgica en el 99 % de las ocasiones. El componente quirúrgico del fracaso implantológico suele representar el menor riesgo asociado con el tratamiento implantológico global.
Fracaso temprano por carga
En algunas ocasiones, un implante puede fracasar poco tiempo después de haberse empezado a «integrar» en el hueso. Antes del fracaso, el implante parece tener una fijación rígida, y todos los indicadores clínicos están dentro de la normalidad. En cualquier caso, una vez que el implante está cargado, se vuelve móvil en el plazo de entre 6 y 18 meses (fig. 4-1). Esto ha sido denominado fracaso temprano por carga por Misch y Jividen. La causa de este fracaso temprano por carga suele ser un estrés excesivo para la interfase hueso-implante. Isidor permitió la integración de ocho implantes en mandíbulas de monos. Las coronas se sujetaban a los implantes cicatrizados con un exceso de contactos oclusales prematuros. Sobre un período de 20 meses, seis de los ocho implantes fracasaron (fig. 4-4). En estos mismos animales, ocho implantes integrados sin cargas oclusales llevaban unas anillas colocadas en el margen gingival para aumentar la retención de placa. Ninguno de estos implantes fracasó a lo largo de los siguientes 20 meses. Los autores concluyeron que en este modelo de animal, el estrés oclusal biomecánico era un mayor factor de riesgo para el fracaso temprano por carga que el componente biológico de la placa bacteriana.
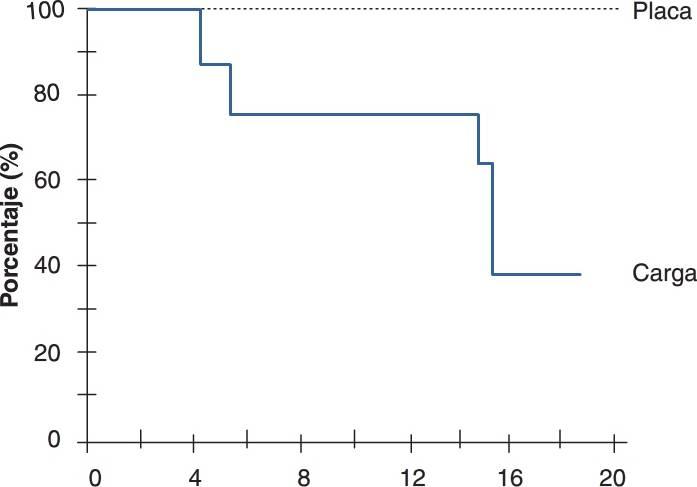
El fracaso de la carga temprana es peor para el odontólogo que cuando se produce un fracaso quirúrgico ya que el paciente puede culpabilizar al odontólogo restaurador. Aunque esto ya es sufidentemente negativo, además el odontólogo habrá empleado entre dos y cinco sesiones para restaurar el implante además de los gastos de laboratorio. El fracaso temprano por carga se relaciona con la cantidad de fuerza aplicada a la prótesis y la densidad del hueso alrededor del implante, y puede afectar al 15% de las restauraciones implantológicas. Se han observado en los tipos de hueso más blandos fracasos tempranos por carga de hasta el 40%, a causa de la sobrecarga biomecánica. No existen informes en la literatura que correlacioen esta extremadamente alta incidencia de fracasos tempranos de implantes con aquellas complicaciones relacionadas con la anchura biológica observadas en la práctica dínica.
Impacto de la sobrecarga oclusal en los componentes mecánicos
Aflojamiento del tornillo
El aflojamiento del tornillo del pilar se ha detectado en una media global del 6 % de las prótesis sobre implantes. En el caso de las coronas dentales individuales esto sucedía en el 25 % en los diseños y conceptos iniciales de los tornillos (incluso hasta un 45 %). Estudios recientes indican que esta proporción se ha reducido a un promedio global del 8%, siendo para las prótesis fijas de múltiples unidades una media del 5 % y para las sobredentaduras de implantes del 3 % (fig. 4-5). Cuanto mayor sea el estrés aplicado a la prótesis (dientes individuales frente a las sobredentaduras), mayor será el riesgo de aflojamiento del tornillo del pilar. Los voladizos aumentan también el riesgo de aflojamiento del tornillo, ya que se incrementan las fuerzas en relación directa con la longitud del mismo. Cuanto mayor sea la altura de la corona sujeta al pilar, mayor será la fuerza aplicada en el tornillo, y mayor el riesgo de aflojamiento del mismo.
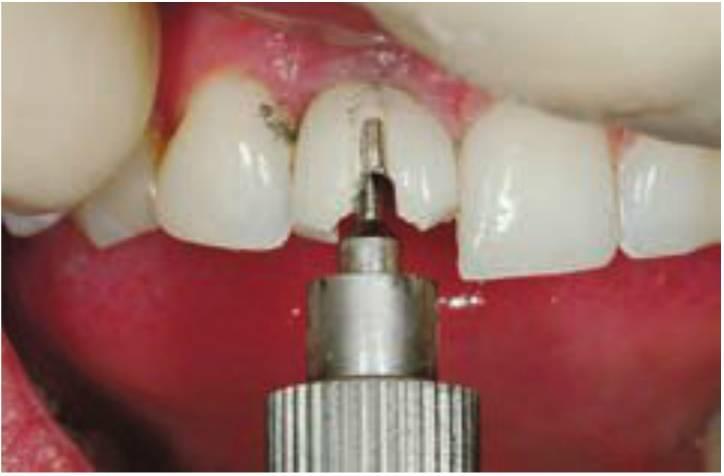
La altura o profundidad de un componente antirotatorio del cuerpo del implante puede afectar también a la cantidad de fuerza aplicada al tornillo del pilar. Cuanto mayor sea la altura (o profundidad) del hexágono menor será el estrés aplicado al tornillo y menor será el riesgo correspondiente de aflojamiento del tornillo del pilar. La dimensión de la plataforma sobre la que se encuentra asentado el pilar es aún más importante que la altura del hexágono. Los implantes de diámetro más ancho, con plataformas de dimensiones más anchas, reducen las fuerzas aplicadas a un tornillo de pilar y cambian el arco de desplazamiento del pilar sobre el módulo de la cresta. El aflojamiento del tornillo puede reducirse también aplicando sobre el tornillo una fuerza de precarga mediante una llave de torque. Por tanto, se pueden emplear métodos protésicos para disminuir el estrés sobre el tornillo de los pilares o también enfoques de ingeniería para disminuir el estrés o aumentar la fijación de la rosca disminuyendo así la incidencia de las complicaciones relacionadas con el aflojamiento del tornillo.
Fracturas por fatiga
Los materiales siguen una curva de fatiga, que está relacionada con el número de ciclos y la intensidad de la fuerza. Existe una fuerza tan grande que un solo ciclo de la misma puede producir una fractura (ej. un golpe de kárate a un trozo de madera). En cualquier caso, si una fuerza de menor magnitud golpea repetidamente un objeto, provocará también una fractura. El perchero de metal que es doblado no se romperá la primera vez, pero si es doblado en repetidas ocasiones el material se acabará fracturando, no porque la última vez haya sido la más fuerte sino debido a la fatiga. De hecho, cuando el paciente dice que mojó el pan en su café y se lo metió en la boca justo antes de la fractura de la porcelana/del tornillo del pilar/del sellado por el cemento/de las prótesis con voladizo, puede haber sido «la gota que colmó el vaso».
La fractura del tornillo de la prótesis se ha observado tanto en las fijas parciales como en las prótesis fijas completas, con una incidencia media del 4 % con un margen del 0 hasta el 19% (fig. 4-6). Los tornillos de los pilares suelen tener un diámetro más grande de ahí que las fracturas sean menos frecuentes, con una incidencia media del 2 % con un margen del 0,2 al 8 % (fig. 4-7). Se han observado también las fracturas de la estructura metálica con una media del 3 % en las fijas completas y las restauraciones con sobredentaduras, con un margen del 0 al 27 % (fig. 4-8). La fractura del cuerpo del implante presenta la menor incidencia en este tipo de complicaciones, con una incidencia del 1% (fig. 4-9). Esta condición se observa con mayor frecuencia en las prótesis fijas a largo plazo y pueden contar para la mayoría de los fracasos a largo plazo. Las fracturas de las carillas de resina de las prótesis fijas sobre implantes presentan una media del 22 %, las fracturas del retenedor/clip de las sobredentaduras una media del 17%, las fracturas de la carilla de porcelana una media del 14%, las fracturas de sobredentadura una media del 12%, y las fracturas de una resina de base acrílica una media del 7%. Las fracturas relacionadas con las prótesis sobrepasan en número a las relacionadas con los componentes de los implantes.

Las restauraciones descementadas (o peor, las prótesis parcialmente descementadas) suelen producirse cuando se aplican cargas crónicas a la interfase de cemento, o cuando fuerzas transversales están presentes (al igual que con los voladizos). Las fuerzas del cemento son más débiles con cargas transversales. El cemento de fosfato de zinc puede resistir una fuerza compresiva de 12.000 psi pero solo puede resistir una fuerza transversal de 500 psi. Es interesante observar que el hueso es resistente también a la compresión pero es un 65 % más débil a las fuerzas transversales. Se ha observado en relación con las cargas transversales el mismo escenario para la porcelana u otros materiales oclusales. Como consecuencia, la evaluación, el diagnóstico, y la modificación de los planes de tratamiento relacionados con las condiciones de estrés tienen una importancia considerable. De ahí que, una vez que el odontólogo implantólogo ha identificado las fuentes de fuerza adicional sobre el sistema del implante, se altera el plan de tratamiento en un intento de minimizar su impacto negativo en la longevidad del implante, del hueso, y la restauración final.
Pérdida de hueso marginal
Se ha observado la pérdida ósea en la cresta alrededor de la porción transmucosa de los implantes dentales durante décadas. Se ha descrito en la región crestal de implantes osteointegrados con éxito independientemente del enfoque quirúrgico. Puede incluir desde la pérdida de hueso marginal hasta un fracaso completo del implante y disminuye enormemente después del primer año (cuadro 4-2). Para los implantes de lámina de una sola pieza, este fenómeno se describió como un «socavamiento» y se producía después de la carga del implante.
Trauma oclusal: pérdida de hueso
Adell y cols, fueron los primeros en cuantificar y notificar la pérdida de hueso marginal. El estudio indica también la mayor magnitud y aparición de la pérdida de hueso durante el primer año de la carga del implante, con una media de 1,2 mm durante este lapso de tiempo, con un margen de 0 a 3 mm. Este estudio midió la pérdida de hueso desde la primera rosca como línea de base de 0 mm, y no como el nivel original del hueso de la cresta en la inserción, que estaba 1,8 mm por encima de este punto de base. De ahí que la media de pérdida ósea en la cresta durante el primer año sea de 3,3 mm alrededor de los implantes observados (fig. 4-10). Los años siguientes al primero mostraron una media de entre 0,05 a 0,13 mm de pérdida de hueso al año. Otros estudios notificaban una media de pérdida ósea durante el primer año de 0,93 mm, con un margen de entre 0,4 a 1,6 mm y una media de pérdida de 0,1 mm después del primer año. La pérdida inicial del hueso de la cresta se ha observado con tanta frecuencia que el criterio propuesto para el éxito de los implantes no suele incluir siquiera la cantidad de pérdida ósea durante el primer año.
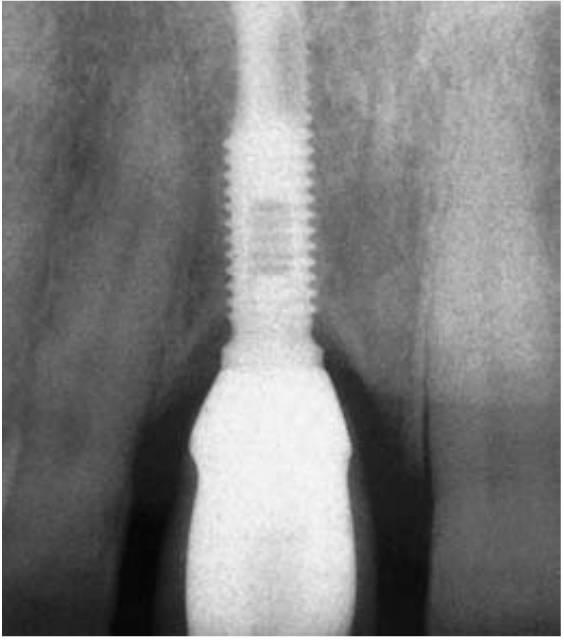
La pérdida transósea inicial alrededor de un implante produce un patrón en forma de V o de U, que ha sido descrita como zanja o socavado alrededor del implante. Las hipótesis actuales sobre la causa de la pérdida de hueso en la cresta van desde el levantamiento del periostio durante la cirugía, la preparación de la osteotomía para el implante, la posición del espacio entre el pilar y el cuerpo del implante, el micromovimiento de los componentes del pilar, la invasión bacteriana, el establecimiento de una anchura biológica, hasta los factores tensionales.
La comprensión de las causas de la pérdida de hueso marginal en la cresta alrededor de los implantes dentales y del fracaso implantológico inicial es crítica en la prevención de dichos sucesos, fomentando la salud periimplantaria, y mejorando las medias de éxito de los implantes a largo plazo y, principalmente, el éxito de la prótesis sobre implantes. La pérdida ósea marginal en la cresta puede influir en la estética al estar directamente relacionada la altura del tejido blando (ej. la papila interdental) con el hueso marginal. Si el tejido se retrae como consecuencia de la pérdida ósea, el perfil emergente de la corona se alarga y la papila cercana al diente adyacente o al implante puede desaparecer. Si el tejido blando no se retrae, el aumento en la profundidad de la bolsa puede relacionarse con la aparición de bacterias anaeróbicas y con periimplantitis.
En el transcurso de los años, la causa de la pérdida ósea marginal ha mantenido ocupada a la comunidad implantológica con debates académicos y estudios clínicos. En cualquier caso, las consecuencias clínicas son tales que to das las fases de la odontología implantológica, desde el diagnóstico y la planificación del tratamiento hasta las fases finales de la oclusión y la entrega de la prótesis, deben concentrarse en su reducción o eliminación.
Hipótesis sobre el levantamiento del periostio
El levantamiento perióstico causa un cambio transitorio en el aporte sanguíneo al hueso cortical de la cresta. El noventa por ciento del aporte de sangre arterial y el 100% del retorno venoso están asociados al periostio en los huesos largos del cuerpo. Cuando el periostio es separado del hueso de la cresta, el aporte sanguíneo del hueso cortical se ve afectado de manera importante, causando la muerte de osteoblastos en la superficie a causa del trauma y la falta de nutrición. Estos hechos han promovido la teoría del levantamiento perióstico como causa de la pérdida ósea inicial alrededor de un implante endoóseo.
Aunque las células del hueso de la cresta pueden morir a causa del trauma inicial del levantamiento perióstico, el aporte sanguíneo es restablecido una vez que el periostio se regenera. Las zonas de avance de la reabsorción se desarrollan a partir de los monocitos de la sangre y preceden a los nuevos vasos sanguíneos en las regiones de la cresta ósea. Entonces los osteoblastos son capaces de remodelar la anatomía del hueso crestal. El hueso cortical se forma rápidamente sobre la superficie del periostio para restaurar su condición original. Además, el hueso trabecular subyacente es una fuente de vascularización porque su aporte sanguíneo suele mantenerse a pesar del levantamiento perióstico de la cresta. Cuanto mayor cantidad de hueso trabecular haya por debajo del hueso cortical de la cresta, menor pérdida de hueso del mismo se observará. Para colocar el implante en una cantidad suficiente de hueso disponible, la cresta ósea tendrá una anchura de 5 mm o más. Como resultado, el hueso trabecular está disponible para favorecer el flujo sanguíneo al hueso cortical y la remodelación alrededor de los implantes. El hueso cortical es remodelado a su contorno original, sin pérdida significativa de altura.
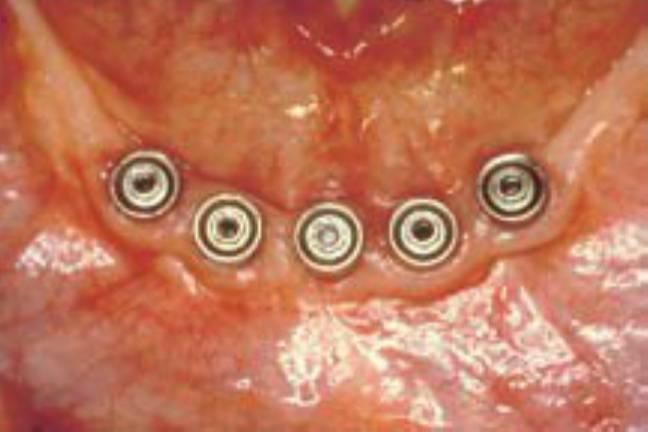
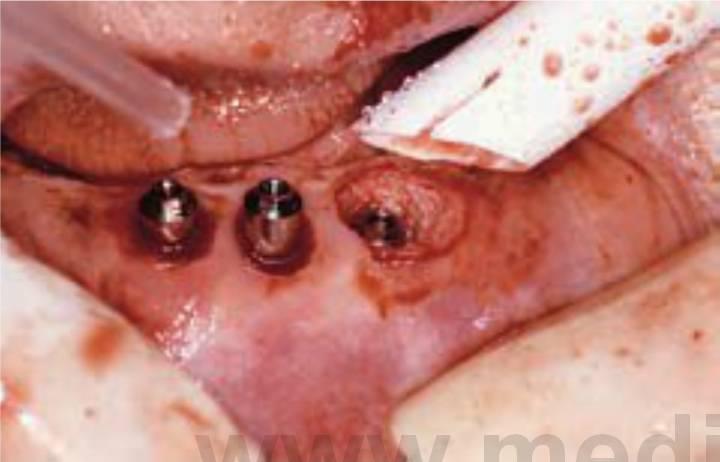
La teoría del levantamiento perióstico conllevaría una pérdida ósea horizontal generalizada de todo el reborde residual expuesto, y no del patrón de zanja localizado alrededor del implante que se observa típicamente. Además, la pérdida ósea generalizada ya debería ser detectable durante la segunda fase de reentrada quirúrgica del cuerpo del implante, entre 4 y 8 meses después de la fase I de la cirugía de inserción del implante. La pérdida ósea generalizada se observa aún raramente durante la segunda fase de cirugía de reentrada implantaría (fig. 4-11). Por tanto, la hipótesis del levantamiento perióstico no aparece como agente causal primario de la pérdida ósea marginal de la cresta alrededor del implante.
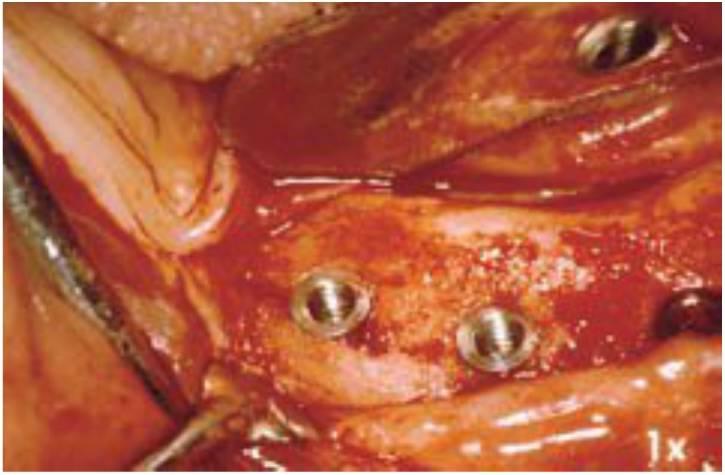
Hipótesis de la osteotomía implantaría
La preparación para la osteotomía implantaría ha sido descrita como agente causal de pérdida ósea inicial en el implante. El hueso es un órgano lábil y sensible al calor. La osteotomía implantaría produce un trauma en el hueso inmediatamente en contacto con el implante, y se crea una zona de hueso desvitalizado de 1 mm aproximadamente alrededor del implante. Para remodelar el hueso en la interfase son necesarios un aporte sanguíneo renovado y frentes de reabsorción. La región de la cresta es más susceptible de perder hueso durante la reparación inicial a causa de su aporte sanguíneo limitado y por la mayor cantidad de calor generada en este hueso más denso, especialmente con la menor eficiencia de cortado de las fresas avellanadoras empleadas en esta región. Esta condición apoya la hipótesis de la preparación de la osteotomía implantaría como agente causal de la pérdida ósea marginal de la cresta alrededor del implante.
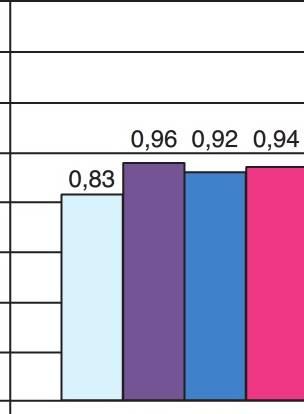
En cualquier caso, si el trauma y el calor durante la preparación de la osteotomía para el implante fueran responsables de la pérdida ósea marginal en la cresta, el efecto sería observable en la segunda fase quirúrgica de reentrada entre los 4 y 8 meses posteriores. La pérdida ósea media de 1,5 mm desde la primera espira no se observa durante la fase II de destape. De hecho, el hueso suele haber crecido por encima del tornillo de cierre de la primera fase, especialmente cuando se encuentra a nivel del hueso o ligeramente avellanado (fig. 4-11). Los estudios en la literatura indican diferentes causas de traumas quirúrgicos y cifras de pérdida ósea. Por ejemplo, Manz observó que la pérdida ósea durante la cirugía de la segunda fase iba de 0,89 a 0,96 mm independientemente de la densidad ósea. Hoar y cols observaron una pérdida ósea de solo 0,2 mm en la fase II de reentrada. El enfoque o sistema quirúrgico pueden influir en estos datos, pero normalmente esta pérdida ósea suele ser mínima.
Uno debería recordar que estas son pérdidas óseas medias observadas. Por ello si se encuentra una pérdida ósea de 2 mm en un implante, y que los siguientes nueve implantes no presentan pérdidas, la media de pérdida ósea sería de 0,2 mm. La mayoría de los implantes durante la fase II de reentrada no muestran pérdida ósea alguna. Por tanto la hipótesis de la osteotomía para implante para la pérdida ósea marginal en la cresta no puede ser responsable primaria de este fenómeno observado rutinariamente.
Hipótesis de la respuesta autoinmunitaria del huésped
La causa primaria de pérdida ósea alrededor de los dientes naturales es su inducción por bacterias. Estudios repetidos han demostrado que las bacterias son el elemento causal de los defectos verticales alrededor de los dientes. El trauma oclusal puede acelerar el proceso, pero el trauma por sí solo no es un factor determinante a considerar. El sulcus gingival del implante en el paciente parcialmente edéntulo con implantes presenta una flora bacteriana similar a la de los dientes naturales. Un supuesto lógico es que si los implantes son similares a los dientes, la pérdida ósea marginal del implante está causada primariamente por las bacterias, con los factores oclusales desempeñando un papel de contribución o aceleración.
En un estudio prospectivo de 125 implantes, Adell y cols observaron que el 80 % de las regiones de los sulcus de los implantes no estaban inflamadas. Lekholm y cols hallaron que las bolsas gingivales profundas alrededor de los implantes no estaban asociadas a la pérdida ósea en la cresta. La pérdida ósea marginal en la cresta hasta la primera espira en los implantes roscados, sigue siendo aún un hallazgo radiológico común. Si las bacterias fuesen el agente causal de la pérdida ósea inicial, ¿por qué la mayor parte de la pérdida se produce durante el primer año (1,5 mm) y más tarde menos (0,1 mm) en los años sucesivos? La profundidad del sulcus del implante aumenta progresivamente a partir de la pérdida ósea inicial, deteriorando la higiene y facilitando que las bacterias anaeróbicas sean la causa de la pérdida ósea relacionada con las bacterias. Si las bacterias son responsables de la pérdida ósea inicial en la cresta de 1,5 mm, ¿qué cambios locales ambientales se producen para reducir su efecto 15 veces después del primer año?. La teoría autoinmunitaria de la bacteria no puede explicar la condición de la pérdida ósea marginal cuando sigue el patrón observado con más frecuencia.
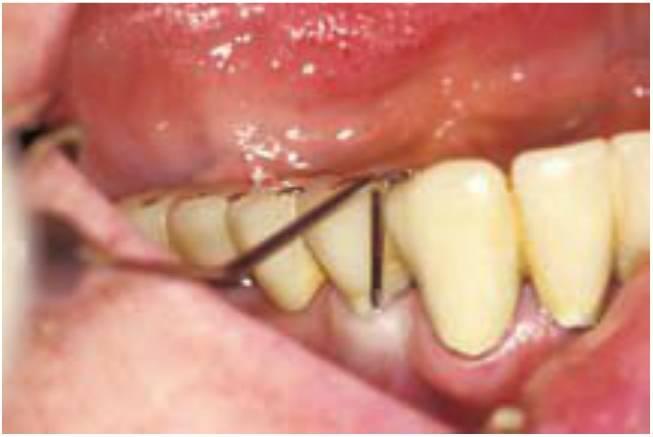
Aunque la teoría de la bacteria no explica adecuadamente el fenómeno de la pérdida ósea marginal en la cresta, esto no significa que las bacterias no sean un factor de contribución importante en la pérdida ósea alrededor del implante. Se ha observado que las roscas y las superficies porosas de implantes expuestas a las bacterias causan una pérdida ósea más rápida alrededor del implante. Se ha observado también que una higiene pobre acelera la pérdida ósea observada alrededor de los implantes endósticos (fig. 4-12). Sería incorrecto afirmar que las bacterias nunca están involucradas en la pérdida ósea marginal alrededor de un implante. La pérdida ósea está asociada con frecuencia con las bacterias como agente causal. En cualquier caso, cuando la mayor parte de la pérdida ósea se produce durante el primer año y es menor posteriormente, la hipótesis de la bacteria como agente causal primario de la pérdida ósea temprana en la cresta no puede ser tomada en consideración.
Hipótesis de la anchura biológica
Las regiones de sulcus alrededor de un implante y un diente natural son similares en muchos aspectos. La formación de crestas epiteliales dentro de la encía adherida y el revestimiento histológico de la encía en el sulcus son similares en implantes y dientes. Se forma un margen gingival libre alrededor de un implante con un epitelio de sulcus no queratinizado, y las células epiteliales en su base son similares a las células epiteliales funcionales descritas en los dientes naturales. En cualquier caso, una diferencia fundamental caracteriza a la base del sulcus gingival.
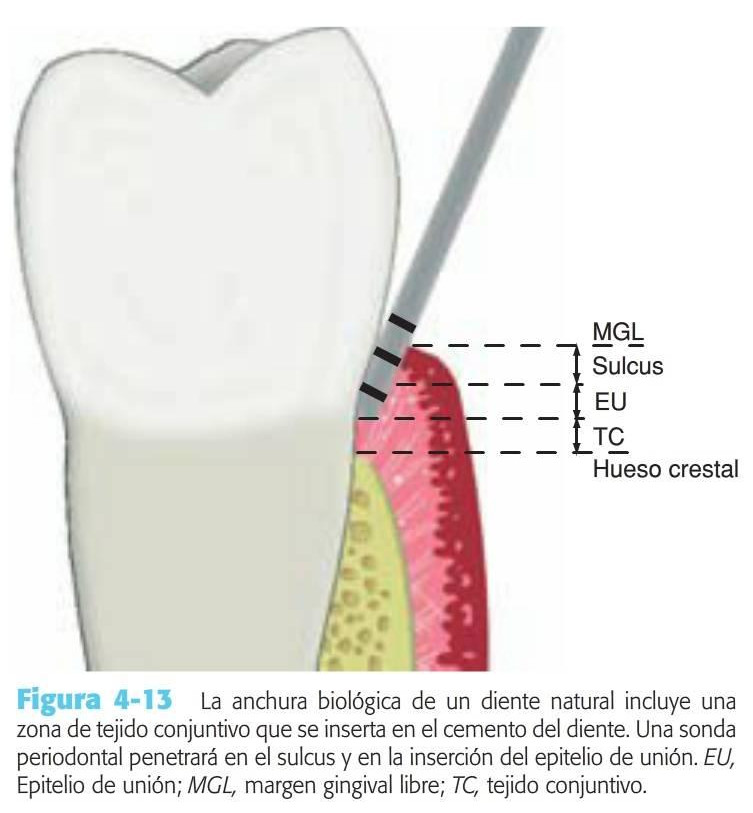
En un diente natural, existe una anchura biológica media de 2,04 mm entre la profundidad del sulcus y la cresta del hueso alveolar (fig. 4-13). Hay que reseñar que la anchura biológica es en realidad una dimensión vertical con una mayor amplitud en la región posterior que en la anterior, y puede ser superior a los 4 mm de altura. En los dientes, consta de una inserción de tejido conjuntivo (TC) (de 1,07 mm de media) supraóseo y una inserción epitelial cruzada (de 0,97 mm de media) en la base del sulcus, siendo la sujeción de TC el valor individual más frecuente. La anchura biológica permite que las fibras gingivales y los hemidesmosomas establezcan un contacto directo con el diente natural, actuando los hemidesmosomas como una barrera biológica contra las bacterias desde el sulcus hasta los tejidos periodontales subyacentes. Cuando el margen de una corona invade la anchura biológica, el hueso crestal retrocede para restablecer un entorno favorable para las fibras gingivales.
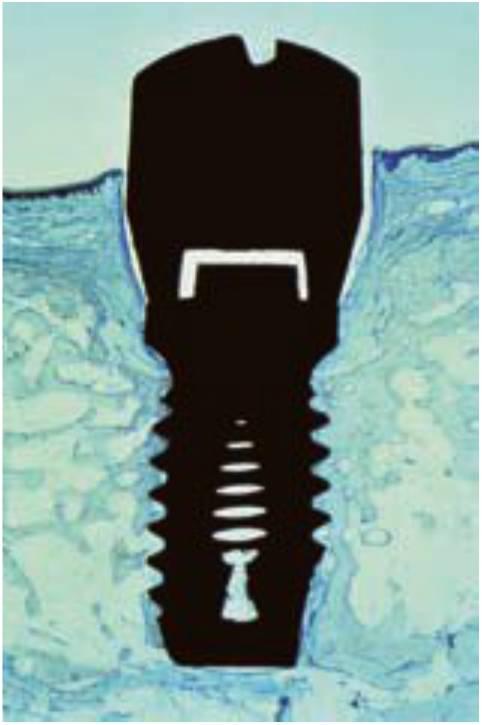
Muchos protocolos quirúrgicos recomiendan la colocación de implantes endósticos por debajo o en la misma cresta del reborde durante la primera fase quirúrgica. La conexión pilar-cuerpo del implante puede compararse con el margen de una corona. Berglundh y cols observaron en perros una pérdida ósea de 0,5 mm por debajo de la conexión pilar-cuerpo del implante durante las dos semanas siguientes a la fase II de reentrada y conexión de pilares (fig. 4-14). Lindhe y cols observaron un tejido conjuntivo inflamado extendiéndose 0,5 mm por arriba y por debajo de esta conexión de pilar a implante. Wallace y Tamow afirmaron que la anchura biológica se forma también con los implantes y puede contribuir a parte de la pérdida ósea marginal observada. La teoría de la anchura biológica parece atractiva para explicar la falta de pérdida ósea entre la primera fase quirúrgica y la pérdida ósea inicial observada durante el primer año después de la segunda fase de colocación del pilar. En cualquier caso, debería considerarse que la anchura biológica en los implantes, tal y como se ha observado, suele incluir la profundidad del sulcus, mientras que la anchura biológica del diente natural no la incluye.
Se observan once grupos diferentes de fibras gingivales alrededor de un diente natural: dentogingival (coronal, horizontal y apical), alveologingival, intercapilar, transgingival, circular, semicircular, dentoperióstico, transeptal, periostiogingival, intercircular e intergingival. Al menos seis de estos grupos de fibras gingivales se insertan en el cemento del diente natural: las dentogingivales (coronales, horizontales y apicales), dentoperiósticas, transeptales, circulares, semicirculares y transgingivales. Además, algunas fibras de la cresta originadas en los haces de las fibras periodontales se insertan también en el cemento por encima del hueso alveolar. En cualquier caso, en una típica región gingival periimplantaria, solo están presentes dos de estos grupos de fibras gingivales y ninguno de fibras periodontales (fig. 4-15). Estas fibras no se insertan en el cuerpo del implante por debajo del margen del pilar como lo hacen en el cemento de los dientes naturales. En su lugar, las fibras colágenas de la inserción de TC alrededor del implante se extienden paralelas a la superficie del implante, y no perpendiculares, como con los dientes naturales. Los grupos de fibras gingivales y periósticas son responsables del componente de la inserción de tejido conjuntivo del ancho biológico alrededor de los dientes, y no están presentes alrededor de la región transósea de un implante. De ahí que la inserción de TC alrededor de la conexión pilar-implante no pueda ser comparada con la inserción de TC de un diente.
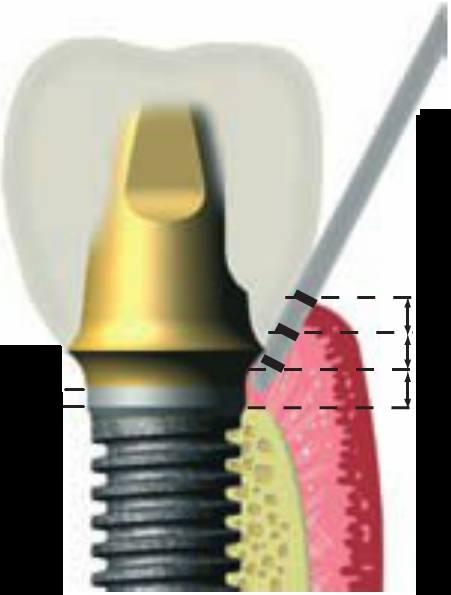
James y Keller fueron los primeros en iniciar un estudio científico sistemático para investigar el fenómeno del sellado biológico de los tejidos blandos alrededor de los implantes. Los hemidesmosomas ayudan a formar una estructura basal del tipo de lámina en el implante, que puede actuar como un sellado biológico. En cualquier caso, los componentes colágenos del cuerpo lineal no se pueden adherir o incrustarse en el cuerpo del implante tal y como hacen en el cemento del diente. El sello hemidesmosómico solo tiene una banda de tejido gingival en su circunferencia para proporcionar una protección mecánica contra el desgarro. Por tanto el sello biológico alrededor de los implantes puede prevenir la migración de las bacterias y las endotoxinas dentro del hueso subyacente. En cualquier caso, no es posible constituir un componente de inserción epitelial de unión del ancho biológico similar al encontrado en los dientes naturales. Por tanto, no parece probable que la pérdida de hueso temprana en la cresta sea el resultado exclusivo de la remodelación de los tejidos blandos y duros para establecer una anchura biológica por debajo de una conexión de pilar. Ninguna zona de inserción de tejido conjuntivo o componentes del cuerpo lineal se incrustan dentro de un implante. La importancia, cantidad, y mecanismo de estas estructuras anatómicas requieren investigaciones posteriores.
La grieta entre el tornillo de cierre y el cuerpo del implante durante la cicatrización inicial es similar a la grieta de la conexión pilar-implante. No obstante, el hueso puede crecer por encima del tornillo de cierre, y por tanto la grieta en sí misma, no tiene porque ser la causa de la pérdida ósea. La grieta entre el implante y la conexión del pilar ha sido denominada «microgap» (microespacio). La dimensión actual de esta conexión suele ser de 0 μm y tiene una conexión directa metal-metal. En cualquier caso, cuando este espacio es expuesto al entorno oral, se suele observar una pérdida ósea de por lo menos 0,5 mm por debajo de la conexión.
La hipótesis de la anchura biológica no puede explicar completamente la pérdida ósea marginal en la cresta de varios milímetros, que se ha observado también en los implantes de una sola fase que se extiende a través de los tejidos en la colocación quirúrgica inicial del implante y que no tienen conexiones pilar-implante. Por ejemplo, los implantes con forma de placa (lámina), implantes transóseos, en pins, los implantes enroscados de una pieza, e incluso los implantes subperiósticos muestran el fenómeno de pérdida ósea marginal en la cresta.
Es cierto que, la pérdida ósea se produce alrededor de una conexión pilar-implante expuesta colocada debajo del hueso y que se observa de las 2 a las 4 semanas siguientes, una vez que la conexión queda expuesta al entorno oral. La pérdida ósea se produce en ocasiones antes de la carga del implante con la prótesis. Es lógico llamar a esta pérdida ósea marginal la anchura biológica.
La pregunta primaria persiste, cuando el cirujano coloca la conexión pilar-implante en zona infraósea, ¿cuánta pérdida ósea se debe a la anchura biológica del implante, y por tanto fuera de la influencia del odontólogo? Diferentes estudios en la literatura observan que la micro y macrogeometría pueden afectar a las dimensiones de la anchura biológica o a la cantidad de pérdida ósea temprana.
La pérdida ósea observada hasta la primera rosca implica que la cantidad de hueso perdido es similar para diferentes diseños de implantes. En cualquier caso la primera rosca se encuentra a una distancia diferente del margen del pilar según el diseño del implante. Se ha asociado una mayor pérdida ósea a un collar pulido de 4 mm infraóseo que a uno de 2 mm. El concepto de anchura biológica del implante no explica completamente la cantidad total de pérdida ósea vertical observada. Además la cantidad de pérdida ósea producida por la anchura biológica se produce durante el primer mes, esté cargado o no el implante, y está relacionada con el diseño del módulo crestal del implante y la posición de la conexión pilar-implante en relación con el hueso pero no está relacionada con la densidad del hueso. Este concepto no explica por qué se observa con más frecuencia una mayor pérdida ósea después de la carga en el hueso blando en comparación con un hueso más denso, como tampoco explica la mayor media de fracasos de implante en hueso de menor calidad después de la carga.
Trauma oclusal
La pérdida ósea marginal en un implante puede deberse a un trauma oclusal. Un trauma oclusal puede definirse como una lesión en el aparato de sujeción como resultado de una fuerza oclusal excesiva. Es controvertido el papel de la oclusión en la pérdida ósea observada después de la colocación de una prótesis implantosoportada. Algunos artículos afirman que la pérdida ósea periimplantaria sin fracaso del implante está asociada primariamente a razones biológicas o complicaciones. Otros autores sugieren la correlación entre la pérdida ósea crestal y una sobrecarga oclusal. Es necesaria ¡a determinación de la causa de la pérdida ósea alrededor de los implantes dentales para minimizar su existencia y fomentar la salud periimplantológica a largo plazo que podría determinar finalmente la supervivencia de la prótesis implantosoportada.
La asociación de trauma oclusal y pérdida ósea alrededor de los dientes naturales ha sido debatida desde que Karolyi estableciera una relación en 1901. Numerosos autores han concluido que el trauma por oclusión es un factor relacionado con la pérdida ósea, aunque la bacteria sea un agente necesario para ello. Por otra parte, Waerhaug y muchos otros han afirmado que no existe relación entre el trauma oclusal y el grado de destrucción del tejido periodontal. Según Lindhe y cols, el «trauma» por oclusión no puede inducir deterioro del tejido periodontal. En cualquier caso, el trauma oclusal puede conllevar una movilidad del diente que puede ser transitoria o permanente. Extrapolando este razonamiento, diferentes autores han concluido también que el trauma oclusal no está relacionado con la pérdida ósea marginal alrededor de un implante dental.
Para establecer una posterior correlación entre la pérdida ósea marginal y la sobrecarga oclusal, hemos recopilado artículos relacionados con la biomecánica celular, principios de ingeniería, propiedades mecánicas del hueso, fisiología del hueso, diseños biomecánicos de implantes, estudios animales, y estudios clínicos.
Biomecánica celular
La remodelación ósea a nivel celular está controlada por el entorno mecánico de la deformación. La deformación relativa se define como el cambio en la longitud dividido por la longitud original, y las unidades de deformación vienen dadas en porcentajes. La cantidad de deformación en un material está directamente relacionada con la cantidad de estrés aplicado. El estrés oclusal aplicado a través de las prótesis implantosoportadas y sus componentes puede transmitir estrés a la interfase implante-hueso. La cantidad de deformación ósea en la interfase implante-hueso está directamente relacionada con la cantidad de estrés aplicado a través de las prótesis de implantes. Los sensores mecánicos en el hueso responden a cantidades mínimas de deformación, y las microdeformaciones de niveles 100 veces inferiores a la resistencia final del hueso, pueden desencadenar la remodelación ósea (fig. 4-16).
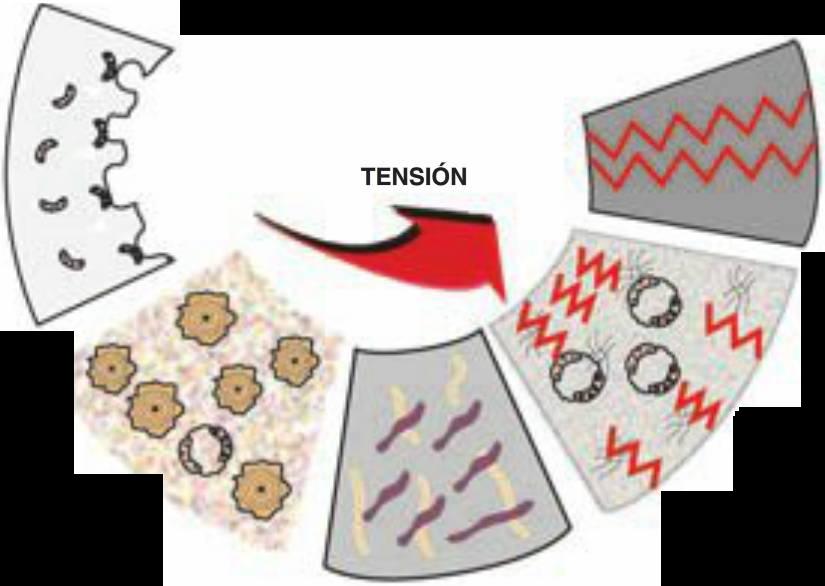
Una de las teorías de la remodelación más antiguas basada en la relación directa entre el estrés y la magnitud de la remodelación ósea fue propuesta por Kummer en 1972. Más recientemente, Frost ha observado diferentes niveles de microdeformación en la reacción celular del hueso. Observó que el hueso se fractura entre 10.000 y 20.000 unidades de microdeformación (un 1 a un 2 % de deformación). En cualquier caso, en niveles de entre el 20 y 40 % de estos valores, las células óseas pueden producir citoquinas para iniciar una respuesta de reabsorción. En otras palabras, una deformación ósea excesiva puede no solamente resultar en una fractura ósea sino además provocar una reabsorción ósea celular. De ahí que la hipótesis de que el estrés oclusivo más allá de los límites fisiológicos del hueso puede resultar en una deformación lo suficientemente significativa como para provocar una reabsorción ósea, sea creíble desde el punto de vista de la biomecánica celular. A día de hoy, los estudios celulares óseos no han conseguido demostrar esta condición cerca de un implante dental. En cualquier caso, las citoquinas en el tejido de interfase hueso-implante obtenido de las prótesis de caderas que han fracasado y conllevado a una pérdida ósea, han sido observadas en los humanos.
Principios de ingeniería
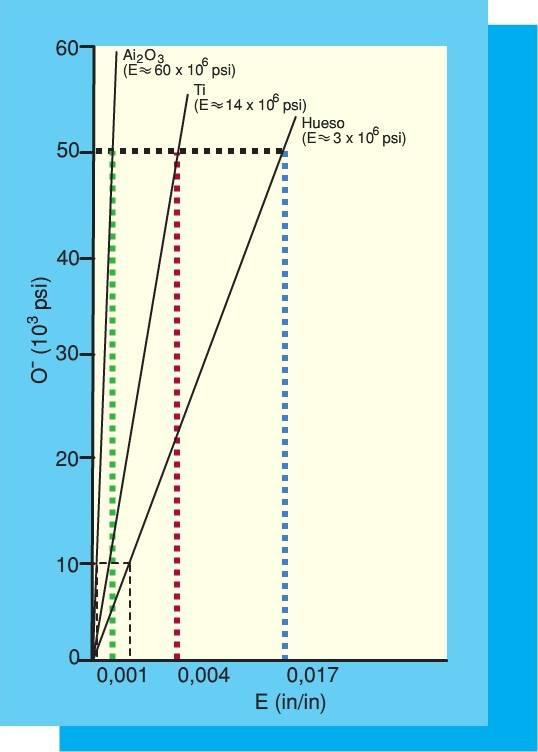
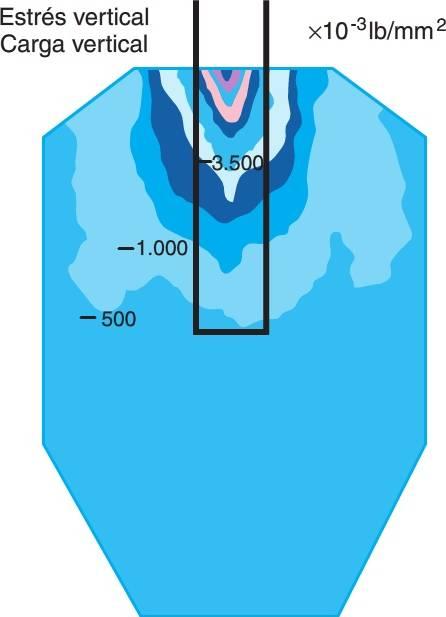
La relación entre el estrés y la deformación determina el módulo de elasticidad de un material (la rigidez). El módulo expresa la cantidad de cambio dimensional en un material en relación a un nivel de estrés determinado. El módulo de elasticidad de un diente es similar al del hueso cortical. Los implantes dentales están fabricados habitualmente de titanio o sus aleaciones. El módulo de elasticidad del titanio es de cinco a diez veces mayor que el del hueso cortical (fig. 4-17). Un principio de ingeniería llamado análisis d e haz complejo, afirma que cuando dos materiales con módulos de elasticidad diferentes son colocados conjuntamente sin la intervención de otro material y uno de ellos es cargado, se observará un incremento del contorno de estrés donde los dos materiales toman contacto en primer lugar. En una interfase hueso-implante, estos contornos de estrés son de mayor magnitud en la región ósea de la cresta. Este fenómeno fue observado tanto en estudios de fotoelasticidad como en análisis de elementos finitos en tres dimensiones (fig. 4-18) cuando los implantes eran cargados en una simulación ósea Estos autores observaron que la pérdida ósea marginal observada clínicamente y radiográficamente alrededor de un implante sigue un patrón similar al de los contornos de estrés de estos estudios.
Propiedades mecánicas del hueso
La densidad ósea está directamente relacionada con la resistencia y el módulo elástico del hueso. En los huesos más densos se produce menos deformación bajo una carga dada en comparación con los huesos más blandos. Como resultado, se produce menos remodelación ósea en los huesos más densos en comparación con los huesos más blandos bajo las mismas condiciones de carga. Una disminución de la remodelación ósea puede conllevar una reducción de la pérdida ósea. En un estudio humano prospectivo, Manz observó que la cantidad de pérdida ósea marginal cercana a un implante estaba relacionada con la densidad del hueso. La pérdida ósea periimplantológica inicial desde la inserción del implante hasta su reentrada era similar para todas las calidades de hueso. En cualquier caso, seis meses después de la entrega de la prótesis, la pérdida ósea periimplantológica adicional observada radiográficamente iba desde los 0,68 mm para una calidad 1 de tipo de hueso hasta los 1,1 mm para la calidad 2, hasta los 1,24 mm para la calidad 3 y los 1,44 mm para la calidad 4 (fig. 4-19). En otras palabras, cuanto más denso sea el hueso, menor pérdida ósea periimplantológica se observa después de la entrega de la prótesis. Un estudio clínico realizado por Appleton y cols demostró que implantes dentales individuales cargados progresivamente en la región del primer premolar de los seres humanos exhibieron un mayor aumento de la densidad ósea en la mitad crestal de la interfase del implante y menor pérdida ósea marginal en comparación con los implantes no cargados progresivamente en la misma región mandibular e incluso en el mismo paciente en el lado contralateral sin carga progresiva. Al estar relacionado el aumento de densidad ósea con la resistencia ósea, el módulo elástico, la remodelación ósea, y una disminución en la pérdida ósea marginal, estas entidades pueden estar relacionadas entre sí.
Estudios animales
Varios estudios animales en la literatura demuestran la habilidad del tejido óseo para responder ante un implante dental. Por ejemplo, Hoshaw y cols insertaron implantes dentales en el fémur de un perro perpendiculares al eje del hueso largo y perpendiculares a la dirección de los osteomas. Después de aplicar una carga de tracción en los implantes durante solo 5 días, las células óseas se reorganizaron para seguir el patrón de la rosca del implante y resistir la carga. Este patrón óseo único solo se observó en 3 o 4 mm alrededor de los implantes. También se observó una pérdida ósea en la cresta alrededor de estos implantes y que se justificaron como resultado de una sobrecarga por estrés. Para reorganizar su estructura, el hueso debe remodelarse.
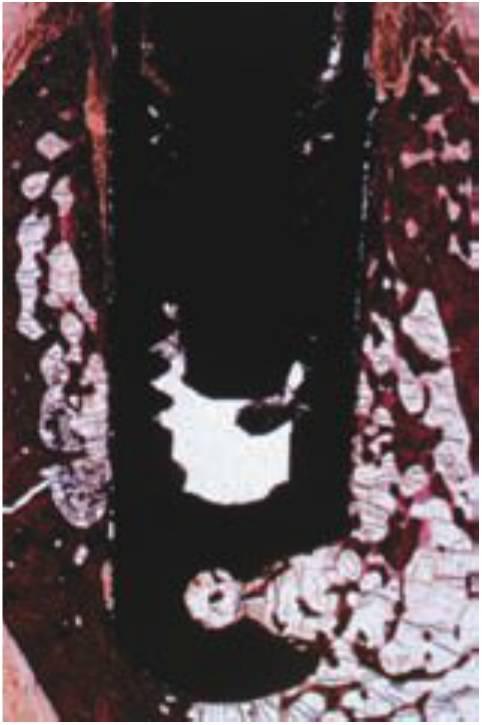
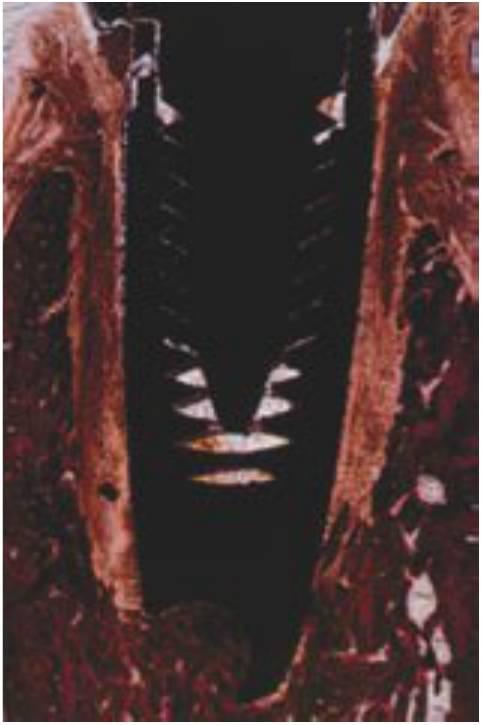
Miyata colocó coronas sobre implantes dentales integrados sin superficies oclusales de contacto (grupo de control), y contactos oclusales prematuros de intercepción de 100, 180 y 250 μm en un mono como modelo animal. Después de 4 semanas de cargas oclusivas prematuras, se extrajeron los implantes en un bloque de sección y se analizaron. Los niveles de hueso de cresta para 100 μm y los implantes de control sin carga eran similares. En cualquier caso, se observó una pérdida ósea en la cresta estadísticamente significativa en el grupo de 180 μm (fig. 4-20). El grupo de 250 μm experimentó de dos a tres veces la pérdida ósea de las coronas con prematuridades moderadas (fig. 4-21). Duyck empleó un modelo canino para valorar la pérdida de hueso crestal alrededor de los implantes tipo tornillo sin carga (con troles), con cargas estáticas y con cargas dinámicas. Los implantes con cargas dinámicas fueron los únicos que mostraron pérdidas óseas. Como la única variable en estos dos estudios fue la intensidad o el tipo de carga oclusal aplicada a los implantes, estos estudios con animales implican que la carga oclusal dinámica puede ser un factor en la pérdida ósea alrededor de los implantes dentales rígidos.
Informes clínicos
Existen informes clínicos que han mostrado un aumento de la pérdida ósea marginal alrededor de los implantes más cerca del cantilever empleado para restaurar la dentición perdida (fig. 4-22).
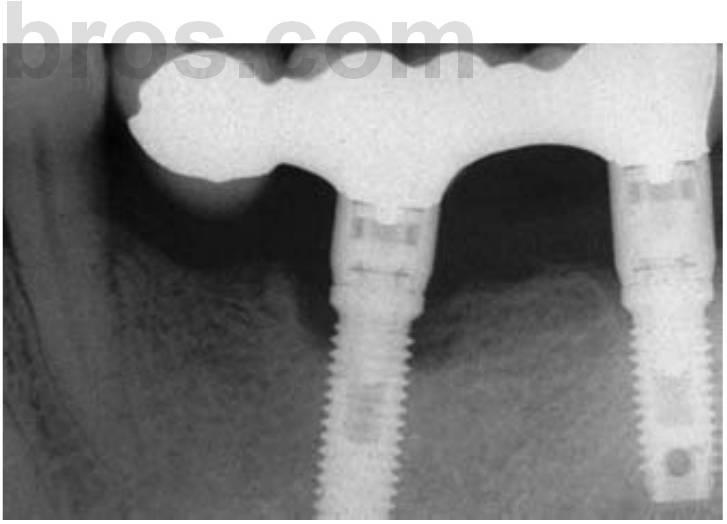
La longitud del cantilever y un aumento del estrés oclusal en el pilar más cercano están directamente relacionados111 y apuntan al hecho de que el aumento de la pérdida ósea marginal puede estar relacionado con el estrés oclusal. Quirynen y cols, evaluaron 93 pacientes con implantes con varias restauraciones de implantes y concluyeron que la cantidad de pérdida ósea en la cresta estaba definitivamente asociada con la carga oclusal. Estos autores observaron también un aumento de la pérdida ósea en la cresta alrededor de los implantes en pacientes sin contactos oclusales anteriores y con hábitos parafuncionales de prótesis fijas de arco completo en ambas mandíbulas. Estos informes clínicos no proporcionan análisis estadísticos que demuestren un eslabón claro entre el estrés oclusal y la pérdida ósea. En cualquier caso, indican un consenso entre varios autores de que la sobrecarga oclusal puede estar relacionada con la incidencia de la pérdida ósea periimplantológica alrededor del aspecto cervical de un implante. De hecho, en un estudio sobre 589 implantes consecutivos, Naerty cols, sugieren que la sobrecarga causada por los hábitos parafuncionales puede ser la causa más probable de la pérdida de implantes y de la pérdida ósea marginal después de la carga.
Range y cols, habían observado que las cargas oclusales sobre un implante pueden actuar como un momento de torsión que aumenta el estrés al nivel marginal del hueso y puede causar la fractura del cuerpo del implante. La pérdida ósea marginal se observó en esta evaluación clínica retrospectiva, antes que la fractura del cuerpo del implante. El mismo estrés que causó la fractura del cuerpo del implante es la causa lógica de la pérdida ósea periimplantológica previa a este hecho.
Rosenberg y cols, encontraron diferencias microbianas en los fracasos de implantes tanto en las complicaciones por sobrecargas como biológicas. Uribe y cols, presentaron un caso de corona de implante mandibular con una periimplantitis marginal y un defecto óseo. Los análisis histológicos revelaron un infiltrado y una zona central de denso tejido fibroconectivo con escasas células inflamatorias. Según los autores, estos hallazgos difieren del tejido crónico inflamatorio asociado a las periimplantitis infecciosas y puede relacionarse directamente con la sobrecarga oclusal.
Un informe clínico por Leungy cols, observó radiográficamente una pérdida ósea angular en la cresta hasta la 7ª rosca en uno de cada dos implantes soportando una prótesis fija en hiperoclusión dos semanas después de la entrega de la prótesis. Se retiró la prótesis y durante los meses siguientes, la observación radiográfica mostró que el defecto en la cresta se había reparado hasta prácticamente el nivel inicial, sin intervención quirúrgica o medicamentosa alguna. Se asentó entonces la prótesis con el ajuste oclusal adecuado. Los niveles óseos se estabilizaron en la segunda rosca del implante y permaneció estable durante los siguientes 36 meses. Este informe indica que la pérdida ósea no solamente pueda deberse a la sobrecarga oclusal, sino que además pueda ser reversible cuando es detectada al inicio del proceso. Por tanto, aunque ningún estudio clínico prospectivo haya demostrado claramente hasta la fecha una relación directa entre el estrés y la pérdida ósea sin fracaso del implante, numerosos odontólogos están de acuerdo en que pueda existir una relación causal.
Biomecánica de los diseños de implantes
Se han observado diferentes cantidades de pérdidas óseas marginales según los distintos diseños de cuerpos de implantes. El diseño y las condiciones de la superficie del implante pueden afectar a la cantidad de deformación distribuida en la interfase hueso-implante. Un informe de Zechner y cols, evaluó la pérdida ósea alrededor de implantes roscados y en carga funcional comparando aquellos de superficie maquinada de roscas «en V» con los de superficie arenada y grabada con ácido y rosca cuadrada (fig. 4-23).

Estos dos diseños de implantes tenían un módulo de cresta similares y una conexión hexagonal externa. Se colocaron cuatro implantes interforaminales en la mandíbula en 36 pacientes que fueron revisados durante 4 años. Durante este período la media de pérdida ósea fue de 2,4 mm (rosca en V) frente a los 1,6 mm (rosca cuadrada). En cualquier caso, la media de pérdida ósea en el estudio fue de 0,1 hasta 8,5 mm en los implantes de rosca en V maquinados, y de 0,2 a 4,8 mm para los implantes de superficie cuadrada rugosa. Veintidós implantes de roscas en V perdieron más de 4 mm de hueso y menos de 1 mm de pérdida fue observada en implantes de roscas cuadradas y superficie rugosa comparado con solo dos implantes de roscas en V de superficie maquinada (fig. 4-24).
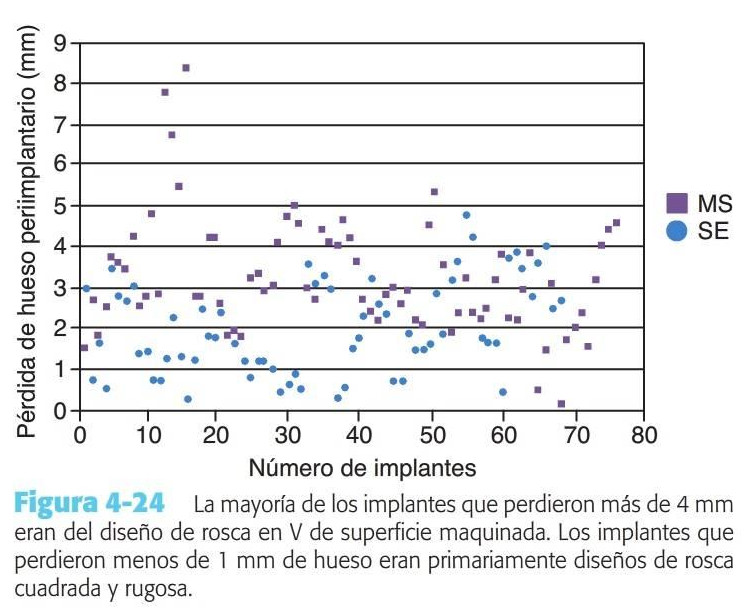
No se hallaron indicios de exudado o inflamación. La media de pérdida ósea con las diferentes condiciones de superficie y diseño de los implantes en un informe clínico sugiere que existen más causas involucradas en el proceso de pérdida ósea marginal en el implante individual además de la anchura biológica, la posición del microgap, y/o las causas quirúrgicas. Los tres factores más probables que influenciaron la cantidad de pérdida ósea en la cresta en este informe son la cantidad de fuerza aplicada en la prótesis, la calidad del hueso para resistir a estas fuerzas y el diseño del cuerpo del implante. Estas tres condiciones implican que la sobrecarga oclusal es la causa de la pérdida ósea marginal alrededor del implante.
Un estudio prospectivo de Karousis y cols, indicó también que los diferentes diseños de implantes y condiciones de superficie se corresponden con las diferentes incidencias de pérdida ósea crestal. Tres diferentes diseños de implantes del mismo fabricante fueron evaluados durante 10 años en un estudio prospectivo. Un diseño de cuerpo de implante perdió 5 mm de hueso el 26 % de las veces, mientras que los otros dos diseños presentaron un 37 y 39 % de incidencia. Se produjo una pérdida ósea marginal de más de 6 mm en el 22 % de los implantes con el primer diseño, en comparación con el 35 y 33 % de los otros dos diseños. Estos resultados indican que un diseño de implante puede provocar menos pérdida ósea que otro y apuntan al hecho de que los informes clínicos con una cicatrización y protocolos de carga similares, pero con diseños de cuerpo del implante y condiciones de superficie diferentes, pueden producir diferentes cantidades de pérdida ósea en la cresta. Al afectar el diseño del implante y las condiciones de su superficie a la cantidad de estrés transmitido al hueso, uno de los motivos de las diferentes cantidades de pérdida ósea según el diseño del implante puede estar relacionado con el estrés transmitido al hueso.
En el campo de la ortopedia, la sustitución de la articulación de la cadera presenta diferentes complicaciones, incluyendo la infección de la cicatriz, la fractura periprotésica, la luxación, el fracaso mecánico y la osteólisis. La osteólisis se refiere a la reabsorción ósea que se produce alrededor de los implantes ortopédicos cementados y no cementados (fig. 4-25).
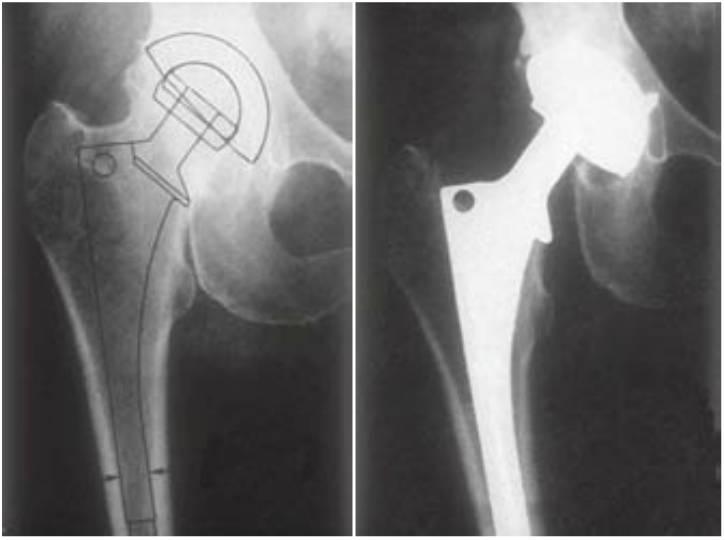
La pérdida aséptica de la interfase hueso-implante a causa de la osteólisis es la causa más importante del fracaso tardío de la sustitución de la articulación (10% durante los 10 primeros años). A esta condición están asociados primariamente factores mecánicos de carga. Los factores del paciente que aumentan el fracaso de la carga incluyen el peso corporal y el nivel de actividad. Un modelo animal y un informe humano han relacionado la reabsorción del hueso en la interfase con la sobrecarga mecánica. El tratamiento del desorden, si el paciente está asintomático con una amplia afectación osteolítica pero sin movilidad del implante, incluye un curetaje de la membrana osteolítica y un injerto óseo. Estos informes ortopédicos aceptan que la sobrecarga mecánica puede ser la causa de la reabsorción ósea en la interfase hueso-implante. El metal más frecuentemente empleado en estas terapias de sustitución de la cadera es la aleación de titanio, y la interfase hueso-implante es muy similar al de un implante dental. Adicionalmente, elementos potencialmente causantes encontrados intraoralmente, como la contaminación oral bacteriana, la posición del microgap, y la pérdida ósea relacionada con microbios, son eliminadas en este entorno aséptico. Es lógico asumir que estos estudios soportan una posterior relación entre la pérdida ósea marginal alrededor de los implantes y el estrés biomecánico.
Discusión
Se ha observado durante décadas alrededor de la porción transmucosa de los implantes dentales una pérdida ósea marginal limitada durante el primer año de función después de la fase II quirúrgica. Las hipótesis para la pérdida ósea en la cresta han incluido la reflexión del periostio durante la cirugía, la preparación de la osteotomía para el implante, el nivel de microgap entre el pilar y el cuerpo del implante, la invasión bacteriana, el establecimiento de la anchura biológica, el diseño del módulo crestal del implante, y la sobrecarga oclusal.
El hecho de que la sobrecarga oclusal pueda ser una causa de la pérdida ósea en la cresta, no significa que no estén presentes otros factores. Por ejemplo, la posición del microgap entre la plataforma del implante y el pilar y la anchura biológica suelen afectar al hueso marginal durante el primer mes después de que el implante se haga transmucoso. En cualquier caso, el odontólogo dispone de ciertas variables bajo su control que pueden influir en la cantidad de pérdida de hueso periimplantario. La posición del microgap en relación con el hueso de la cresta y el diseño del módulo crestal del implante están inicialmente bajo el control del cirujano. Por otra parte, la respuesta autoinmunitaria o bacteriana del paciente, la anchura biológica y la respuesta del paciente al trauma quirúrgico por la colocación del implante son variables que escapan con frecuencia del control del odontólogo. Una vez que se ha entregado la prótesis final al paciente, ya se han producido varios elementos responsables de la pérdida ósea marginal, mientras que otros tales como la sobrecarga oclusal y sus relaciones con la calidad ósea aún persisten. La sobrecarga oclusal es uno de los factores más controlados por el odontólogo. Si existe una relación entre sobrecarga oclusal y la pérdida ósea en la cresta, parece apropiado buscar enfoques para disminuir el estrés de la superficie de un implante.
Uno de los elementos que encajan en la relación entre la fuerza oclusal y la pérdida ósea periimplantaria es la ausencia de pérdida continuada de hueso hasta el fracaso del implante. La altura de la corona del implante debe medirse desde el plano oclusal hasta la cresta ósea. La altura de la corona es un cantilever vertical, lo que puede magnificar el estrés aplicado sobre la prótesis. Como resultado de una mayor altura de la corona, resultado de la pérdida ósea, la sobrecarga oclusal aumentará después de que se produzca la pérdida ósea en la cresta. De ahí que, si las fuerzas de carga oclusal pueden causar la pérdida ósea en la cresta, los momentos de fuerzas aumentados resultantes deberían favorecer la pérdida de hueso hasta el fracaso del implante. La mayoría de estudios clínicos indican que la media de pérdida ósea disminuye después del primer año de la carga y es mínima de ahí en adelante. Existen dos motivos por los que el nivel óseo se mantiene estable después de la pérdida ósea inicial marginal, incluso cuando la causa sea una sobrecarga oclusiva: la fisiología del hueso y la mecánica del diseño del implante.
Fisiología del hueso
El hueso es menos denso y más débil durante la fase 2 de la cirugía del implante de lo que es un año después de la carga protésica. El hueso está mineralizado en un 60 % a los 4 meses y tarda 52 semanas en completar su mineralization. Un hueso parcialmente mineralizado es más débil que uno completamente mineralizado. Además, la organización microscópica del hueso progresa durante el primer año. El hueso reticular es menos organizado y más débil que el hueso laminar, que está organizado y más mineralizado. El hueso laminar se desarrolla varios meses después de que el hueso reticular de reparación haya reemplazado al hueso desvitalizado a causa del trauma producido por la inserción quirúrgica alrededor del implante. Los niveles de estrés oclusales pueden ser lo suficientemente altos como para causar microfracturas del hueso reticular o una sobrecarga durante el primer año, pero el aumento en la fuerza del hueso conseguido después de la organización y mineralization completa puede resistir los mismos niveles de estrés durante los años siguientes.
Al aplicar las fuerzas funcionales sobre el implante, el hueso a su alrededor es capaz de adaptarse al estrés y de aumentar su densidad, especialmente en la mitad crestal del cuerpo del implante desde el 6° mes hasta el año después de la carga del implante. En un estudio histológico e histomorfométrico del hueso, Piatelli y cols, observaron reacciones en monos con implantes cargados y no cargados (figs. 4-26 y 4-27). El hueso cambió de un patrón fino trabeculado después de la cicatrización inicial a un patrón trabecular más denso y grueso después de la carga, especialmente en la mitad crestal de la interfase del implante. Hoshaw cargó implantes insertados en perros con una carga tensional y observó que el patrón de hueso fino trabecular se transformó en hueso trabecular grueso alrededor del implante. Además, el hueso se reorganizó en una condición más favorable para resistir la dirección y el tipo de la carga oclusal (fig. 4-28).

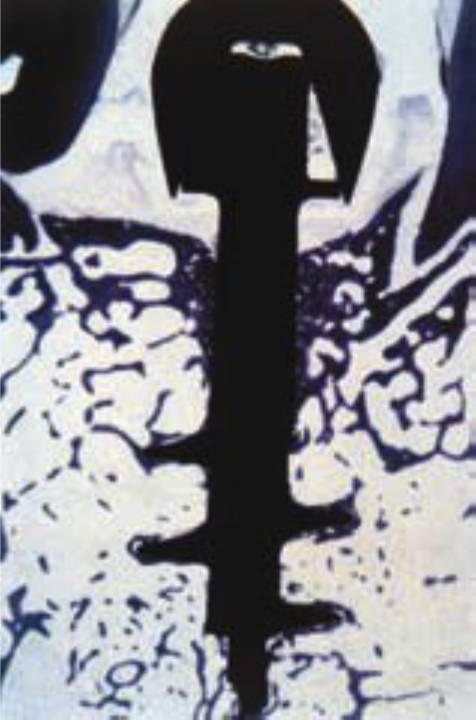
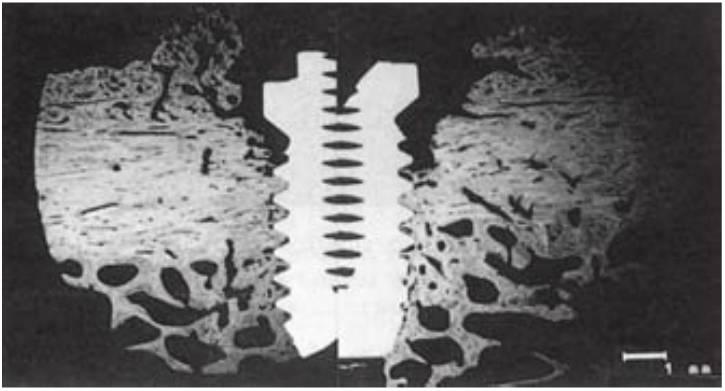
El hueso fino trabecular es menos denso que el hueso trabecular grueso. Al estar directamente relacionada la densidad ósea con su fuerza y su módulo elástico, la fuerza ósea en la cresta y la mala combinación biomecánica entre el titanio y el hueso puede disminuir gradualmente durante la fase de carga progresiva. En otras palabras, el estrés aplicado al hueso periimplantario puede ser lo suficientemente grande como para provocar reabsorción ósea durante el primer año, porque las tensiones óseas son mayores en la cresta. En cualquier caso, las tensiones aplicadas en zona ósea subcrestal son de menor magnitud y pueden corresponder a la deformación fisiológica que permite al hueso ganar fuerza y densidad. Como resultado, la carga oclusal que provoca la pérdida ósea inicial (sobrecarga) no es lo suficientemente grande para causar una pérdida ósea continuada una vez que el hueso madura y se vuelve más denso.
Un informe clínico realizado por Appleton y cols, demostró que los implantes dentales individuales cargados progresivamente en la región del primer premolar de los humanos mostraron una menor pérdida ósea y un mayor aumento de la densidad ósea en la mitad crestal de la interfase del implante, en comparación con los implantes no cargados progresivamente en la misma región mandibular, e incluso en el lado contralateral del mismo paciente (fig. 4-29).
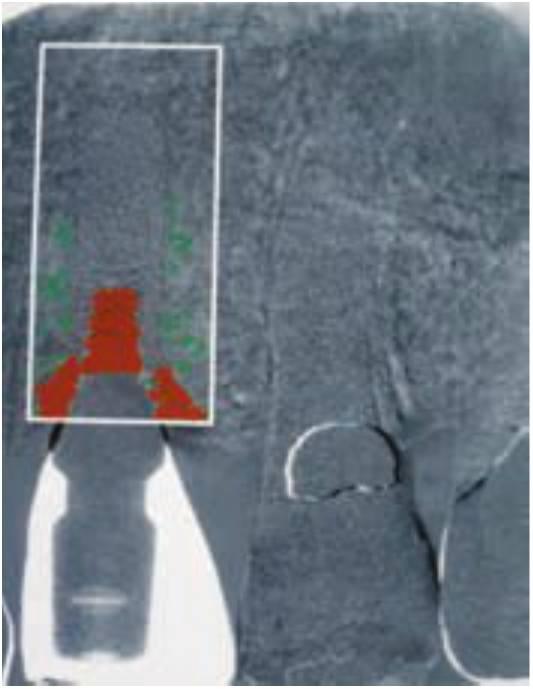
La pérdida ósea marginal es menor en la mandíbula en comparación con la del maxilar en diferentes estudios clínicos. El hueso es más denso en la mandíbula que en el maxilar. La pérdida ósea crestal disminuida observada en la mandíbula, en densidades óseas mayores, y en implantes cargados progresivamente apuntan al hecho de que el estrés/deformación es una causa primaria de pérdida ósea crestal después de que el implante sea sometido a carga. Por tanto las tensiones en el reborde crestal pueden causar microfracturas o sobrecarga durante el primer año, las modificaciones en la resistencia del hueso después de que la carga y la mineralization se hayan completado un año después cambia la relación estrés/deformación y reduce el riesgo de microfracturas durante los años siguientes.
Biomecánica del diseño de los implantes
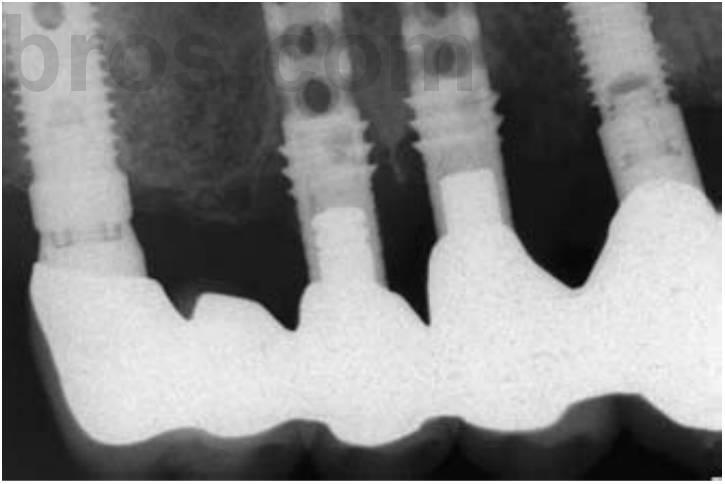
El diseño del implante puede afectar a la magnitud o el tipo de fuerzas aplicadas en la interfase hueso-implante. Un cuello liso en el módulo crestal puede transmitir fuerzas transversales al hueso. El hueso es más fuerte ante fuerzas compresivas, un 30% más débil ante cargas de tracción y un 65% más débil ante fuerzas transversales. El hueso puede haber cicatrizado hasta el cuello liso metálico del módulo crestal desde la inserción del implante hasta su reentrada; pero cuando se coloca bajo condiciones de carga, la interfase más débil puede sobrecargar más fácilmente el hueso. La primera rosca u otra zona rugosa de la superficie del implante es el lugar donde cambia el tipo de fuerza de initialmente transversal a carga compresiva o de tracción. Por tanto en numerosas situaciones, el aumento de fuerza del hueso del 35 al 65%, a través de cambios de cargas transversas a compresivas y/o de tracción, es suficiente para detener el proceso de pérdida ósea. Esta puede ser una de las razones por las que los diseños de implantes con un cuello pulido de 2 o 4 mm por encima de la primera rosca pierden hueso hasta esta primera rosca «frontera» (fig. 4-30).
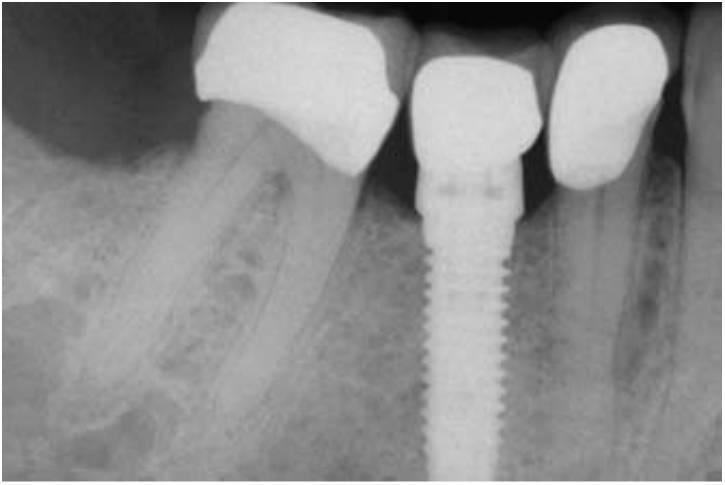
Una revisión previa observó la media de pérdida ósea en relación a los diferentes tipos de diseños de implantes. Al poder afectar el diseño del módulo crestal del implante a la cantidad de pérdida ósea, y su diseño contribuir a la transferencia de la fuerza a la interfase hueso-implante, se refuerza la teoría relacionada con el estrés como una de las causas de pérdida ósea (fig. 4-31).
Toda la literatura acerca de la biomecánica celular, de los principios de ingeniería, de las diferencias de pérdidas óseas relacionadas con la densidad ósea, los estudios animales y los informes clínicos fundamentan que la sobrecarga oclusal pueda ser una causa de pérdida ósea periimplantaria. La literatura relacionada con los aparatos ortopédicos de sustitución de las articulaciones indican claramente que el estrés biomecánico y la sobrecarga contribuyen a la pérdida ósea en la interfase del implante. El aumento de la organización y mineralización ósea durante el primer año, el aumento de la densidad ósea en la interfase del implante, y el tipo de cambio de fuerzas en la primera rosca del cuerpo del implante son todos factores que pueden detener el fenómeno de pérdida ósea después de la pérdida marginal inicial. Aunque este concepto de sobrecarga oclusal no niega la relación de otros factores con la pérdida ósea marginal, es más dependiente de la clínica que la mayoría de los demás parámetros. Los planes de tratamiento que hacen énfasis en la reducción del estrés oclusal en la prótesis son por tanto preceptivos.
Efecto sobre la planificación del tratamiento
Entender las relaciones del estrés y las complicaciones con él relacionadas proporciona una base para un sistema de tratamiento consistente. Un concepto general de ingeniería consiste en determinar la causa de una complicación y desarrollar un método que reduzca las condiciones que causan el problema. El éxito clínico y longevidad de los implantes dentales endósticos como pilares de soporte de carga están ampliamente controlados por el medio biomecánico en el que funcionan. El teorema del tratamiento del estrés, desarrollado por el autor, indica que la mayoría de los tratamientos relacionados con la ciencia de la odontología implantológica deberían centrarse alrededor de los aspectos biomecánicos del estrés.
Las condiciones relacionadas con el estrés que afectan a la planificación del tratamiento en la odontología implantológica incluyen la pérdida de volumen óseo después de la pérdida del diente, las complicaciones de la cirugía, el posicionamiento del implante, la cicatrización inicial de la interfase del implante, la carga inicial de un implante, el diseño del implante, los conceptos oclusales, la fijación de la prótesis, la pérdida ósea marginal, el fracaso del implante, el componente de fractura, la fractura de la prótesis y la fractura del implante. Los parámetros biomecánicos son unos excelentes pronosticadores de los riesgos incrementados porque son objetivos y pueden medirse. No solo se puede predecir qué condición presenta mayor estrés, y por tanto el mayor riesgo, sino también en cuánto ha aumentado dicho riesgo.
Un factor de riesgo no es una contraindicación absoluta, pero aumenta significativamente la media de complicaciones. Con tantas variables, el éxito o el fracaso en la odontología implantológica suele ser un tema complejo y no necesariamente una ciencia exacta. Pero esto no significa que no se pueda establecer un método para disminuir el riesgo. Por ejemplo, el fumar es un factor de riesgo para la longevidad.
Un fumador a largo plazo tiene un 75 % menos de posibilidades de vivir más allá de los 75 años. Esto no significa que un fumador a largo plazo siempre muera antes de la media de vida de los no fumadores (el fumar no es un veneno que mate inmediatamente). Varios años atrás, la persona de más edad del planeta, que tenía 116 años, era un fumador. En cualquier caso, esto no niega que el hecho de fumar sea un factor de riesgo considerable para la longevidad. Del mismo modo los factores de fuerzas son un factor de riesgo considerable. Las mayores fuerzas en un aspecto del tratamiento no son siempre sinónimo de fracaso del implante o de complicaciones, especialmente cuando hay tantos factores involucrados, incluyendo la densidad del hueso alrededor del implante. Aunque los riesgos pueden disminuir considerablemente atenuando el estrés sobre el conjunto del sistema.
Para valorar el aumento de los factores de riesgo, cada factor debe ser considerado separadamente. El objetivo es disminuir el riesgo global.
Entender las relaciones entre el estrés y las complicaciones con él relacionadas proporciona una base para un sistema de tratamiento consistente. El teorema del tratamiento del estrés ha evolucionado hacia una secuencia particular de planificación del tratamiento (cuadro 4-3).
Diseño de la prótesis
Los pacientes edéntulos parciales o completos quieren dientes, no implantes. El resultado final (la prótesis) debería ser planificado prioritariamente respecto de los fundamentos (los implantes). El diseño de la prótesis está relacionado con un número de factores. Casi la mayoría de los tratamientos para pacientes parcialmente edéntulos son planificados como una restauración fija. La restauración fija debe tener en cuenta al tejido blando y si requiere un enfoque quirúrgico o de sustitución de prótesis.
Los pacientes completamente edéntulos deben ser tratados con una sobredentadura removible o una prótesis fija. En cualquiera de los enfoques, la pérdida ósea debida a la pérdida del diente y los métodos para reducir la pérdida ósea futura forman parte de la planificación del tratamiento. Prácticamente todos los pacientes deberían llevar con el tiempo una restauración completamente implantosoportada (cap. 5).
Factores de fuerza del paciente
Un equipo implantológico debería evaluar más de 60 puntos antes de desarrollar una planificación de tratamiento. De todas estas condiciones, los factores que influyen en la cantidad de estrés en el paciente deberían influir en el tratamiento más que varios de los otros factores combinados. Puesto que el estrés es igual a la fuerza dividida por el área en la que estas fuerzas son aplicadas, la cantidad de fuerza está directamente relacionada con la cantidad de estrés. Se deben considerar varios factores de fuerza, incluyendo: 1) el bruxismo, 2) el apretamiento, 3) el empuje de la lengua, 4) la altura de la corona, 5) la dinámica masticatoria y 6) la arcada antagonista. Las fuerzas aplicadas sobre la restauración difieren también por su 1) magnitud, 2) duración, 3) tipo y 4) factores predisponentes (ej. los cantilevers).
Los factores de fuerza de algunos pacientes son más importantes que otros. Por ejemplo, un bruxismo severo es el factor más significativo y, en una escala de riesgo del 1 al 10, es un 10. Las fuerzas del bruxismo suelen ser las más difíciles de contener a largo plazo. Como resultado de esta condición, tienen más facilidad para producirse la pérdida ósea marginal en el implante, la no retención de los pilares, y fracturas por fatiga de los implantes o de las prótesis. El aumento de la magnitud y duración de la fuerza es un problema significativo. El paciente con bruxismo es un paciente de alto riesgo en dos sentidos. La magnitud de la fuerza aumenta porque los músculos se vuelven más fuertes y el número de ciclos del componente protésico es mayor como resultado de la parafunción. Con el tiempo «algo» se romperá si la enfermedad oclusal no puede ser reducida en intensidad y duración. No se pueden esperar resultados protésicos a largo plazo exentos de problemas en pacientes con bruxismo severo.
El segundo factor de alto riesgo es el apretamiento severo, que está en el 9 en la escala de riesgo. Los cantilevers, incluyendo la altura de las coronas, son los siguientes en la lista, seguidos de la dinámica masticatoria de los músculos. La posición del implante en la arcada es seguida por la dirección de la carga, con un riesgo de 5. Estos números son arbitrarios, al estar influenciados por los otros factores de fuerza. Por ejemplo, las fuerzas anguladas más de 30 grados respecto del cuerpo del implante son más dañinas que una altura de corona de 20 mm con una carga sobre el eje longitudinal. El odontólogo debería evaluar el número de condiciones de fuerza y la severidad de sus factores de influencia. Al aumentar el número total, el riesgo aumenta, y la planificación del tratamiento global debería ser modificada para disminuir la fuerza aumentada o ampliando el área de soporte (cap. 6).
Densidad ósea
La densidad del hueso está directamente relacionada con la resistencia del mismo. Misch y cols, habían informado sobre las propiedades biomecánicas de cuatro diferentes densidades óseas en las mandíbulas. El denso hueso cortical es 10 veces más fuerte que el blando, fino hueso trabecular. El hueso D2 es aproximadamente un 50 % más fuerte que el hueso D3. Adicionalmente, la rigidez del hueso se ve afectada por la densidad del hueso. El módulo de Young para el hueso compacto es 10 veces más grande que el hueso esponjoso. Cuanto más denso sea el hueso, más rígido será, y menor será la mala combinación biomecánica del titanio durante la carga.
La carga ósea progresiva cambia la cantidad y densidad del contacto hueso-implante. Se le da tiempo al hueso para responder a un aumento gradual en la carga oclusal. Esto aumenta la cantidad de hueso en la interfase del implante, mejora la densidad ósea y mejora el mecanismo global del sistema de soporte.
Posiciones clave de los implantes y el número de implante/pilar
Posiciones clave de los implantes
En cualquier prótesis, existen unas posiciones de los implantes que son más importantes desde una perspectiva de gestión del estrés. En las prótesis de una o dos unidades, un implante debería ser colocado en cada posición prospectiva del diente, sin corona de contorno de cantilever alguna en dirección alguna (ej. facial, lingual, mesial o distal). En una restauración de tres a cuatro unidades, los pilares más importantes son los pilares terminales. Si no está presente un pilar terminal, se crea un cantilever, lo que magnifica el estrés en el resto del sistema de soporte. Los cantilevers son un amplificador de fuerza que representa un factor de riesgo considerable para un implante de soporte, una pérdida de tornillo, una pérdida ósea en la cresta, una fractura y cualquier otro elemento afectado negativamente por la fuerza. Por tanto la posición debería tener como objetivo la eliminación de cantilevers cuando fuera posible, especialmente cuando otros factores de fuerza están aumentados.
En una prótesis de 5 a 14 unidades, los pilares intermedios también son importantes para limitar los espacios edéntulos a menos de tres pónticos. Una prótesis de tres pónticos se dobla 18 veces más que una prótesis de dos pónticos, mientras que una restauración de dos pónticos se dobla 8 veces más que una de un póntico. Se sugiere que múltiples dientes adyacentes perdidos sean reemplazados con posiciones escalonadas (efecto trípode), o mediante la inserción de un implante intermedio de mayor tamaño.
La posición del canino es una posición importante para un implante siempre que falten el canino y dos dientes adyacentes. De ahí que, cuando faltan los dos premolares, ya sea un primer premolar y uno lateral o uno lateral y uno central, cerca del canino, esté justificado un implante de canino.
Una mandíbula edéntula puede dividirse en tres secciones desde un punto de vista biomecánico: la anterior (de canino a canino) y las regiones posteriores bilaterales (premolares y molares). Una posición clave para los implantes consiste en un implante en cada región, al menos tres implantes claves.
Un maxilar edéntulo puede dividirse en cinco secciones: la región anterior (laterales y centrales), los caninos bilaterales, y la región bilateral posterior (premolar y molar). Una posición clave para los implantes consiste en un implante en cada región, o al menos cinco implantes claves.
Los planes de tratamiento deberían incorporar métodos para reducir el estrés y minimizar sus complicaciones iniciales y a largo plazo. Existen varios parámetros diferentes bajo el control del odontólogo para mejorar el entorno de la región transósea para dominar el estrés alrededor y en el interior de los implantes endósticos. La definición de estrés es la fuerza dividida por el área funcional sobre la que está aplicado. Un enfoque biomecánico para reducir el estrés consiste en aumentar el área de la superficie del sistema de soporte del implante (cap. 8).
El estrés global sobre todo el sistema del implante puede reducirse aumentando el área sobre la que está aplicada la fuerza. El método más efectivo para aumentar el área de la superficie de soporte del implante consiste en aumentar el número de implantes de soporte de la prótesis (fig. 4-32). Por ejemplo, estudios previos de Bidez y Misch han demostrado que la fuerza distribuida sobre tres pilares da como resultado un estrés menos localizado en la cresta del hueso que con dos pilares. Este estudio se aplica únicamente a los implantes que están ferulizados conjuntamente. De ahí que, cuando las fuerzas están aumentadas, debería reducirse el número de pónticos y aumentar el de pilares de implantes, en comparación con la planificación de tratamiento para un paciente ideal con factores de fuerza mínimos.
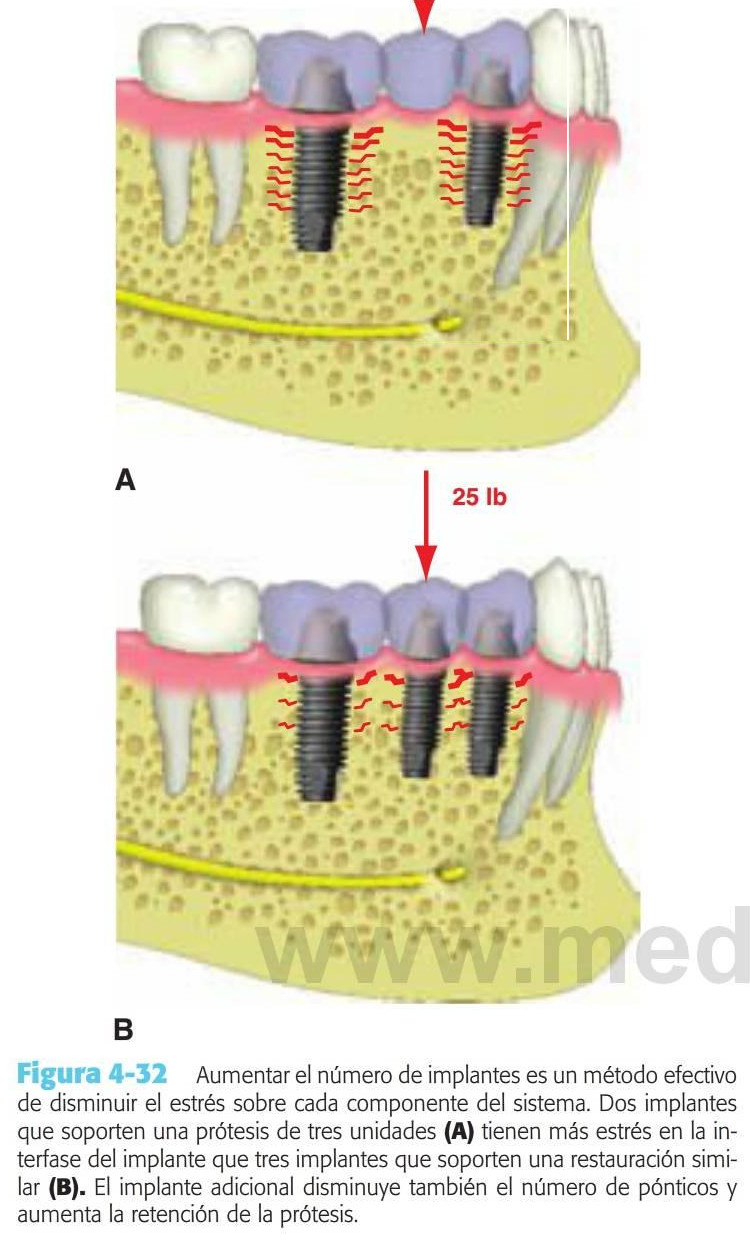
La retención de la prótesis también se ve mejorada con un mayor número de pilares ferulizados. Este enfoque disminuye también la incidencia de las restauraciones no retenidas. Los implantes ferulizados disminuyen también las fracturas de la porcelana. Se reduce la cantidad global de estrés sobre el sistema, y los rebordes marginales de las coronas de los implantes son soportadas por las conexiones de las coronas ferulizadas, dando como resultado más fuerzas compresivas que las cargas intermitentes sobre la porcelana.
El sentido común clínico indica que es mejor errar con un implante adicional que errar con uno de menos. Con un implante de menos, puede fracasar todo el tratamiento. Con un implante de más, raramente suele observarse como un problema. Colocar un implante para cada raíz bucal suele estar indicado raramente, independientemente del número total de factores de riesgo. En cualquier caso, se puede indicar un implante para cada diente perdido en las regiones posteriores de la boca para un paciente varón, grande y joven con una parafunción severa. Es raro que se requieran más de 10 implantes en un arco completamente edéntulo, y es aún más raro sugerir menos de cinco implantes.
El tamaño del implante
Una longitud excesiva del implante no es tan crítica en la interfase ósea de la cresta, si no más bien para la estabilidad inicial y la cantidad global de interfase hueso-implante. Un aumento de la longitud proporciona también una mayor resistencia a fuerzas de torque o transversas cuando se atornillan los pilares en su sitio. En cualquier caso, la longitud excesiva hace bien poco para reducir el estrés que se produce en la región transósea alrededor del implante en la cresta del reborde durante la carga oclusal. Una longitud excesiva del implante no es un método tan efectivo para disminuir el estrés ocasionado por los factores de fuerza.
Por otra parte, con una gestión biomecánica incorrecta, los implantes más cortos pueden tener medias de fracaso más altas después de la carga. Por tanto, el plan de tratamiento inicial debería emplear implantes de por lo menos 12 mm de longitud. De una manera ideal, los huesos de tipo más blando requieren implantes más largos que el hueso denso. El área de la superficie de cada implante esté directamente relacionada con la anchura del implante. Los implantes con forma de raíz más ancha tienen una mayor área de contacto óseo que los implantes estrechos (o de diseño similar), como resultado del incremento de la circunferencia de sus áreas de contacto óseo. Cada aumento de 0,25 mm en el diámetro del implante puede aumentar aproximadamente el área de la superficie entre un 5 y un 10% en un implante de cuerpo cilíndrico. El aumento de la anchura ósea puede estar indicado para aumentar el diámetro del implante de 1 mm cuando los factores de fuerza son mayores de lo ideal. Además se ha sugerido que un aumento en el diámetro del implante puede ser más efectivo que escalonar los implantes para reducir el estrés.
Es interesante tener en cuenta que los dientes naturales son más estrechos en las regiones anteriores de la boca, donde la cantidad de fuerza generada es menor. El diámetro de los dientes naturales aumenta en la región premolar y de nuevo en la región molar donde aumenta la cantidad de fuerza, con un aumento del 300 % de la superficie del área desde los dientes anteriores más bajos hasta llegar a los molares. La longitud de las raíces de los dientes naturales no aumenta de la región anterior a las regiones posteriores del arco, pero sí su sección. El soporte de implante suplementario ganado mediante un mayor diámetro, no solo disminuye el estrés, sino que además disminuye la probabilidad de fracturas del implante y reduce la fuerza en el tornillo del pilar, lo que resulta en un menor aflojamiento de los tornillos (cap. 9).
Hueso disponible
Una vez que se han determinado todos los pasos previos de la secuencia del plan de tratamiento, se evalúa la cantidad de hueso disponible en los lechos implantológicos potenciales. Si está presente la cantidad adecuada de hueso para la posición del número, tamaño y diseño de los implantes preseleccionados, la secuencia del tratamiento procede al siguiente factor. Si no está presente la cantidad de hueso disponible, se requiere el aumento o modificación del hueso. Si estas opciones no son posibles, la secuencia del tratamiento se vuelve a iniciar, empezando por el diseño de la prótesis.
En el pasado, la cantidad de hueso disponible era la primera condición evaluada y el tratamiento continúa, basado en el número y posición de los implantes, prestando poca atención al tamaño o al diseño. Este enfoque conlleva con frecuencia a las altas medias de complicaciones relacionadas con las condiciones de aumento del estrés (cap. 10).
Diseño del implante
El macrodiseño del implante puede afectar al área de la superficie incluso más que un aumento de la anchura. Un implante cilíndrico (en forma de bala) proporciona un 30 % menos de área de superficie que un implante roscado convencional del mismo tamaño. Strong y cols, han identificado 11 variables diferentes que pueden afectar al área de la superficie funcional global de un implante. Un implante roscado con 10 espiras por cada 10 mm tiene un área de superficie mayor que uno con 5 espiras Una espira de 0,2 mm de profundidad tiene menos área de superficie que un implante con 0,4 mm. De ahí que el diseño del implante pueda ser el método más fácil para aumentar el área de superficie de manera significativa y disminuir el riesgo global en la interfase del implante (cap. 11).
Además del teorema del estrés y la secuencia relativa de la planificación del tratamiento, se han desarrollado unos corolarios para facilitar la selección del tratamiento más apropiado (cuadro 4-4).
Resumen
La comprensión de la etiología de las complicaciones más comunes de los implantes ha llevado al desarrollo de un teorema para la planificación del tratamiento basado en el estrés. Una vez que el odontólogo implantólogo ha identificado las fuentes de las fuerzas sobre el sistema de implantes, se puede diseñar el plan de tratamiento para minimizar su impacto negativo sobre el implante, el hueso y sobre la restauración final. Bajo estas condiciones, una solución consistente es el aumentar el área de la superficie hueso-implante. Los implantes suplementarios son la solución escogida para disminuir el estrés, junto con un aumento del ancho o de la altura del implante y el empleo de más implantes para disminuir el número de pónticos para disipar el estrés de manera más efectiva de la estructura ósea, especialmente en la cresta. La retención de la prótesis final o de la superestructura se ve mejorada aún más con pilares implantológicos adicionales. La cantidad de hueso en contacto con el implante aumenta como múltiplo del número de implantes.