El Recién Nacido
Adaptación a la vida extrauterina
A. Definición de recién nacido o neonato
La OMS recomienda incluir como nacidos vivos a todos aquellos niños que tienen al nacer alguna señal de vida: respiración o palpitaciones del corazón o cordón umbilical, o movimientos efectivos de músculos de contracción voluntaria. En los fallecidos se considera sólo a aquellos que pesan más de 500 gramos.
Según la SEGO (2008) nacido vivo:
Es la expulsión completa o la extracción de su madre de un producto de concepción, independientemente de la duración del embarazo y el cual, después de dicha separación, respira o muestra cualquier otra evidencia de vida, tal como latido del corazón, pulsación del cordón umbilical o movimiento apreciable de los músculos voluntarios, aparte de que se haya cortado o no el cordón umbilical o la placenta permanezca unida. Cada producto de icho nacimiento es considerado un/a nacido/a vivo/a.
B. Recuerdo anatomofisiológico de la etapa fetal
a. Respiración fetal, papel de la placenta
En la vida intrauterina, el feto respira a través de la placenta, órgano encargado además del aporte de O2 al feto, de la captación de CO2 del torrente sanguíneo fetal, así como del aporte de nutrientes y eliminación de sustancias de desecho. Por ello, podemos decir que la placenta hace las veces del pulmón fetal, hígado, intestino e incluso riñones en la vida intrauterina.
En el periodo intrauterino, el pulmón fetal no tiene desarrollada su función de intercambio gaseoso, por lo que se encuentra hipoperfundido, mediante mecanismos que veremos más adelante, manteniendo un flujo sanguíneo mínimo y suficiente para la oxigenación tisular. Aunque en la vida extrauterina de su óptimo funcionamiento depende la vida del neonato, en el periodo fetal es precisamente uno de los órganos que se sacrifican en casos de hipoxia intrauterina, con la consiguiente cascada de fallos funcionales en el pulmón neonatal. Todo ello lo veremos en capítulos posteriores.
El tejido pulmonar tiende al colapso, en el medio aéreo esto se evita, entre otros mecanismos, gracias al Volumen Residual y al surfactante. El crecimiento normal pulmonar intrauterino depende, en gran medida, del balance entre una adecuada producción y un drenaje controlado de líquido pulmonar; por ejemplo, en caso de obstrucción traqueal, el drenado de secreciones se ve comprometido, con la consiguiente sobredistensión del pulmón y la alteración de las células alveolares tipo II. Otro ejemplo es la hipoplasia pulmonar, en caso de oclusión de la arteria pulmonar, compresión del tórax por oligoamnios crónico o hernia diafragmática.
En el control del estado fetal, los movimientos respiratorios fetales (que se producen en la fase R.E.M. del sueño fetal) son indicativos de bienestar fetal
En la vida intrauterina el surfactante (sustancia tensoactiva producida por los neumocitos tipo II) comienza a producirse desde la semana 20, es en la semana 26- 28 cuando podría ser capaz de desarrollar su función (lo que justificaría el uso de corticoides IM maternos, para aumentar la producción del mismo en situaciones de riesgo de parto pretérmino), pero no es hasta semana 35 que alcanza su madurez funcional fisiológica (edad gestacional hasta la que se consideran necesarios los corticoides para la “maduración pulmonar fetal”).
El surfactante es un complejo de proteínas, fosfolípidos y carbohidratos, siendo el componente principal la fosfatidil-colina, que representa el 70 % de los lípidos, un 60 % de ella en forma de dipalmitoil-fosfatidil-colina (DPPC), principal componente del surfactante para reducir la tensión superficial de la interfase aire - líquido alveolar.
Se han descrito cuatro proteínas asociadas al surfactante:
- SP-A interviene en la secreción y reciclaje del surfactante y en la estabilización de la mielina tubular, aumentando su actividad. También tiene un importante papel en las defensas del huésped.
- SP-B aumenta la acción superficial de los fosfolípidos, facilitando su reciclado por los neumocitos tipo II. Su déficit causa un cuadro de dificultad respiratoria en el RN a término.
- SP-C aumenta el reciclado de los fosfolípidos, habiéndose descrito una enfermedad pulmonar asociada a su déficit.
- La función de la SP-D no es bien conocida, pero su presencia facilita la rápida distribución del surfactante en la interfase aire-líquido.
Existen otras proteínas presentes en el lavado bronco-alveolar cuya función no se ha determinado con precisión.
El efecto de los corticoides en la maduración pulmonar sería el siguiente:
- Modulan la síntesis de lecitina y proteínas del surfactante.
- Provocan una inducción de los receptores β adrenérgicos de los neumocitos tipo II.
- Modifican el parénquima pulmonar y disminuyen el edema.
- Producen una maduración de los sistemas antioxidantes.
Sin el efecto del surfactante en el pulmón neonatal, éste no sería capaz de cumplir su misión de intercambio gaseoso y se avocaría a un fallo multiorgánico.
Hemos hecho referencia al Volumen Residual como otro mecanismo fundamental en la fisiología de la respiración, pero intraútero, este mecanismo de prevención del colapso pulmonar se realiza por las propias secreciones pulmonares, que serán eliminadas al nacimiento para ser renovadas por el aire ambiente, mediante primero, la compresión del canal del parto sobre el tórax fetal, las propias respiraciones y, fundamentalmente, mediante la reabsorción linfática de las mismas. Es por ello, que una alteración en alguno de los siguientes mecanismos conllevará a una mala ventilación en el RN:
- Parto por cesárea: nula compresión torácica.
- Dificultad en las primeras respiraciones.
- Escasa reabsorción de las secreciones pulmonares.
b. Circulación fetal
La circulación fetal es un conjunto de mecanismos adaptativos a las necesidades del feto que, tras el nacimiento, sufren y deben sufrir unos cambios drásticos y fundamentales para su funcionalidad en el neonato. De la adecuada transición de la circulación fetal a la circulación neonatal, dependerá la supervivencia del RN.
La sangre oxigenada le llega al feto a través de la vena umbilical.
La sangre venosa o de retorno, sale del feto en dirección a la placenta a través de las dos arterias umbilicales.
Definimos a continuación los mecanismos encaminados a saltar el paso circulatorio hacia el pulmón, órgano que no recibirá su flujo sanguíneo total hasta la primera respiración.
Agujero oval: comunicación valvular entre la aurícula derecha y la izquierda.
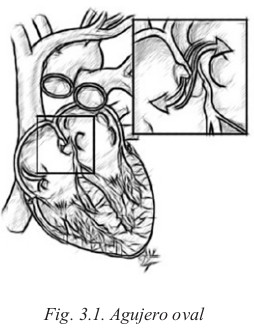
Ductus arterioso: comunicación entre arterias pulmonares y arteria aorta.
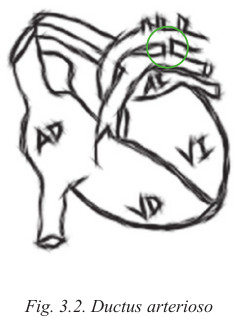
C. Cambios tras el nacimiento
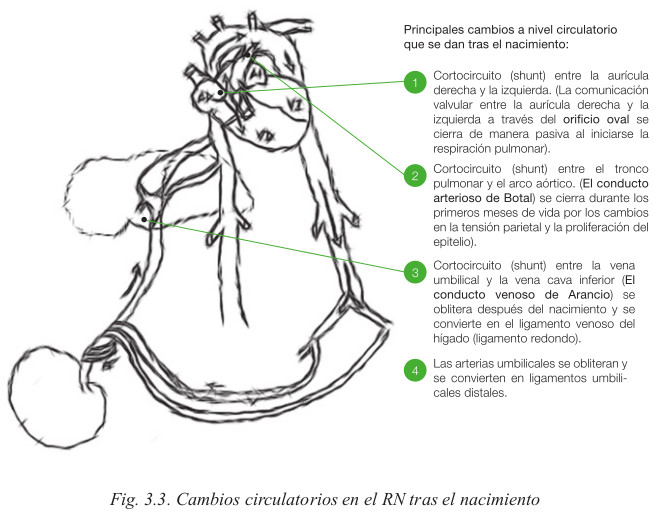
Vamos a analizar los cambios circulatorios que se producen tras el nacimiento (los cambios respiratorios los analizaremos más adelante en el tema 4) que son, principalmente, los siguientes:
Cierre del foramen oval: con la primera respiración se produce la dilatación de las arterias pulmonares y una cascada de acontecimientos, que llevan a una disminución de la resistencia pulmonar y a una disminución de la presión del corazón derecho, además aumenta la presión hidrostática de la aurícula izquierda. Todo ello, hará que se cierre funcionalmente el foramen oval, porque el cierre permanente ocurrirá varios meses después del nacimiento. Hasta que se produzca el cierre anatómico, puede existir cierta comunicación que dará lugar a un murmullo cardiaco fisiológico.
Cierre del ductus arterioso: el ductus arterioso es sensible a los niveles de O2 y a las prostaglandinas endógenas del RN (PGE2 y PGI2), que produce entre otros su cierre aproximadamente a las 15 horas de vida, y definitivamente a las 3 semanas.
La hipoxemia mantenida puede producir una persistencia del ductus arterioso.
Cierre del ductus venoso: tras clampar el cordón umbilical, se produce el progresivo cierre del ductus venoso hasta la fibrosis de este shunt en la primera semana de vida.
Cierre de los vasos umbilicales: se produce tras el clampado del cordón.
Aumento de las resistencias vasculares sistémicas.
Disminución de las resistencias vasculares pulmonares.
Aumento del flujo sanguíneo pulmonar.
Aumento del gasto cardíaco del RN, gracias a la maduración perinatal de los receptores βadrenérgicos mediado por el aumento de hormonas tiroideas, lo que le permite manejar el nuevo circuito sanguíneo.

Valoración del estado de salud del neonato. Test de Apgar. Exploración física. Evaluación del peso y la edad gestacional. Clasificación de los recién nacidos según peso y edad gestacional
A. Valoración del estado de salud del RN test de Apgar
Se trata de una escala de valoración inicial del RN. Consta de 5 parámetros (frecuencia cardiaca, respiración, tono, reflejos y coloración) puntuados de 0 a 2, (siendo 0 la puntuación más desfavorable) que se analizan al minuto de vida y a los cinco minutos de vida, lo que nos da una aproximación a la adaptación extrauterina del RN; nos orienta a las maniobras que se deben realizar sobre el RN, aunque con los nuevos algoritmos de reanimación en sala de partos, las primeras intervenciones se realizan a los 30 segundos de vida.
No indica necesariamente el compromiso fetal intraútero, aunque sí tiene valor predictivo el puntaje a los 5 minutos y a los 10 minutos. A los 5 minutos el test de Apgar indica la efectividad de la reanimación. La realización del test de Apgar posteriormente dependerá de la evolución del recién nacido, y se realizará cuando en ese momento se prosiga la reanimación del mismo. A pesar de que el test no guarda relación de forma general con el pronóstico neurológico a largo plazo del niño, se ha demostrado un peor desarrollo neurológico en los niños que presentan una puntuación menor de 6 a los 20 minutos de vida.
Es importante destacar que aplicando la escala antes del minuto de vida, falsearíamos los resultados y la impresión diagnóstica en el RN, ya que podríamos determinar actuaciones no necesarias en las horas posteriores al nacimiento, rompiendo un posible C.P.P. e impidiendo un inicio precoz de la lactancia materna.
- La frecuencia cardíaca normal en el RN es de 120-160 lpm, con ritmo regular. Comprobar que los pulsos femorales y humerales tengan la misma amplitud (para descartar la presencia de una coartación de aorta).
- El esfuerzo respiratorio se valora mediante el llanto del neonato, ya que si un niño llora vigorosamente será favorable. La frecuencia respiratoria normal oscila entre 40 y 60 rpm. Es más periódica que regular; pudiendo presentar pausas respiratorias fisiológicas no superiores a 10-15 seg (Apneas).
- La irritabilidad refleja se valora con la introducción de una sonda nasogástrica por la nariz, se le da una puntuación según la reactividad del RN, pudiendo no reaccionar (0), hacer una ligera mueca (1) o reaccionar con tos o un estornudo ante la introducción (2).
- El tono muscular valora la postura en la que se encuentra el RN, pudiendo estar flácido y débil (0), encontrarse con una ligera flexión de las extremidades, pero algo hipotónico (1) o la mejor puntuación es que tenga buen tono con movimientos activos de las extremidades.
- La coloración es el ítem que hace que la mayoría de los recién nacidos en perfecto estado no tengan puntuación 10 sino 9, ya que es fisiológico y frecuente en las primeras 24 horas de vida, que presenten una acrocianosis en manos y pies (coloración azulada de la piel), debido a una inestabilidad vasomotora.
Conviene advertir que la valoración de la irritabilidad refleja se realiza con el estímulo y respuesta ante el paso de sonda nasogástrica por la nariz, aunque esa rutina en cuidados inmediatos en el RN ya está desterrada, con lo que la valoración de este parámetro no es real si no es preciso el paso de sonda (asumiremos un 2 en la valoración del reflejo en caso de un RN reactivo con buen tono y llanto en el momento del nacimiento).

La valoración del test es la siguiente:
- Apgar de 0 a 3 → nos indica dificultades marcadas para adaptarse a la vida extrauterina, un recién nacido intensamente deprimido.
- Apgar de 4 a 6 → unas dificultades moderadas, recién nacido moderadamente deprimido.
- Apgar de 7 a 10 → ausencia de dificultades, estado satisfactorio.
B. Valoración de las características físicas
Piel: la piel del recién nacido pretérmino se ve delgada y transparente, las venas son prominentes en el abdomen en una etapa temprana de la gestación. A medida que se aproxima el término del embarazo, la piel se ve opacada por el aumento de tejido subcutáneo. La desaparición de la vérnix caseosa protectora promueve la descamación cutánea que con frecuencia, se observa en lactantes postérmino.
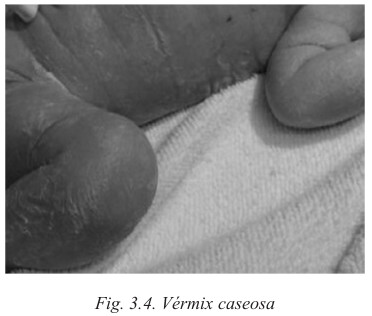
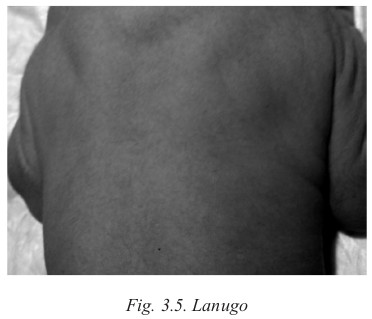
Lanugo: la cubierta de pelo fino, disminuye conforme aumenta la edad gestacional. La cantidad de lanugo alcanza el máximo a las 28-30 semanas y luego, desaparece, primero de la cara, luego del tronco y las extremidades.
Pliegues plantares: son indicadores fiables de la edad gestacional en las primeras 12 horas de vida. Después de este tiempo, la piel del pie empieza a secarse y aparecen pliegues superficiales. El desarrollo de los pliegues plantares empieza en la parte superior (anterior) de la planta y conforme progresa el embarazo, avanza hacia el talón. También puede existir descamación. Varían con la raza, los neonatos negros pueden tener menos desarrollados los pliegues al término del embarazo.
Mamas: se palpa el tejido mamario con suavidad, con la yema de los dedos y se mide. Al término del embarazo medirá entre 5 y 10 mm. Conforme avanza el embarazo aumenta la masa de tejido mamario y la areola. Sin embargo, puede existir una masa grande de tejido mamario por situaciones distintas a la edad gestacional avanzada, o los efectos de las hormonas maternas sobre el recién nacido.
Forma de la oreja y distribución del cartílago: se desarrollan con la edad gestacional. En un recién nacido menor de 34 semanas, la oreja es relativamente imperfecta y plana, tiene poco cartílago, por lo que se pliega sobre sí misma y permanece doblada. Cerca de las 36 semanas, existe un poco de cartílago y una curva ligera en la parte superior del pabellón, el cual regresa a su sitio despacio cuando se dobla. Al término del embarazo, el pabellón auricular del recién nacido es firme, permanece erecto alejado de la cabeza y regresa rápido cuando se pliega.
Genitales masculinos: se valoran en cuanto al saco escrotal, la presencia de arrugas y el descenso de los testículos. Antes de las 36 semanas, el pequeño escroto tiene pocas arrugas y los testículos son palpables en el canal inguinal. Hacia la semana 36-38, los testículos están en la parte superior del escroto y ya se desarrollaron arrugas sobre su cara anterior. Al término del embarazo, casi siempre los testículos están en la parte baja del escroto, el cual es péndulo y cubierto de arrugas.
Genitales femeninos: su apariencia depende en parte del depósito de grasa subcutánea del feto, y por eso, se relaciona con el estado nutricional de éste. El tamaño del clítoris varía. Hacia las 30-32 semanas, el clítoris es prominente y los labios mayores son pequeños y separados, los labios menores suelen cubrir a los mayores; conforme aumenta la edad gestacional crecen los labios mayores. A las 36-40 semanas casi cubren el clítoris. A las 40 semanas y después los labios mayores cubren a los menores y al clítoris.
C. Exploración física del RN
- Somatometría (RN a término) valores promedio:
Peso: 2500-4.000 g
En la primera semana el peso desciende aproximadamente 5-10 %
Talla: 48-52 cm
Perímetro cefálico: 32-36 cm
Perímetro torácico: 31-35 cm
- Piel:
- Coloración: la coloración del RN depende de la desadaptación térmica inicial (violáceo) y de la progresiva normalización de los niveles de saturación de oxígeno en sangre neonatal hasta llegar al tono rosado normal del RN.
- Podremos encontrarnos RN pletóricos en caso de policitemia, que puede ser debida a una situación de hipoxia crónica intraútero.
- Vérmix caseoso: protección térmica.
- Lanugo fetal: vello fino.
- Millium facial.
- Mancha mongólica: hallazgo casual que se presenta en región lumbosacra, consistente en una coloración oscura más o menos irregular.
- Exantema toxoalérgico.
- Costra láctea: descamación del cuero cabelludo propia del RN, no presenta interés clínico.
- Signos potencialmente de alarma:
- Ictericia en las primeras 24 h (signo inicial de riesgo de Kernicterus).
- Máscara facial, que puede aparecer en el caso de la presencia de una circular de cordón en el cuello del recién nacido, en el momento del nacimiento.
- Cianosis perilabial, que puede darse en caso de desadaptación térmica al medio.
- Plétora (poliglobulia por hipoxia crónica intraútero, infección, transfusión materno-fetal).
- Palidez (signo de infección, anemia, hemorragias).
- Petequias, no desaparecen a la presión (signo característico en sepsis).
- Manchas en la piel:
- Color café con leche: característica en neurofibromatosis
- Acrómicas: propias del síndrome Struge-Weber
- Exantemas, pústulas, ampollas (signo de infección).
- Muguet, característico de infecciones por hongos.
- Dermatitis del pañal.
- Cráneo:
La exploración del cráneo tiene como objetivo la evidenciación de anomalías no diagnosticadas intraútero. La medición del perímetro cefálico así como la exploración de las fontanelas nos da información sobre la normalidad del mismo.
Las fontanelas son zonas no óseas entre la unión de varios huesos del cráneo para permitir su movilidad durante el parto y en el desarrollo posterior del SNC.
Fontanela anterior o bregmática: forma romboidal y es pulsátil. Se suele cerrar entre los 12-18 meses.
Fontanela posterior o lambdoidea: forma triangular. Se suele cerrar entre los 2-4 meses. La sutura escamosa es la que separa los temporales de los parietales.
Fontanela hundida en el neonato → Signo de deshidratación
- Caput y cefalohematoma (Fig. 3.6):
- Caput succedaneum:
- Colección de líquido entre la aponeurosis y el periostio.
- Es una lesión que puede atravesar las suturas.
- A la palpación se detecta, porque el cráneo está blando, hay una sensación de estar notando líquido en la cabeza.
- Se reabsorbe en un plazo inferior a 48 h.
- Cefalohematoma:
- Se produce una hemorragia entre el periostio y el hueso.
- A la palpación no se nota nada, ya que el líquido está por debajo del hueso.
- No atraviesa suturas.
- Se ve la cabeza deformada.
- El líquido se acaba reabsorbiendo ±2 semanas, porque el líquido está por debajo del hueso, y esta zona está menos vascularizada.

Cara, sin signos de malformación, labio leporino, microrretrognatia (S. Pierre Robin)
Boca, ausencia de dientes (dientes fetales, que son con los que nace el RN, dientes neonatales, que son los que aparecen en las primeras semanas)
Ojos, presencia, simetría, tamaño, hendidura palpebral
- Esclerótica blanca
- No existe producción de lágrimas
- Las pupilas reaccionan a la luz
- Nistagmo o estrabismo normal
- Ausencia de cataratas
- Orejas: implantación y morfología
- Reflejo cocleopalpebral
- Cuello
- Tortícolis
- Hematoma del esternocleidomastoideo
- Fractura de clavícula
- Torax
- Intumescencia mamaria
- Pectus excavatum
- Pectus carinatum
- Genitales
- Femeninos: es normal cierto grado de edema y prominencia
- Pseudomenstruación: debido al paso hormonal de la madre a la hija
- Explorar genitales para evidenciar malformaciones
- Masculinos: exploración y evidencia alteraciones:
- Hidrocele
- Hipospadias
- Epispadias
- Criptorquídia: testículos en abdomen
- Columna vertebral y ano
- Inspeccionar en busca de malformaciones:
- Espina bífida
- Fisuras o fístulas anales
- Ano imperforado
- Extremidades: son cortas en comparación con el resto del cuerpo, inspeccionar en busca de malformaciones
- Sindactilia.
- Polidactilia.
- Agenesia.
- Clinodactilia.
- Fractura de clavícula. Lesión obstétrica más frecuente, investigar si
“chasquido”, macrosoma o dificultad en la salida de los hombros. Dx
crepitación, moro, Rx.
- Parálisis braquial:
- Alta o de Duchenne-Erb: brazo caído e inmóvil (C5-C6)
- Baja o de Dejerine-Klumpke: afecta a la mano (C7-T1)
- Luxación de cadera, Dx:
- Maniobra de Barlow, nos informará sobre una cadera luxable.
- Maniobra de Ortolani, será positiva si la cadera se encuentra luxada.
- Parálisis braquial:
D. Evaluación del peso y la edad gestacional
La valoración del peso y de la EG nos será de vital importancia a la hora de planificar los cuidados del RN. Un RN con peso extremo (>4000 g. ó <2500 g.) precisará de controles de glucemia en el área de partos, según protocolos. Así mismo, la concreción de la madurez del RN será definitiva para la decisión sobre el CPP o la necesidad de remitirlo a la unidad de neonatología. El RN de bajo peso en el nacimiento es más susceptible de sufrir los efectos de la hipotermia en el momento del nacimiento, así como dispone de menores reservas para compensar los cambios bruscos de temperatura, por lo que deberemos esmerar los cuidados encaminados a preservar la temperatura del neonato.
La evaluación del peso del RN es uno de los cuidados demorables en el RN, excepto en el caso que creamos que deberemos realizar algún cuidado específico respecto a ese valor, en cuyo caso está indicada la determinación del peso en la primera hora de vida para poder planificar nuestra actuación.
Existen una serie de indicadores o marcadores que nos hacen determinar, de manera aproximada, la EG del RN que estamos valorando (en caso de que no dispongamos de ese dato).
a. Postura
Se debe valorar la postura mientras el lactante está tumbado sobre una superficie plana.
- Signo de la ventana cuadrada: se busca este signo flexionando la mano del neonato hacia la cara ventral del antebrazo. Se mide el ángulo que se forma en la muñeca. El ángulo de 90º sugiere un recién nacido inmaduro de 28-30 semanas. Él ángulo de 30º a menudo se encuentra en las 38-40 semanas. Cuando el ángulo es de 0º no existe espacio, la edad gestacional estará en torno a las 40-42 semanas.
- Retroceso del brazo: es una prueba de desarrollo de la flexión. El retroceso de los brazos se prueba con la flexión al nivel del codo y extensión de los brazos a los lados del recién nacido. Mientras el lactante está en posición supina, se flexiona por completo ambos codos, los mantiene en esta posición durante 5 segundos, se extienden los brazos a los lados y se libera. En este momento los codos de un recién nacido a término forman un ángulo menor de 90º y regresan rápido a la flexión. Los codos de los neonatos pretérmino tienen un retroceso más lento y tienen un ángulo que no llega a los 90º. El retroceso de los brazos también es más lento en los recién nacidos sanos, pero agotados después del parto, por tanto, esta respuesta se obtiene mejor después de la primera hora de edad, cuando el lactante ya ha tenido tiempo para recuperarse del estrés del parto. La valoración del retroceso de los brazos debe ser bilateral para descartar parálisis braquial.
- Ángulo poplíteo: es el grado de flexión de la rodilla. Se flexiona el muslo sobre el abdomen o tórax y se coloca el dedo índice de la otra mano detrás del tobillo para extender la pierna hasta que se obtenga resistencia. Luego se mide el ángulo. Los resultados varían desde ausencia de resistencia en el lactante muy inmaduro a un ángulo de 80º en el neonato a término.
- Signo de la bufanda: se busca tirando del brazo a través del pecho hacia el hombro opuesto, hasta que se obtenga resistencia. Luego se observa el sitio del codo en relación a la línea media del tórax. No se observa resistencia hasta después de las 30 semanas de gestación. El codo puede moverse con facilidad más allá de la línea media. A las 36-38 semanas el codo llega a la línea media y más allá de las 38-40 semanas el codo no alcanza la línea media.
- Maniobra talón-oreja: se realiza tirando del pie hacia la oreja del mismo lado hasta que se note resistencia. Se valoran tanto el ángulo poplíteo como la proximidad del pie a la oreja. En un neonato muy inmaduro la pierna permanecerá recta y el pie llegará a la oreja o más allá. Las maniobras sobre las extremidades inferiores de los neonatos que mantuvieron una presentación pélvica franca, deben retrasarse para permitir que se normalice la posición de las piernas (Ballard y col., 1979).
b. New Ballard Score
Este test junto con otros como la clasificación de Farr-Dubowitz, el método de Capurro, el test de Usher son los más utilizados para calcular la edad gestacional del recién nacido; basándose en una serie de parámetros físicos y neurológicos. Ya en la década de los 70, autores como Dubowitz idearon métodos clínicos para poder inferir una edad gestacional determinada. Una década más tarde, establecieron otro nuevo método que reducía a 6 las variables físicas y neurológicas por evaluar, y en 1991 Ballard, estableció un nuevo método en el que introdujo algunas modificaciones y al que llamó Nuevo Método de Ballard, con el objetivo de poder utilizarlo en recién nacidos prematuros extremos.
El New Ballard Score (NBS) es un test utilizado para valorar la edad gestacional del neonato en semanas según: la madurez física y la madurez neuromuscular. El NBS es un método clínico utilizado en los distintos servicios de neonatología.

La valoración del NBS se realiza haciendo un sumatorio de las valoraciones: física y neuromuscular. Al tener la suma de ambos parámetros se puede estimar la edad gestacional del recién nacido.
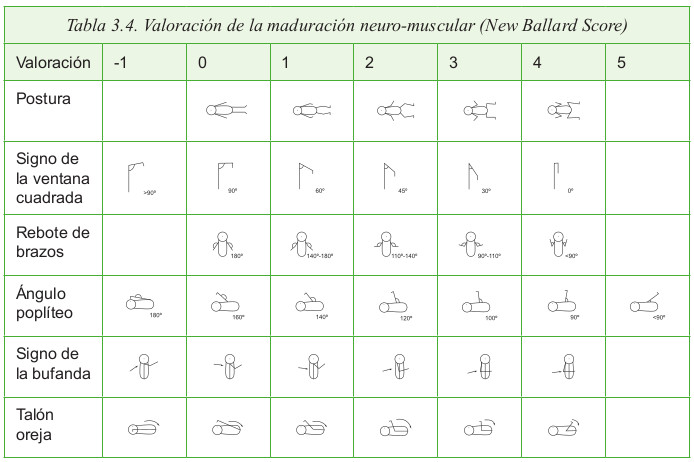
Cada hallazgo físico y neuromuscular tiene un valor y la calificación total se equipara a la edad gestacional. La clasificación máxima según el método de Ballard es 50, el cual corresponde a una edad gestacional de 44 semanas.

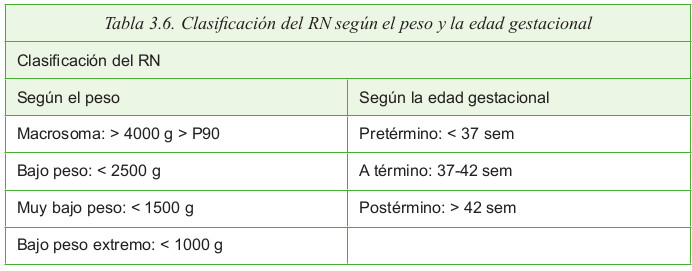
E. Clasificación de los recién nacidos según peso y edad gestacional
Atendiendo al peso o a la EG, podemos clasificar los RN de la siguiente manera:
Atención inmediata al recién nacido. Cuidados inmediatos al recién nacido. Reanimación neonatal: niveles
A. Introducción
La neonatología es una rama de la pediatría que se encarga de la atención del RN, sano o enfermo. Etimológicamente proviene del latín “natos” (nacer) y “logos” (tratado o estudio), es decir el “estudio del recién nacido”.
Los inicios de esta rama de la ciencia datan de 1892, con las aportaciones de Pierre Budin, médico francés, considerado el padre de la Neonatología, quien escribió un libro para lactantes con problemas nacidos de un parto prematuro y diferenció a los lactantes en pequeños y grandes para la edad gestacional.
En 1914, el Dr. Julius Hess en Chicago creó unidades de cuidados para recién nacidos prematuros en el Hospital Michael Reese.
En 1924, Albrecht Peiper centró sus estudios en la maduración neurofisiológica de los recién nacidos prematuros.
La década de los 40 es importante por el comienzo en la unificación de criterios para el manejo de RN pretérminos. Aparecen las primeras incubadoras, destinadas al mantenimiento y estabilización de la Tª de los neonatos; son aportaciones clásicas las de Budin sobre la relación entre la Tª ambiente y la mortalidad del prematuro, siendo el primero en usar botellas de vidrio con agua caliente para termorregulación durante el traslado neonatal.
En 1953, Virginia Apgar desarrolla una escala de valoración del RN que aportaba luz sobre el grado de asfixia perinatal y de adaptación a la vida extrauterina, usada hasta la actualidad.
En 1957, Ethel Dunham escribió el libro “El Prematuro”.
Desde 1960, la cirugía neonatal ha sido cada día más agresiva, lográndose en la actualidad hacer cirugía intrauterina.
En 1967, el Colegio Americano de Ginecología y Obstetricia reconoció la necesidad de la estrecha relación entre el Obstetra y el Neonatólogo, para disminuir la morbimortalidad perinatal, iniciándose en 1973 el primer Servicio de Cuidados Perinatales en EEUU.
En la década de los 70 hubo progresos importantes en la nutrición, la alimentación por sondas y la alimentación parenteral.
En el período reciente, Volpe ha contribuido con la fisiopatología y clasificación de la hemorragia intracraneal y las convulsiones neonatales. Sarnat con la fisiopatología de la encefalopatía hipóxico isquémica.
Desde la década de 1970, se insiste cada vez más en el cuidado especial de enfermería, en los cuidados de asepsia, antisepsia y lavado de manos para prevención de infecciones intrahospitalarias.
Uno de los principales cambios en la neonatología han sido los cuidados intensivos en el RN prematuro, así como los avances en la ventilación mecánica y solución de problemas respiratorios. En 1887, Dwyer utilizó el primer ventilador rudimentario de presión positiva y en 1888 Egon Braun y Alexander Graham Bell introdujeron la presión negativa. En 1953, Donald y Lord introdujeron el uso del ventilador ciclado. En 1971 Gregory, Kitterman y Phibbs introdujeron la Presión Positiva Continua en las vías aéreas (CPAP). Poco después Bird con la colaboración de Kirby, desarrollaron el primer ventilador neonatal a presión positiva, el “Baby Bird”.
Posteriormente, con el estudio y conocimiento de la fisiología respiratoria neonatal, mejoraron notablemente los resultados en la asistencia respiratoria mecánica de los recién nacidos. Destacan las contribuciones de Downes, Anderson, Silverman, Gregory y Fujiwara en la actualidad con el uso de surfactante exógeno.
B. Atención inmediata al recién nacido
La valoración inicial se puede realizar en contacto piel con piel
Clásicamente las intervenciones se basaban en la prevención de complicaciones, históricamente, podemos resumir los cuidados del RN según el siguiente esquema:
RN con la madre → RN con ↑ morbi/mortalidad RN en observación → ↓ complicaciones (mediados S. XX)
Con lo que inferíamos que realizando inmediatamente los cuidados del RN, disminuiríamos la morbimortalidad, pero… ¿Es preciso hacerlo con todos los nacidos?
La respuesta es no, no es preciso realizar cuidados inmediatos generales a todos los RN, debemos individualizar nuestras actuaciones, basándonos en los conocimientos de la fisiología e identificando aquellos neonatos que precisen de nuestras intervenciones.
Minimizar las intervenciones precisa de profesionales cualificados y adiestrados que permitan la evolución espontánea del RN
OMS: hasta en un 20 % de los RN puede ser precisa alguna intervención, de ellos, el 10 % precisa de intervenciones mayores (2 % del total de partos)
Multitud de organismos nacionales e internacionales avalan las intervenciones personalizadas y bogan por evitar los cuidados inmediatos de rutina.
La primera valoración del RN no sólo se basa en ausencia de enfermedad, sino que debe apoyarse en una historia clínica completa y en una clasificación anteparto de factores de riesgo.
Anticipación → conocimiento de signos de malestar intraútero:
- Aparición de meconio
- Deceleraciones
- Bradicardia
- Prematuridad
- CIR
- Macrosomía
- Abuso de drogas
- Patología fetal conocida
RN sano: Aquel sin factores de riesgo y que realiza una transición sin problemas
Vamos a analizar una serie de parámetros en la asistencia del RN en el nacimiento, basándonos en las recomendaciones del SNS, así como de la OMS.
Lugar de nacimiento. La AEP recomienda la asistencia al RN sin factores de riesgo en medio hospitalario para garantizar la asistencia especializada en caso de que lo precise
No se recomienda rutinariamente:
- Paso de sondas (fosas nasales, esófago y/o ano). La simple observación es suficiente para descartar la mayor parte de los problemas graves del RN.
- Lavado o aspiración gástrica rutinaria (riesgo > beneficios).
- Manejo activo RN con meconio.
Contacto piel con piel:
- Prevención de la hipotermia (sincronía térmica, Nills Bergman).
- Silencio, respeto e intimidad, minimización de estímulos.
- No se han encontrado efectos adversos.
- ¿Cuánto tiempo? 50´— 120´.
- Piel con piel en cesáreas.
- Medidas a realizar durante CPP.
- Niño sobre madre (decúbito prono)
- Cubrir con prendas precalentadas
- Valoración APGAR
- Pinzamiento cordón
- Identificación RN
- Colocar gorro
- Valoración toma lactancia
- Demorar acciones innecesarias
Nivel de alerta: Periodos de adaptación del RN*
- Primer periodo (30´vida): reactividad.
- Segundo periodo (30´- 2 h): respuesta disminuida.
- Tercer periodo (2 h – 8 h): reactividad.
Precisamente, durante el segundo periodo de alerta, periodo de respuesta disminuida, es durante el cual se producirá el C.P.P., por lo que tendremos que discriminar entre un RN normal y siguiendo los patrones fisiológicos de respuesta neurológica frente a la posibilidad de no identificar un RN con problemas de adaptación al medio en el contexto de las primeras horas de vida.
C. Cuidados inmediatos al recién nacido
a. Pinzamiento de cordón
Se refiere al momento en el que realizamos el clampado del cordón umbilical y cortamos el vínculo físico del RN con su madre.
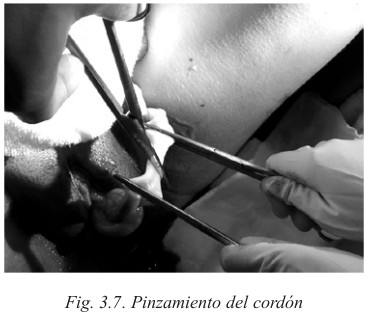
Se clasifica según el tiempo que transcurre hasta que se corta el cordón:
- Precoz (≤ 60 segundos)
- Tardío (2 ó 3 minutos o hasta el cese de pulso en el cordón)
Precoz
Clásicamente se ha realizado pinzamiento precoz por la idea de la posibilidad de producir una hemorragia en el RN por transferir sangre a la madre mediante vasos comunicantes, o un aumento en los niveles séricos de bilirrubina que precisen ingreso del RN para fototerapia. Actualmente estas ideas están desterradas (flujo sanguíneo arterias umbilicales durante 20-25 s. tras el nacimiento. A los 40-45 s. flujo insignificante. Flujo vena umbilical 3´, después insignificante) e incluso conocemos inconvenientes asociados a un pinzamiento precoz, tales como:
- Mayor dificultad respiratoria, anemia e hipovolemia.
- En los casos de circular de cordón, puede provocar hipovolemia y anemia.
Tardío
Ventajas del pinzamiento tardío:
- Permite la transfusión de un volumen de sangre al recién nacido de
hasta 20-35 mL/kg de peso fetal. Aunque se ha detectado un aumento de
policitemia en algunos lactantes en los que se retrasó el pinzamiento del
cordón al nacer, esta condición hematológica parece ser benigna.
- Los defensores del pinzamiento tardío argumentan que incrementa los depósitos de hierro en el recién nacido, disminuyendo el riesgo de anemia por déficit de hierro durante el primer año de vida o los 4-6 primeros meses de vida.
- La tasa de transfusión placentaria está influida por la posición del bebé. Parece que la posición idónea sería 10 cm por encima o por debajo del nivel de la placenta. Cuando el recién nacido se encuentra a 50-60 cm por encima de la placenta, no recibe sangre de ésta; en cambio, mantener al niño 40 cm por debajo de la placenta aumenta y acelera la transfusión placentaria en el plazo de 1 minuto.
- Varios estudios concluyen que el retraso del pinzamiento del cordón durante al menos 30 segundos es seguro, no compromete al recién nacido prematuro en la adaptación inicial posparto, y puede adoptarse como práctica habitual. Como efectos beneficiosos, se mencionan la mejora de la oxigenación cerebral en las primeras 24 horas y la mayor estabilidad vascular, la menor necesidad de transfusión y la menor incidencia de hemorragias intraventriculares, así como de sepsis de aparición tardía.
- Previene la incidencia de encefalopatía isquémica y el retraso mental.
- Algunos autores recomiendan retrasar el pinzamiento para que la sangre oxigenada tenga oportunidad de regresar al recién nacido y realizar la reanimación con cordón intacto.
- Inconvenientes del pinzamiento tardío:
- Algunos autores postulan que puede aumentar la morbilidad neonatal por un volumen sanguíneo excesivo, policitemia e hiperbilirrubinemia con ictericia sintomática.
- Otras investigaciones relacionan el pinzamiento tardío con cambios hemodinámicos y respiratorios en el recién nacido, pero sin evidencia que muestre que estos cambios elevan la morbilidad neonatal. El volumen sanguíneo neonatal aumentado por la transfusión sanguínea parece que es bien tolerado y compensado por el mismo.
- El pinzamiento tardío está contraindicado en los casos de crecimiento intrauterino retardado, porque existe riesgo de policitemia inducida por la hipoxia.
- Reduce los valores del pH de la arteria umbilical.
Con lo que, como medida general, debemos fomentar el pinzamiento tardío de cordón, siempre que no exista una contraindicación expresa para ello.
b. Cuidados del cordón umbilical
El cordón umbilical representa tras el nacimiento una vía de riesgo de colonización e infección para el RN, no sólo en el momento mismo del pinzamiento y de la sección del cordón, sino posteriormente hasta su caída y cicatrización final. Es prioritario, por lo tanto, la sección de este con material estéril y la colocación de un sistema seguro de cierre, igualmente en condiciones de esterilidad para prevenir el riesgo de hemorragia.
Clásicamente se ha usado para el cuidado inmediato y a domicilio; del cordón umbilical se han utilizado productos específicos tales como alcohol 70º, Clorhexidina 4 % o antibióticos, pero actualmente se recomienda cubrir el cordón con una gasa limpia o incluso sin cubrir, excepto en caso de evidencia de problemas de salubridad en el hogar, en cuyo caso usaremos Clorhexidina 4 %.

c. Vitamina K
El uso de vitamina K está justificado como medida preventiva de la denominada enfermedad hemorrágica del RN. Si bien es verdad, la expresión clásica o temprana de la misma (1ª semana de vida) no puede prevenirse con la administración de vitamina K, sí podemos incidir en la expresión de su versión tardía (> 2 semanas).
Debemos conocer los factores de riesgo de la enfermedad hemorrágica neonatal:
- Lactancia materna exclusiva (fórmulas artificiales con vit K incorporada, no sería preciso prof Vit K).
- No profilaxis con vit K.
En caso de que los padres no deseen la administración de vitamina K vía IM, ofreceremos la alternativa de administración oral, siempre siguiendo los protocolos del servicio, debemos saber que la administración IM otorga mayor protección que vía oral, y esta última siempre será mejor opción que la no administración del producto. Existe reticencia a la administración IM de la vitamina K, ya que ha habido intentos de relacionarla con la aparición de tumores, aunque ya ha sido totalmente desterrada esa teoría.

d. Profilaxis oftalmia neonatal
La oftalmia neonatal se define como una conjutivitis con secreción durante las dos primeras semanas de vida, aunque habitualmente aparece entre 2-5 días después del nacimiento. De no darse un tratamiento adecuado, la progresión del proceso va desde una lesión corneal, ulceración, perforación, panoftalmitis, sinequia, y finalmente ceguera. Es por ello, que debemos informar a los padres de los beneficios y la indicación de dicha profilaxis, aunque es cierto que no existe consenso de en qué momento debemos aplicar el colirio o pomada antibiótica, lo que está claro es que no debe interferir en el C.P.P. ni con la lactancia materna.
e. Baño del RN
Parece razonable postponer el baño del RN hasta que estabilice la Tª. Limpiar el exceso de vérmix y restos de LA con suavidad. Actualmente no se recomienda el baño inmediatamente tras el nacimiento.
f. Medición de gases en sangre arterial de cordón umbilical ph fetal
La determinación de gases arteriales en sangre del cordón es de utilidad no solo diagnóstica, sino pronóstica en situaciones de compromiso de la oxigenación y perfusión fetal intraútero. Su determinación es recomendable en partos de alto riesgo, pero también puede ser de ayuda en situaciones en las que el riesgo fetal es bajo. La normalidad de los gases en sangre del cordón de los RN vigorosos, junto con otros datos clínicos, confirma la ausencia de episodios hipóxico-isquémicos.
Durante las dos últimas décadas, la valoración del Apgar había sido considerado como un reflejo de asfixia perinatal y predictor de secuelas neurológicas, pero en la actualidad los mejores métodos para evaluar la estabilidad fetal y el riesgo fetal de asfixia, ha sido a través de estudios clínicos y de la medición de indicadores bioquímicos tales como pH de arteria umbilical.
El análisis de sangre de cordón umbilical se recomienda tomar en todos los RN, haya sido parto normal o no, se obtiene en pacientes con partos de alto y bajo riesgo para hipoxia o asfixia fetal, así como cuando ocurre depresión del recién nacido.
Esta práctica puede ser importante ya que tiene repercusiones legales. El resultado y el manejo clínico puede ayudar a excluir el diagnostico de asfixia al nacimiento.
El parámetro más utilizado es el pH arterial ya que este es más representativo de la condición metabólica fetal.
Los estudios de gases de cordón umbilical sirven para valorar el estado metabólico del feto en los minutos y escasas horas previos al parto.
Los valores normales establecidos por el colegio americano de ginecología y obstetricia en R. N. a término son:
- Sangre arterial pH: 7,25 rango inferior 7.10. Acidemia fetal patológica relacionada con un aumento del riego de lesión neurológica pH por debajo de 7.
- Sangre venosa pH: 7,34 rango inferior 7,20.
Existen muchos factores intraparto que pueden modificar el pH y no es raro que recién nacidos sanos presenten datos de acidez.
Se recomienda el doble pinzamiento del cordón, la separación de un segmento del mismo tras el nacimiento, que se coloca en la mesa y se emplea para determinar los gases en caso de que cualquier anomalía importante del proceso del parto, o la persistencia de problemas en la situación del neonato, más allá de los primeros cinco minutos de vida lo hagan recomendable.
El proceso de embarazo, parto y puerperio de la Junta de Andalucía recomienda estudiar el pH en la sangre fetal tras el nacimiento.
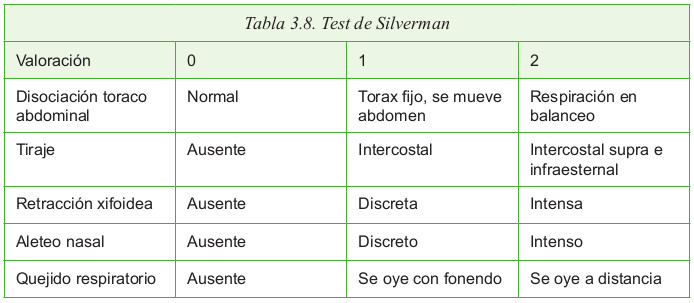
g. Test de Silverman-Andersen
El test de Silverman se utiliza desde hace más de 40 años para valorar la dificultad respiratoria. Se le realiza a neonatos que presentan algún tipo de dificultad en la respiración, ya que suele ser normal en los que no tienen dificultades.
Valora 5 parámetros:
- Disociación tóraco abdominal
- Tiraje costal
- Retracción xifoidea
- Aleteo nasal
- Quejido espiratorio
Retracciones de la pared torácica: como la pared torácica del neonato es muy distensible (gran complianza), en pacientes con enfermedades que disminuyan esta distensibilidad, (enfermedad de la membrana hialina, edema pulmonar, bronconeumonía) o aumento de la resistencia de la vía aérea (aspiración de meconio, obstrucción por tapón de moco, broncoespasmo) la mayor presión pleural negativa, que ha de generarse por el diafragma y otros músculos de la respiración para lograr un volumen corriente aceptable, “succiona” las estructuras de la pared ocasionando su retracción (intercostal, supraclavicular, subcostal, xifoidea, supraesternal), que será más intensa cuanto menos distensibles sean los pulmones o más ocluida esté la vía aérea.
Aleteo nasal: la dilatación de los orificios nasales durante la inspiración, por la activación del músculo de las alas de la nariz, conduce a una disminución de la resistencia nasal al flujo aéreo, y por consiguiente, a una disminución importante del trabajo respiratorio, especialmente en los recién nacidos, que respiran preferentemente por la vía nasal. El aleteo nasal, es un “intento” para disminuir la resistencia de la vía aérea, puede ser intermitente, a veces muy obvio y otras veces apenas perceptible. En ocasiones, se observa en ausencia de otros signos de dificultad respiratoria, como por ejemplo, durante la alimentación.
Quejido espiratorio: es el sonido producido durante la salida del aire del final de la espiración hacia el exterior, a través de unas cuerdas vocales parcialmente cerradas. Es un mecanismo de adaptación o compensación, para lograr mejorar el cociente ventilación/perfusión, y así el intercambio gaseoso, debido al aumento de presión en la vía aérea y de la capacidad residual funcional.
El test de Silverman puntúa cada parámetro de 0 a 2 puntos, de manera que la puntuación global oscilará entre 0 y 10 puntos.
Es inverso al Test de Apgar, por lo que la mejor puntuación será 0 puntos indicando que la respiración está correcta y no existe dificultad.
Las conclusiones son:
- 1-2 puntos → situación normal o leve dificultad respiratoria.
- 3-5 puntos → dificultad respiratoria moderada
- 5 puntos → dificultad respiratoria grave
Los signos de dificultad respiratoria deben vigilarse con frecuencia en las primeras 6 horas de vida, período en el cual pueden debutar la mayoría de enfermedades graves pulmonares. En los primeros 30 minutos de vida, se acepta como normal la presencia de aleteo nasal, polipnea, quejido y pequeñas retracciones de la pared costal. Cuando estos signos son importantes o persisten pasadas las primeras horas de vida, es obligada la vigilancia muy estrecha y la realización de exploraciones complementarias, ya que puede existir patología cardiopulmonar.
D. Reanimación neonatal: niveles
Vamos a analizar este apartado desde un punto de vista práctico, esto es, los pasos que seguiríamos en la recepción y asistencia del RN.
a. Análisis de la situación
Debemos conocer los antecedentes y factores de riesgo en la asistencia del RN. Aquí la historia clínica y la anticipación cobra un papel fundamental.
Clásicamente debíamos responder a una batería de preguntas para situarnos en el contexto de la asistencia neonatal: edad gestacional, tono, respiración, características del líquido amniótico, frecuencia cardiaca… Ahora hacemos una modificación en la anamnesis y debemos contestar a las siguientes preguntas:
- ¿RN a término?
- ¿Llora?
- ¿Tiene buen tono?
b. Actuación
Si alguna de las respuestas es “NO”, procederemos a la valoración del RN en la cuna de reanimación para planificar la actuación en base a la valoración del RN.
Actuación sobre el RN: si atendemos a un RN en la cuna térmica, debemos realizar una primera valoración en la cuna de reanimación.
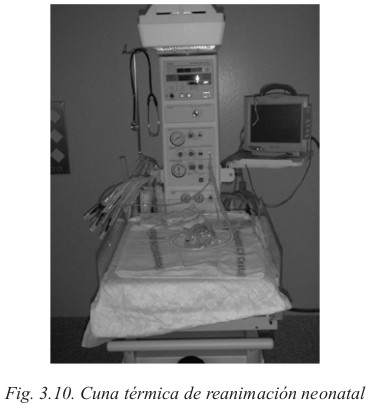
Durante 30 segundos estabilizaremos al RN secándolo, colocándolo bajo una fuente de calor y consiguiendo una posición neutra de la cabeza, ni flexionada, ni hiperextendida, para favorecer la ventilación espontánea.
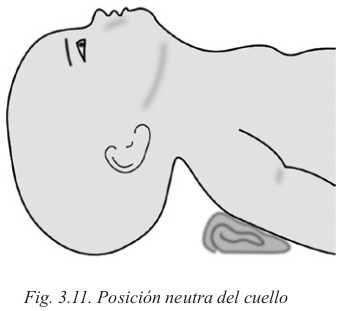
Pasados esos 30 primeros segundos de evaluación, procedemos a valorar FR y FC; si la respiración es ineficaz y/o la FC es < 100 ppm, procederemos a ventilación con presión espiratoria positiva (teniendo especial cuidado en la colocación de la cabeza del RN, así como de la mascarilla, que debe tener el tamaño correcto, no debe apoyarse en los ojos y no debe sobrepasar el mentón, permitiendo el sellado total de la boca y la nariz) durante otros 30 segundos, momento en el que reevaluaremos al RN.
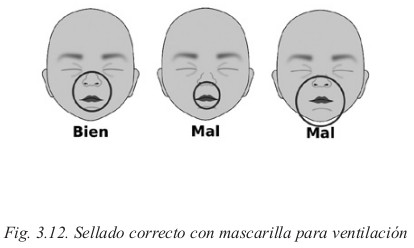
Si tras la evaluación del primer minuto (APGAR del primer minuto en este momento) nos encontramos con un RN con una respiración ineficaz y/o FC< 100 ppm, volveremos a ventilar durante otros 30 segundos, pero si nos encontramos con un RN con la FC< 60 ppm, iniciaremos el masaje cardiaco (colocar los pulgares, uno al lado del otro en caso de recién nacido a término o uno encima del otro, si es pretérmino, sobre el tercio inferior del esternón, por debajo de la línea intermamilar, y el resto de los dedos abrazando el tórax. Otra forma consiste en comprimir en el mismo punto con dos dedos colocados perpendicularmente al esternón. Esta técnica puede ser más útil en caso de un solo reanimador. La profundidad de la compresión debe ser 1/3 del diámetro antero-posterior del tórax) además de las ventilaciones con PEP (relación 3/1 compresión/ventilación).
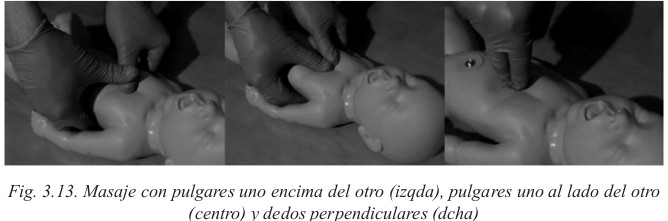
Llegamos al 1er minuto y 30 segundos… valoramos respiración y FC, si la respiración es ineficaz mantendremos la ventilación con PEP (valorar necesidad de intubación), pero si nos encontramos con un RN con FC < 60 lpm deberemos asociar a la ventilación y el masaje, el uso de adrenalina (0,01-0,03 mg/kg IV, 0,03-0,1 mg/kg ET).

No debemos olvidar la reevaluación de la ventilación; tanto en el posicionamiento del neonato, como en el correcto uso del material (colocación de la mascarilla) así como en la existencia de elementos obstructivos de la vía aérea (fundamentalmente tapones de moco), esto lo haremos en cada valoración que realizamos al RN durante la reanimación.

c. Situaciones especiales en la reanimación neonatal
- LA meconial: clásicamente se realizaba aspiración de secreciones a la salida de la cabeza del RN con LA teñido, y se procedía a la aspiración sistemática y enérgica de las secreciones, independientemente del estado inicial del RN. Actualmente, sólo se contempla la aspiración de secreciones en caso de encontrarnos con un RN deprimido, hipotónico, no inicia la respiración o ésta es ineficaz estando indicada la aspiración de tráquea de las secreciones con ayuda del laringoscopio. Si no cumple esos requisitos, procederemos a la valoración habitual del RN en contacto piel con piel con su madre.
- RN prematuro: es otro caso especial en las medidas a tomar, debemos diferenciar además si se trata de un RN ≤ 28 semanas, o > 29 semanas de gestación.
- Hernia diafragmática: se debe intubar inmediatamente evitando los estímulos que favorecen el inicio de la respiración. Además, se debe colocar una sonda gástrica antes de proceder al traslado.
Características anatómicas y fisiológicas del recién nacido. Regulación térmica. Aparatos: respiratorio, circulatorio, digestivo y urinario. Importancia de la valoración neurológica: reflejos, tono muscular y aspectos sensoriales
A. Características anatómicas y fisiológicas del recién nacido
Este punto lo hemos analizado en el tema 2.3, apartados B y C
B. Regulación térmica
El RN debe considerarse como un individuo que tiende a la pérdida de calor, tanto por sus características anatómicas como por los factores ambientales al nacimiento.
Podemos resumir los siguientes factores:
- Gran superficie corporal en relación con el peso.
- Escaso tejido adiposo.
- Piel fina.
- Vasos sanguíneos próximos a la superficie de la piel.
- La piel del RN está húmeda al nacimiento.
- La temperatura ambiente es mucho más fría que la intrauterina (por eso debemos preparar la habitación para el nacimiento).
a. Existen cuatro mecanismos de pérdida de calor en el RN
- Conducción: cesión de calor de un objeto + caliente a otro + frío cuando entran en contacto. 3 % pérdida de calor.
- Evaporación: conversión de líquido a gas, a través de la respiración y piel. 25 % pérdida de calor.
- Convección: por un gradiente de Tª entre la superficie corporal y el aire ambiente. 11 % pérdida de calor.
- Radiación: comunicación de calor entre dos cuerpos que no están en contacto. 60 % de la pérdida calor.
Por todo ello, nuestra primera prioridad para salvaguardar la temperatura del RN será la preparación de la zona de nacimiento.
b. ¿Cómo afecta la disminución de la temperatura al RN?
Ante un episodio de hipotermia, el RN sufrirá una vaso constricción, debemos recordar que el RN no es capaz de elevar su temperatura mediante el escalofrío.
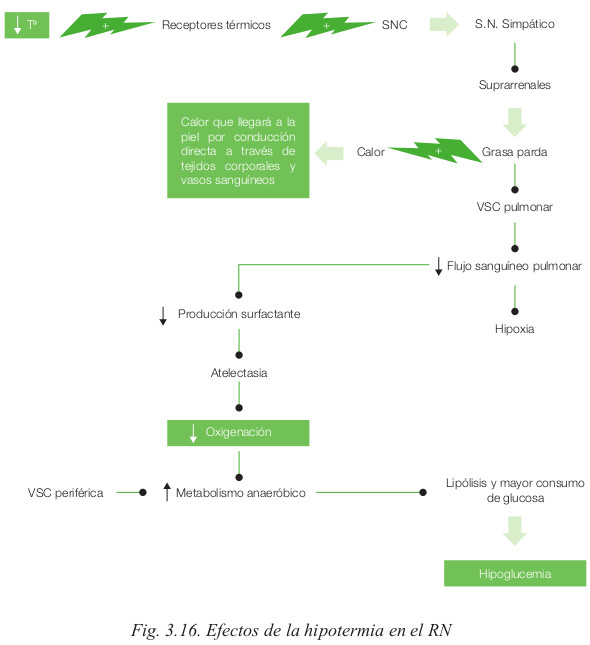
La grasa parda es un tejido adiposo exclusivo del RN que se usa fundamentalmente para compensar la disminución de la temperatura en el RN. Localizada alrededor de grandes vasos, riñones, cápsulas suprarrenales, axilas, nuca y entre las dos escápulas. Aparece en semana 26 y persiste hasta 3-5 semanas después del nacimiento.
El problema es que conseguir elevar la temperatura sin escalofrío (nula contracción muscular) y fundamentalmente por vía metabólica, generan un gasto elevado de O2 y glucosa, lo normal es que el RN consiga los requerimientos con la polipnea y el consumo de los depósitos de glucosa del hígado. El problema es que si se prolonga en el tiempo esta situación el RN llegará a la hipotermia e hipoglucemia.
c. ¿Qué ocurre en caso de hipertermia?
- VSD (vaso dilatación) para disipar el calor.
- La sudoración no es una opción (el RN tiene menor capacidad de sudoración que el adulto).
- Se consigue disminuir la temperatura por la respiración con la evaporación.
d. Cambios que suceden en la piel, tejido subcutáneo y graso
La piel del RN progresivamente consigue un pH de 5.5 gracias al efecto de bacterias, sudor, jabones, cremas, etc… hasta que se transforma en la barrera defensiva que todos conocemos. Este proceso tarda de 2 a 8 semanas tras el nacimiento.
El vérmix caseoso es una sustancia blanca, producida por las glándulas sebáceas, cubre la piel del feto desde la semana 34 y se reabsorbe gradualmente por la piel concentrándose en axilas o ingles en el RN a término. Tiene como misión proteger la piel del contacto con el LA para evitar su maceración intraútero.
El lanugo es un vello fino y suave que cubre el cuerpo del feto, aparece en la semana 16-18 y va desapareciendo al final de la gestación. Su localización es espalda, hombros y frente.
C. Aparato respiratorio
Como ya hemos hablado, en el momento del nacimiento es fundamental la correcta transición al medio aéreo. Existen una serie de mecanismos que desencadenan la primera respiración:
- Físicos: cambio de la temperatura al entrar en contacto con el aire. Los receptores térmicos, fundamentalmente de la cara y tórax, estimulan la respiración. Paradójicamente, un enfriamiento importante puede provocar una depresión respiratoria.
- Sensoriales: estímulos táctiles, olfatorios, auditivos, etc…
- Químicos: en el proceso del nacimiento se desarrolla un episodio momentáneo de asfixia aguda (↓ Pa O2, ↑ Pa CO2) que estimula los quimiorreceptores de la arteria aorta y carótidas→ estímulo del centro respiratorio.
- Mecánicos: el propio proceso de paso por el canal del parto y drenado de las secreciones (hasta un 30 % del total de las secreciones pulmonares) es un estímulo del inicio de las respiraciones.
Hemos visto los factores que ayudan a que se produzca la primera respiración, veamos ahora la fisiología de la misma: el diafragma genera una presión intratorácica negativa, descendiendo hasta generar 40-80 mm H2O (lo que justifica los neumotórax espontáneos en el 1 % de los RN). Ahora el aire penetra en los pulmones, distiende los alveolos (disminuyendo la tensión superficial de los mismos), y fuerza el drenado del fluido pulmonar (por medio de los capilares pulmonares y vasos linfáticos). Aparece la capacidad residual pulmonar. Gracias a todo ello, la respiración es ahora menos costosa para el RN.
Se produce una VSD a nivel capilar pulmonar, ↑Pa O2 a nivel alveolar, que junto con la bradikinina provoca la dilatación de las arterias pulmonares. Disminuyen las resistencias vasculares pulmonares (que estaban ↑ en la vida intrauterina) con lo que ↑ la vascularización y el aporte de sangre en los vasos pulmonares. El aumento del flujo sanguíneo pulmonar facilita el intercambio gaseoso.
La hipoxemia y acidosis mantenida provoca una VSC de las arterias pulmonares, lo que conlleva una hipoperfusión pulmonar y una situación de distrés respiratorio. Este cuadro es el que se produce en el momento del nacimiento cuando ha existido un proceso de asfixia intraútero y una ↓ pH fetal.
D. Aparato circulatorio
a. Hemoglobina fetal (Hb F)
La Hb F es la Hb más importante hasta la madurez fetal y en un recién nacido a término constituye el mayor porcentaje de su Hb. Posteriormente, va siendo remplazada por la Hb A (este proceso suele darse al final de la gestación).
Está constituida por 2 cadenas α y 2 cadenas γ (adulto 2 cadenas α y 2 cadenas β).
La Hb Fetal tiene ciertas características que la hacen diferente a la del adulto:
- Tiene mayor afinidad por el O2 que la Hb materna.
- Además, en condiciones normales la Hb fetal tiene una curva de disociación desviada hacia la izquierda con respecto a la del adulto, como podemos observar en la siguiente figura:
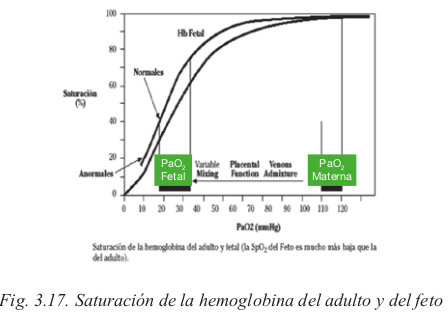
La desviación a la izquierda refleja que la liberación de O2 a los tejidos se produce a niveles más bajos de PO2 que en el adulto. Esto se debe a que el feto crece y se desarrolla en un ambiente relativamente hipóxico, pero con suficiente O2 como para cubrir sus necesidades.
El rango normal de la saturación arterial de O2 en el feto se encuentra entre el 30-70 %, zona que ocupa la mitad de la curva de disociación de la Hb F, por eso, pequeños cambios en el pH o en la PO2 causan grandes variaciones en la saturación de O2 de la Hb F.
b. Características particulares de la coagulación del RN
- ↓ Transitoria de la función plaquetaria.
- Déficit transitorio de los factores de coagulación (II, VII, IX, X, XI, XII) debido a la inmadurez hepática, con lo que las enzimas que los producen no lo hacen de forma adecuada.
- Déficit transitoria de vitamina K (síntesis mediada por la flora intestinal inexistente), precisa para la producción de alguno de los factores de coagulación.
E. Aparato digestivo
a. Existen una serie de hechos esenciales a tener en cuenta
- A las 26 semanas empieza el peristaltismo no organizado
- A las 32-34 semanas aparece la coordinación succión-deglución
- A las 36-38 semanas se completa la madurez de las vías gastrointestinales
Es fundamental alcanzar el control metabólico en el RN, esto se consigue entre otros, gracias a un aparato gastrointestinal maduro, cosa que suele ocurrir tras varias semanas después del nacimiento, lo que justifica que se produzcan alteraciones en el control de la glucosa, líquidos, electrolíticos y equilibrio ácido-base.
b. Características del RN
- La salivación es escasa.
- Puede producir lipasa lingual y amilasa, para poder iniciar la digestión de los ac. Grasos de la leche.
- El cardias es inmaduro e incompetente durante el primer mes de vida, por lo que el reflujo gastroesofágico es fisiológico y habitual.
- La lactasa es madura a las 36-40 semanas.
- La actividad enzimática proteínica aumenta rápidamente tras el nacimiento.
- El peristaltismo y la motilidad intestinal alcanza la madurez funcional en el tercer trimestre (por lo que no es común LA teñido en el segundo trimestre…).
El RN está preparado sólo para recibir alimentos líquidos. Está claro que la alimentación del RN será la que regula el crecimiento y la función de las vías gastrointestinales, la flora intestinal, los precesos metabólicos y los nutrientes incorporados al organismo dependen directamente de la dieta.
En la etapa fetal se produce un acúmulo de glucógeno en el hígado, de 2-10 veces más cantidad que en un adulto, ya que este glucógeno será el que seriva como reserva energética en el periodo de transición.
Gracias a esto un RN sano puede tolerar periodos de ayuno o mala alimentación, periodos típicos en el inicio de la lactancia materna hasta su instauración inicial. Esta fuente de glucógeno proporciona energía directamente al cerebro.
El meconio está compuesto por bilis y descamación de células intestinales, se produce durante la etapa fetal y se elimina en las primeras 24 horas.
F. Aparato urinario
El paso a la vida extrauterina hace que el flujo renal pase de un flujo disminuido por la alta resistencia vascular a nivel renal a un flujo optimizado tras el nacimiento, ya que disminuye la resistencia vascular renal.
Aunque el tejido nefronal es completo desde la semana 32-34, no se completa su maduración funcional durante la lactancia.
La formación de orina, que ayuda a la formación del LA, comienza en el primer trimestre del embarazo.
El eje renina-angiotensina-aldosterona funciona en el RN. El flujo plasmático renal aumenta progresivamente en las primeras semanas de vida. El flujo intrarrenal depende de los cambios en las resistencias vasculares, concretamente en la disminución de la resistencia vascular de los riñones que se da tras el nacimiento. La filtración glomerular se duplica en las primeras 2 semanas (20-40 ml/min/1,73 m2) y se triplica a los dos años de vida. El RN no es capaz de concentrar la orina como lo hará el adulto.
Respecto al equilibrio ácido-base, el RN tiene un déficit en su equilibrio, debido a:
- Menor capacidad para compensar los desequilibrios ac-base
- ↓ de la capacidad de reabsorción de bicarbonato, así que ↓ el pH
- ↓ filtrado glomerular
- Menor capacidad de extraer ác. orgánicos
Tras el pinzamiento de cordón, ↑ el volumen intravascular, eso dará lugar a un aumento del volumen extracelular, eliminado con la micción de la primera semana de vida. Echo por el cual se produce la pérdida fisiológica de peso respecto al nacimiento (5-10 % de pérdida de peso); esa excreción de líquidos será por vía renal y extrarrenal, principalmente pérdidas insensibles (10-15 ml/kg/día) que serán más importantes en el primer día y vías respiratorias.
G. Cambios hormonales e inmunitarios
a. Cambios hormonales
TSH, T3, T4: el RN sufre un ↑TSH debido al enfriamiento al nacimiento (este hipertiroidismo fisiológico es necesario para contrarrestar la hipotermia mediante la metabolización de la grasa parda). El pico máximo se da a los 30 minutos y ↓en los días siguientes.
↑TSH → ↑T3, ↑T4, pico máximo 36-48 h de vida, durante 4-5 semanas.
Los valores de las hormonas tiroideas están en relación con la edad gestacional y el peso.
Los andrógenos ↑al nacimiento y se normalizan en los primeros días, tras el nacimiento se produce una ↓de estrógenos, lo que puede provocar en las niñas un sangrado vaginal en los primeros días de vida.
Por último analizaremos el cortisol, hormona cortico suprarrenal que interviene en el control de la glucosa, desarrollo, crecimiento, reacciones inflamatorias, función cardiovascular y reacciones al estrés.
En el RN a término, las glándulas suprarrenales son 2 veces mayor que en el adulto; en el feto el cortisol proviene tanto de la glándula suprarrenal como de la placenta.
Los niveles de cortisol ↑durante la gestación, están en relación con el inicio del trabajo de parto así como:
- Maduración enzimas intestinales
- Mayor metabolismo T3 y T4
- Maduración del agente tensioactivo pulmonar
- Mayor conversión de noradrenalina en adrenalina
- Estimulación de enzimas hepáticas que regulan la glucosa
- Incremento receptores β adrenérgicos en pulmón, corazón y tejido adiposo
- Los niveles de cortisol plasmático están ↑al nacimiento y ↓en los primeros días de vida
b. Cambios inmunitarios
El timo tiene un gran tamaño al nacimiento y disminuye a partir del 2º día de nacimiento de forma progresiva.
IgG:
- Pasan de la madre al feto a través de la placenta
- Ofrece inmunidad al RN
IgM:
- No atraviesan la placenta
- Aumenta rápidamente tras el nacimiento
- Se pueden detectar niveles ↑IgM en caso de infecciones fetales
IgA:
- No atraviesa la placenta
- En el RN presenta niveles ↓hasta 2ª, 3ª sem de vida
- Común en las vías gastrointestinales, respiratorias, calostro y leche materna
IgE:
- Escasos niveles en feto y RN, relacionado con reacciones alérgicas
H. Valoración del estado neurológico
El examen neurológico valora la integridad del sistema nervioso neonatal. Debe comenzar con un periodo de observación, notando las características físicas generales y el comportamiento del recién nacido. Los comportamientos que es importante observar son el estado de alerta, la postura de reposo, el llanto y la calidad del tono muscular y la actividad motora. Todo esto se valora con la valoración de los reflejos arcaicos.
La postura usual del recién nacido es con las extremidades en flexión parcial, con las piernas abducidas hacia el abdomen. Si está despierto el neonato puede realizar movimientos bilaterales sin coordinación con las extremidades; si no existen éstos, se debe sospechar disfunción neurológica mínima y asimétrica. Pueden observarse movimientos oculares durante los primeros días de vida; el neonato alerta puede fijar cara y objetos brillantes, su respuesta será de parpadeo al ponérselo frente a los ojos. El llanto debe ser fuerte y vigoroso; los llantos agudos, débiles o la ausencia de éstos son causas de preocupación.
El tono muscular se valora con la cabeza en posición neutral, conforme se mueven en forma pasiva varias partes del cuerpo. El recién nacido es un poco hipertónico, es decir, existe resistencia a la extensión del codo y las rodillas. El tono muscular debe ser simétrico, una disminución del mismo y flaccidez necesitan una valoración más profunda.
En el recién nacido a termino pueden existir temblores y hay que distinguirlos de las convulsiones. Los temblores se pueden relacionar con hipoglucemia o hipocalcemia y las convulsiones neonatales pueden consistir nada más que en movimientos de masticación o deglución, desviaciones de los ojos, rigidez o flaccidez, por la inmadurez del sistema nervioso central.
También deben observarse signos de disfunción neurológica como llanto débil, actividad disminuida, alteración de la vigilia, convulsiones y perímetro craneal anormal. A los tres meses, debe examinarse el retraso de las adquisiciones psicoafectivas como la sonrisa, incoordinación oculomotriz, incapacidad para mantener la cabeza erguida o alteraciones vasomotoras como palidez, amoratamiento, irritabilidad e hipertonía.
a. Estados de sueño-vigilia según Prechtl
- Estado 1: ojos cerrados, respiración regular, sin movimientos.
- Estado 2: ojos cerrados, respiración irregular, algunos pequeños movimientos.
- Estado 3: ojos abiertos, movimientos poco amplios.
- Estado 4: ojos abiertos, movimientos amplios, sin llorar.
- Estado 5: ojos abiertos o cerrados, llorando.
b. Exploración de reflejos
Los reflejos son una respuesta motriz involuntaria que se manifiesta de forma inmediata tras la aplicación de un estimulo sobre un receptor especifico. El sistema nervioso del recién nacido tiene, en el nacimiento, todas las células nerviosas de la edad adulta aunque en los primeros años de vida su tamaño aumenta y se mielinizan. El cerebro es todavía inmaduro. Se calcula que existen entre 15- 20 neuronas en el momento de nacer. El último trimestre del embarazo es un periodo de rápida maduración del sistema nervioso central, lo que va acompañado por un aumento de la complejidad y la capacidad de la función neurológica. Las reacciones especiales del recién nacido tienen como finalidad concreta la alimentación (succión y búsqueda), defensa (extensión cruzada, flexión de la pierna) o locomoción (arrastre y marcha), pero también puede ser una respuesta a un estimulo propio (abrazo del moro, tónico del cuello, prensión y enderezamiento).
El examen neurológico tiene como finalidad valorar la normalidad y detectar las anomalías.
- Reflejo de Moro o reflejo de los brazos en cruz. Se valora colocando al bebé en una superficie dura, semisentado y con el tronco y la cabeza caídos hacia atrás. Consta de tres movimientos, extensión abducción de los brazos (Fig. 3.18), abertura de manos y llanto. Seguidamente se efectuará un movimiento de aproximación parecido a un abrazo. Se valora la rapidez y la amplitud de la respuesta, así como la capacidad de aprendizaje después de repetirlo varias veces. Según algunos autores se manifiesta en las extremidades inferiores como Moro inferior o signo de aplauso podálico. La respuesta está presente al nacimiento, la reacción completa puede observarse hacia las ocho semanas de edad y el salto del cuerpo sólo se observa entre las 8 y las 18 semanas: la respuesta está ausente hacia los 6 meses si no hay retraso en la madurez neurológica; la 386respuesta puede ser incompleta si el bebé esta profundamente dormido. Oriente a los padres sobre la respuesta normal. Una respuesta asimétrica puede significar lesión del plexo braquial, las clavículas o el húmero. Una respuesta que persiste más allá del 6º mes indica un posible daño cerebral.

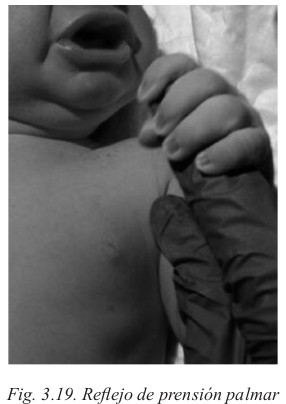
- Reflejo de Prensión Palmar. Se examina la intensidad con que agarra un objeto, la simetría de los miembros superiores y la persistencia de la prensión. Se observa introduciendo un dedo o un pequeño objeto en la palma de la mano del niño; el pequeño flexiona los dedos y lo agarra fuertemente (Fig. 3.19). Desaparece entre el tercer y cuarto mes de vida.
- Reflejo de Babinski. Se determina sobre la planta del pie. La mano se desplaza a lo largo de la cara lateral de la planta, comienza por el talón hacia los metatarsianos y moviendo los dedos a lo ancho del pie. La respuesta normal del recién nacido será la hiperextenxión del dedo gordo y la separación del resto de los dedos. La ausencia requiere una valoración neurológica. Desaparece en los primeros meses de vida, máximo primer año.
- Reflejo tónico cervical (llamado por otros autores reflejo tónico del cuello de Magnus-Klein). También llamada por otros autores Posición de Esgrimista. Éste se analiza con el neonato decúbito supino. Al girar la cabeza hacia el lado izquierdo, el brazo y la pierna de ese lado se extienden y el brazo y la pierna del lado opuesto se flexionan. Desaparece a los tres o cuatro meses. La presencia de este signo puede alertar sobre una afección del sistema nervioso central; aunque puede no observarse durante el periodo neonatal temprano. Las respuestas de las piernas son más constantes. La respuesta completa desaparece hacia el tercer o cuarto mes; la incompleta puede observarse hacia el tercer o cuarto año. Después de las seis semanas una respuesta persistente es un signo de una posible parálisis cerebral.
- Reflejo de succión. El neonato tiene muy desarrollado este reflejo. Se examina introduciendo en la boca algún objeto, que puede ser el pezón, el chupe o el dedo del explorador (Fig. 3.20). Está presente en los primeros años de vida. La disminución de este reflejo puede ser la causa de numerosas alteraciones, entre ellas la prematuridad, una patología prenatal o bien trastornos neurológicos. La respuesta es difícil, si no imposible, de suscitar después de que el niño ha sido alimentado; si la respuesta es débil o no se da, considere prematuridad o un defecto neurológico. Orientación a los padres: evite girar la cabeza hacia el pecho o el pezón, permita que el bebé los busque; la respuesta desaparece del tercero al cuarto mes pero puede persistir hasta el año.

- Reflejo de los puntos cardinales (de A.Thomas o de búsqueda de Peiper, según algunos autores). Éste se observa estimulando las comisuras y los labios. El recién nacido gira la cabeza orientándola hacia la dirección en que está siendo estimulado.
- Reflejo nauseoso del neonato. Este reflejo se practica en la sala de partos, mediante la introducción de una sonda nasogástrica y se registra como puntuación de Apgar. Debe reaccionar a la introducción de cualquier objeto en las fosas nasales.
- Reflejo de danza. Este reflejo también es una evaluación sistemática. El examinador sujeta al bebé de modo que los pies descansen en una superficie dura para que extienda y flexione las piernas, semejando el caminar. Desaparece 1º y 3º mes.
- Reflejo de gateo. Debe examinarse colocando al bebé sobre el abdomen. Hace movimientos de gateo con las piernas y con las manos, como si estuviera rodando. Desaparece en los primeros meses de vida. Por otros autores llamado reflejo de arrastre.
- Reflejo de la marcha automática. Se analiza en todos los recién nacidos. El examinador lo sostiene por las axilas y, tras su enderezamiento, inicia unos cuantos pasos al ser llevado hacia delante. Desaparece a los tres o cuatro meses, para ser reemplazado por un movimiento involuntario.
- Reflejo de imán. Se examina en los primeros días de vida y consiste en colocar al bebe en decúbito supino, flexionando parcialmente las extremidades inferiores. Se aplica una presión en la planta de los pies, próxima a los dedos, éstos se flexionan y las extremidades se extienden. La ausencia de este reflejo sugiere una patología neonatal, daño en la médula espinal o malformaciones. Este reflejo puede estar abolido o exagerado en el caso de partos de nalgas, puede indicar un síndrome de estiramiento del nervio ciático.
- Reflejo de deglución. Presente a partir de las 33 o 34 semanas de gestación. Una respuesta débil o ausente puede indicar prematuridad o un déficit neurológico. La succión y la deglución a menudo están descoordinadas en el bebé prematuro.
- Respuesta de retirada. Consiste en la flexión de la pierna o giro de la cabeza, huyendo del estimulo molesto aplicado a la planta del pie o lóbulo auricular.
- Reflejo de incurvación del tronco (Galán). Al friccionar la región paravertebral de arriba abajo, el raquis se incurva con concavidad hacia el lado estimulado. La respuesta desaparece hacia la cuarta semana. En las lesiones transversas de la médula espinal no hay respuesta por debajo del nivel de la lesión. La respuesta puede variar, pero debe obtenerse en todos los bebés, incluidos los prematuros.
- Reflejo extensor cruzado. Si el neonato tiene una pierna extendida y otra flexionada, al presionar sobre la planta del pie del lado extendido, la pierna flexionada se extiende y aproxima hasta llegar a cruzar la línea media. Este reflejo debe estar presnte durante el período neonatal. La ausencia sugiere una lesión de la médula espinal; una respuesta débil sugiere daño en un nervio periférico.
- Reflejo del paso del brazo. En decúbito prono con la cara contra la cama, el lactante gira la cabeza a un lado y va desplazando la extremidad superior del lado del rostro hasta colocarla junto a su boca, llegando a introducir la mano en la boca para succionar.
- Reflejo Glabelar. Golpee levemente la frente, el puente de la nariz o el maxilar del neonato cuando tiene los ojos abiertos. El RN parpadea en los cuatro primeros golpes. Un parpadeo continuo con los golpecitos repetidos se corresponde con un trastorno extrapiramidal.
- Reflejo cocleopalpebral. Haga un aplauso fuerte con las manos, se suscita mejor si el RN tiene más de 24-36 horas de vida. Los brazos se abducen con flexión de los codos, las manos permanecen cerradas. La respuesta debe desaparecer hacia el cuarto mes de edad. La respuesta se suscita más fácilmente en el bebé prematuro. Informar a los padres sobre esa característica.
Atención al recién nacido. Cuidados generales: higiene, temperatura, cuidados del cordón umbilical. Importancia de las medidas de asepsia en el recién nacido. Historia del recién nacido. Exploración física. Control de signos vitales. Técnicas somatométricas. Interacción madre-hijo y vínculo de relación madre/pareja
A. Atención al recién nacido. Cuidados generales: higiene, temperatura, cuidados del cordón umbilical
Desarrollado en el tema 3.3 apartados B y C.
B. Importancia de las medidas de asepsia en el RN
Las medidas de asepsia en la sala de partos se centran en los cuidados del cordón umbilical, principalmente en el momento de su sección, que siempre debe ser con material estéril, así como su clampado, para evitar riesgos de infección neonatal; hay que recordar que la onfalitis es una complicación severa en el neonato debido a su inmunodepresión.
Igualmente hay que tener en cuenta el uso de guantes por personal sanitario para cualquier tipo de manipulación al RN.
C. Historia del RN
La asistencia adecuada al RN pasa por la anticipación de los posibles problemas que pueda presentar, por lo que la correcta identificación de los factores de riesgo a través de la historia clínica es fundamental.
En la historia clínica debe hacerse constar los antecedentes familiares y maternos, así como cualquier incidencia relevante durante la gestación. Edad gestacional, serologías, cultivos vaginales y toda información que nos pueda ayudar a prepararnos para cualquier eventualidad en la asistencia inmediata o tardía del RN.
En la historia clínica debemos hacer constar horas de bolsa rota, así como las características del líquido amniótico. Hacer constar si ha existido fiebre o cualquier otro factor de riesgo infeccioso. Tipo de analgesia, sedación o anestesia durante el parto. Tipo de parto (eutócico, instrumental, cesárea), características de la monitorización fetal intraparto, así como descripción de la placenta y el cordón.
Debemos anotar además las características de la reanimación neonatal, APGAR y somatometría (peso, talla, perímetro cefálico).
Hacer constar cualquier hallazgo de interés respecto a las características del neonato (anatómicas o adaptativas) Tª, frecuencia cardiaca, frecuencia respiratoria y procedimientos rutinarios en la asistencia neonatal (vacunación hepatitis B, toma de gases de cordón umbilical, profilaxis antihemorrágica, profilaxis ocular, etc…).
D. Exploración física. Control de signos vitales
La exploración física del RN se ha desarrollado en el tema 3.2 apartado C
La valoración de signos vitales del RN se centra en
- Frecuencia cardiaca: 120-160 lpm, tomada con fonendoscopio.
- Frecuencia respiratoria: 40-60 rpm.
- Temperatura (axilar): en torno a 37 ºC.
Conviene tener en cuenta que durante los primeros 15 minutos de vida, los recién nacidos pueden presentar una frecuencia cardiaca de hasta 180 lat/min y una frecuencia respiratoria de hasta 80 resp/min producto de la descarga adrenérgica del periodo del parto, sin que ello sea patológico. Además, hay que saber reconocer la respiración periódica (ritmo regular durante 1minuto con periodo de ausencia de respiración de 5-10 segundos) que presentan algunos RN a término y que está dentro de la normalidad.
No es preciso en un recién nacido tomar la tensión arterial, determinar el hematocrito o la glucemia, si no presenta alteraciones de las variables anteriores, no es macrosómico o tiene un peso inferior a 2500 g, o si no es hijo de madre diabética y tiene buen color y perfusión.
E. Técnicas somatométricas
Al nacimiento, como técnica habitual se procederá a la determinación del peso, talla y perímetro cefálico del RN para tener esos datos como base de seguimientos posteriores, así como cribado inicial de malformaciones neonatales.
- Peso: previo calibrado del aparato, depositamos el RN sin ropa y sin pañal en la báscula, haciendo especial hincapié en los cuidados en la prevención de caídas por tratarse el neonato de un paciente de riesgo. Anotaremos en la historia el peso del nacimiento que servirá como punto de partida para el control del desarrollo posterior, así como para la valoración de la alimentación en las primeras semanas.
- Talla: con una cinta métrica, mediremos desde el occipucio hasta el talón, teniendo especial cuidado en adaptarnos al contorno del RN, ya que tiende a la flexión de sus miembros.
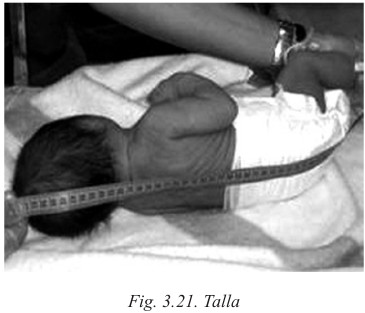
- Perímetro cefálico: con una cinta métrica mediremos la circunferencia del cráneo justo por encima de las orejas y de las cejas. Esto nos servirá para poder identificar problemas de aumento de volumen craneal en los primeros días tras el nacimiento.
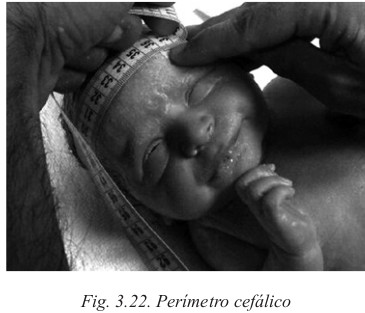
- Perímetro torácico: aunque no es rutinaria su determinación, puede ser protocolo de cada servicio; con una cinta métrica, medimos el contorno del tórax a través de una línea imaginaria que une los dos pezones y pasa por debajo de las axilas.
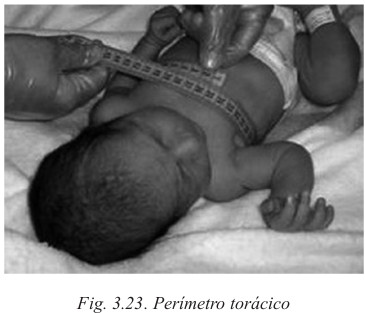
F. Interacción madre-hijo y vínculo de relación madre-pareja
Actualmente se intenta preservar el contacto piel con piel (CPP) entre madre-hijo desde el nacimiento. Para realizar este tipo de cuidados debe existir como premisa fundamental el deseo materno, así que nuestro papel de información y resolución de dudas aquí se hace fundamental. Además, debe existir un consenso en los RN que se puedan beneficiar de este CPP: con lo que debemos tener presente que al realizar este tipo de vínculo inicial no significa que nuestra actuación disminuya en intensidad, más bien todo lo contrario. Debemos identificar aquellos RN que se beneficiarían de una vigilancia más intensiva por parte de personal especializado. Debemos pensar que en pocos minutos tendremos que anticiparnos a unas posibles complicaciones que tendrían nefastos resultados. Existen varios estudios en los que se analizan los llamados “eventos aparentemente letales asociados al CPP”, que no son más que la expresión en grado máximo de una desadaptación al medio o de complicaciones arrastradas desde el parto, que se manifiestan en el contexto del CPP y que no llegaron a la muerte neonatal gracias a la rápida actuación de los padres y profesionales. Con todo ello, y partiendo de los incuestionables beneficios del CPP, suficientemente contrastados en la literatura científica (sincronía térmica, Nills Bergman, lactancia materna, involución uterina…).
No podemos terminar esta introducción sin hacer hincapié en la necesidad de una vigilancia continua del RN en el CPP tanto por parte de los profesionales, como y muy importante, por parte de los padres, a quienes deberemos informar y asesorar en la identificación de signos de alerta en el RN.
Otro punto fundamental es la elaboración de protocolos, tanto de cribado de RN susceptibles o no del CPP, como de medidas extraordinarias a realizar durante el vínculo, como puede ser el caso de asociar un saturímetro al seguimiento del RN en caso de encontrarse en algún grupo susceptible de mayor seguimiento, siendo injustificado el ingreso en unidades especiales para su observación.
Como medidas generales en el CPP podemos resumir las siguientes:
- Informar a los padres del CPP.
- Informar de los signos de alarma y/o alerta asociados al CPP:
- RN deprimido o no respira.
- RN cambia coloración y no es sonrosada.
- Madre muy agotada, incapaz de valorar al RN y no se encuentra acompañada.
- Implicar a los padres en la vigilancia y cuidados del RN en el CPP.
- Niño sobre la madre (decúbito prono).
- Cubrir con paños precalentados.
- Valorar APGAR.
- Pinzamiento de cordón.
- Identificación del RN.
- Colocar gorro.
- Valoración del RN c/15´ como máximo.
- Valoración de toma de lactancia si procede.
- Demorar acciones innecesarias en ese momento.
- Brindar un ambiente de respeto y seguridad, tanto a la madre como al RN.

El vínculo afectivo está también desarrollado dentro del volumen II, embarazo, en el apartado 11.5 y en el tema 1 parto, de este volumen.
Alimentación del recién nacido. Necesidades nutricionales del neonato. Tipos de lactancia. Lactancia artificial. Concepto. Alimentación con formulas lácteas. Técnicas de la lactancia artificial
A. Alimentación del recién nacido
Un 98 % de madres pueden amamantar por periodos largos de tiempo, de ellas, un 20-30 % precisan asistencia para superar algunos problemas que surgen durante la lactancia… Partiendo de esta estadística, y de los beneficios de la lactancia materna, nuestra postura deberá ser siempre proactiva frente a la lactancia materna, apoyando a las madres que la elijan, así como asesorando en las dudas o manteniendo una actitud positiva ante las madres que opten por la lactancia artificial, ya que no debemos juzgar en este tipo de decisiones.
Las recomendaciones actuales para la alimentación del RN son: lactancia materna exclusiva los 6 primeros meses. Introducir después de forma progresiva todos los alimentos, manteniendo la lactancia el máximo tiempo posible.. En el segundo semestre, la LM puede aportar el 50 % del aporte calórico y hasta el 30-20 % en el 2º año.
La leche materna es el alimento óptimo para el recién nacido, ya que cubre todas sus necesidades nutritivas, se aporta a demanda y se regula al volumen adecuado para su crecimiento sin sobrecarga para el aparato digestivo ni de otros sistemas aún inmaduros. La leche materna, suple y estimula el desarrollo del sistema inmune del recién nacido que no funciona de forma completa durante los primeros meses de vida. Sus componentes, junto con el intercambio de estímulos físicos y afectivos entre madre e hijo, logran el máximo potencial de desarrollo. Los RN alimentados con LM logran puntuaciones superiores en algunos ítems en las escalas de desarrollo psicomotor que los alimentados con fórmulas de inicio (FI).
Podemos resumir en los siguientes los beneficios de la lactancia materna:
- Estimula sistemas enzimáticos y metabólicos específicos que logran la programación nutricional, intestinal, enzimática y metabólica para el futuro.
- La leche de la propia madre consigue el mayor rendimiento nutritivo con la menor sobrecarga metabólica.
- Es el órgano inmunológico de transición que moldea y estimula el desarrollo del sistema inmune del recién nacido. Con el contacto cercano madre-hijo, la madre es estimulada para producir y transferir por la leche anticuerpos. Todo ello, explica los beneficios en la salud del niño mientras recibe LM y después, con menor número y gravedad de las enfermedades infecciosas y de enfermedades relacionadas con una respuesta inmune anómala.
- Se añaden un gran número de ventajas en el establecimiento del vínculo afectivo.
- Mayor desarrollo cerebral y sensorial con especial importancia en los prematuros y recién nacidos de bajo peso (BPN).
- Ventajas sobre la salud de la madre con un puerperio más fisiológico, retrasando la ovulación, disminuyendo el sangrado posparto y con mejor recuperación posterior de las reservas de hierro. Menor incidencia de algunos tumores ováricos y mamarios premenopáusicos.
- Supone un gran ahorro económico para los servicios sanitarios y la sociedad.
- Comodidad para la madre y sin riesgos derivados de la preparación de las FI.
B. Necesidades nutricionales del neonato
El crecimiento implica síntesis de tejidos y, por lo tanto, una acumulación progresiva de macro y micronutrientes, los que deben ser proporcionados por la alimentación de acuerdo a los requerimientos establecidos para cada grupo de edad. Los requerimientos para todos los nutrientes por parte del recién nacido y lactante, son superiores por unidad de peso corporal a los de cualquier otro grupo de edad y situación fisiológica, ya que son necesarios para el rápido crecimiento, desarrollo y maduración.
a. La necesidad energética del niño
Puede definirse como la ingesta calórica necesaria para mantener un estado de salud y crecimiento normal, así como un nivel de actividad física adecuado. Se expresa en función del peso corporal y corresponde a la suma de la energía requerida para metabolismo basal, crecimiento, actividad física y efecto termogénico de los alimentos.
b. Componentes del metabolismo energético
- Metabolismo basal 50-55 Kcal./kg./día.
- Energía para crecimiento20-40 Kcal./kg./día.
- Actividad muscular 20-25 Kcal./kg./día.
- Termogénesis postprandial5- 7 Kcal./kg./día.
- Pérdidas por excreción 7- 8 Kcal./kg./día.
La demanda calórica de los lactantes es superior a la de los adultos debido a una mayor pérdida de calor, a través de una superficie corporal relativamente mayor en relación al peso y al mayor porcentaje de tejido metabólicamente activo. Durante el primer año de vida, se emplea aproximadamente un 85 a 90 % de la ingesta energética estimada en el crecimiento y en la conservación del organismo, mientras que solo se destina un 10 a 15 % aproximadamente a la actividad física.
El conocimiento de las necesidades nutricionales del lactante en los primeros meses se ha obtenido del modelo biológico insuperable que es la leche materna. Se admite que la leche materna es capaz de cubrir por sí sola las necesidades energéticas hasta los seis meses, pero a partir de entonces podrían establecerse carencias en algunos nutrientes. Al utilizarse fórmulas lácteas en la alimentación del lactante, la proporción de energía suministrada por los principios inmediatos debe ser similar a la aportada por la leche materna, es decir, 38 % de hidratos de carbono, 48 a 54 % de lípidos y 8 % de proteínas. Años atrás, los requerimientos energéticos de los lactantes menores de un año se estimaron mediante estudios de ingesta efectuados en lactantes sanos, con crecimiento normal, incluyendo lactantes alimentados con pecho exclusivo y con alimentación artificial. En niños de uno a diez años, los requerimientos de energía se han establecido a partir de ingestas observadas en niños sanos, que crecen normalmente y que viven en países desarrollados.
Las recomendaciones de ingesta de energía correspondían por lo tanto al requerimiento promedio estimado, ya que no sólo debía evitarse el riesgo de desnutrición sino también el aporte excesivo que lleve a sobrepeso u obesidad. Por lo tanto, la vigilancia periódica del crecimiento es el mejor método para evaluar la suficiencia del aporte calórico.
Las necesidades de energía que se utilizaron hasta el año 2004 provenían de las establecidas por FAO/OMS/UNU en 1985, que se basaron en la ingesta diaria observada en lactantes y niños sanos más un 5 % extra, considerando una posible subestimación; éstas fueron actualizadas por la Organización Mundial de la Salud y adoptadas por nuestro país a partir del año 2005, ya que se considera que las ingestas observadas no reflejan necesariamente las ingestas requeridas. La estimación en base a gasto energético, depósito de tejido durante el crecimiento y composición corporal, estimada por el método de agua doblemente marcada, es lo más adecuado hoy en 400día y las nuevas recomendaciones de la OMS están basadas en estos métodos. El método permite la medición del gasto energético total o de 24 horas, determinando con muy buena precisión los requerimientos energéticos de una persona en su entorno, realizando su actividad diaria normal. La técnica fue desarrollada por Nathan Lifson y colaboradores a comienzos de los años 50 en la Universidad de Minnesota. La técnica del agua doblemente marcada consiste en la administración de una dosis oral conocida de agua marcada con isótopos estables del hidrógeno y de oxígeno. Posteriormente, se toman muestras de orina, saliva o plasma, en las que se determina la concentración de dichos isótopos y se calculan las curvas de velocidad de eliminación de los mismos. La determinación de las curvas, requiere un mínimo de dos muestras posteriores a la ingestión del agua marcada, sobre un período de varios días a varias semanas, dependiendo de la edad del sujeto y del nivel de consumo de agua.
c. Necesidades de proteínas
Las proteínas proporcionan aminoácidos esenciales y no esenciales necesarios para la síntesis proteica, el crecimiento y la reparación tisular.
Aminoácido esencial para el lactante puede definirse como aquel necesario para:
- Favorecer el crecimiento igual al de los lactantes amamantados por sus madres.
- Para mantener concentraciones de albúmina en suero iguales a la de los lactantes alimentados con leche humana.
- Para permitir el equilibrio nitrogenado positivo con una relación entre retención de nitrógeno e ingestión de nitrógeno equivalentes a lactantes alimentados por sus madres.
Los aminoácidos esenciales en el niño son: isoleucina, leucina, lisina, metionina, fenilalanina, treonina, triptofano, valina e histidina.
En recién nacidos, especialmente en prematuros, se agregan cisteína, tirosina y taurina que se comportan como condicionalmente esenciales dado que la capacidad de síntesis es insuficiente. A la taurina y nucleótidos se atribuyen efectos beneficiosos para el desarrollo gastrointestinal y el sistema inmune, la microflora intestinal y la absorción de hierro.
Las necesidades de proteínas en los menores de 6 meses, se han estimado por datos de ingesta en niños alimentados al pecho que crecen a velocidad satisfactoria. En mayores de seis meses, los requerimientos de manutención han sido calculados mediante estudios de balance nitrogenado, en tanto que las necesidades de nitrógeno para crecimiento se han estimado considerando la velocidad de ganancia de peso esperada y la concentración de nitrógeno corporal.
Es importante que para que el aprovechamiento proteico sea máximo, debe asociarse a una ingesta calórica adecuada, pues de lo contrario, parte de los aminoácidos son derivados a la producción de energía.
Se define que cifras mayores de 6 g./kg/día, se asocian con mayor morbilidad y mortalidad, acidosis, deshidratación hipertónica, fiebre y niveles séricos elevados de urea y amonio.
d. Lípidos
Además de actuar como fuente energética concentrada (9 Kcal/g), sirven de vehículo para vitaminas liposolubles y son proveedores de ácido linoleico y alfa- linolénico, precursores de la serie omega 6 y omega 3, respectivamente. Ambos deben constituir el 3 a 4 % de las calorías totales de la dieta. El aporte insuficiente de ellos, especialmente en los primeros meses de vida, puede producir detención del crecimiento. Los AGE son necesarios para la formación de membranas celulares, y en la síntesis de fosfolípidos y prostaglandinas fundamentales para la estructura del cerebro y tejido nervioso. Las grasas deben aportar un mínimo del 30 % de las calorías totales para asegurar la ingesta calórica y la sensación de saciedad. La leche materna tiene menor cantidad de grasa saturada y mayor de insaturada que la de vaca, destacando su riqueza en ácido oleico, ácidos grasos esenciales y eicosapentaenoico y docosahexaenoico. En el caso del lactante, la Academia Americana de Pediatría recomienda que las fórmulas infantiles proporcionen el 2,7 % de energía como mínimo en forma de ácido linoleico, y la Sociedad Europea de Gastroenterología y Nutrición Pediátrica (ESPGHAN) establece que ese aporte esté entre 4,5 y 10,8 % de la ingesta energética total. El límite máximo se establece para evitar reacciones adversas, especialmente una mayor peroxidación lipídica, inhibición de la formación de ácido araquidónico y de componentes de la serie de ácidos grasos omega 3 y de los correspondientes eicosanoides, así como posibles efectos inmunodepresores.
e. Hidratos de carbono
Constituyen la principal fuente energética de la dieta, siendo la lactosa el preponderante en los lactantes y el almidón en los niños mayores. No tienen un rol destacado como nutriente esencial, deben aportar el 60 % de las calorías totales aproximadamente. La leche humana aporta el 38 % de sus calorías como hidratos de carbono, la leche de vaca el 29 % y las fórmulas alrededor del 35 %, siendo el hidrato de carbono mayoritario la lactosa. La lactosa es fuente de galactosa para la formación de galactocerebrósidos. El recién nacido tiene limitada la capacidad de digestión de almidones como consecuencia de la deficiencia de amilasa pancreática, por lo que se recomienda que las fórmulas infantiles no contengan almidón o harina. Se permite que contengan glucosa y/o dextrinomaltosa.
f. Vitaminas y minerales
Su ingesta adecuada también es esencial para el logro de un crecimiento y desarrollo normales. Muchos de estos nutrientes actúan como cofactores o catalizadores en el metabolismo celular, y otros participan en el crecimiento de tejidos. Dentro de este último grupo merecen importancia el calcio, fósforo y magnesio que son incorporados mayoritariamente al tejido óseo. Ello indica la necesidad de mantener una ingesta suficiente de leche o sus derivados durante toda la etapa de crecimiento.
La leche humana es el patrón de referencia que permite una adecuada absorción tanto de vitaminas como de minerales, a diferencia con lo que ocurre en la leche de vaca; ejemplo es, la absorción del calcio y del hierro a partir de la leche humana que es del 75 y 70 %; en cambio, cuando el aporte proviene de la leche de vaca es del 20 a 30 %. Lo mismo ocurre en el caso de las fórmulas lácteas. La eficacia digestiva es mucho mayor a partir de la leche humana. Por esto, las fórmulas infantiles presentan aumentados niveles de muchos de estos nutrientes, al tener en cuenta que el aprovechamiento digestivo de las fórmulas es menor.
Hierro y zinc pueden ser limitantes potenciales del crecimiento a partir del segundo semestre de vida y muy especialmente en etapa preescolar. El hierro puede dar lugar a deficiencias, aunque la leche materna es pobre en hierro, su biodisponibilidad es muy elevada y puede cubrir las necesidades hasta los 6 meses.
Las fórmulas sin embargo, deben ser suplementadas.
g. Agua y electrolitos
Las necesidades diarias de agua son aproximadamente 150 ml/kg de peso al día en los primeros 6 meses de vida. Aunque puede variar en función de la temperatura, aumento de pérdidas o carga renal de solutos de la alimentación. El agua en condiciones normales ingresa al organismo por la alimentación y la sintetizada como resultado de la oxidación de macronutrientes. Existe una directa relación entre consumo calórico y los requerimientos de agua, de tal forma que por cada 100 Kcal. metabolizadas, el organismo necesita entre 110 – 150 ml. de agua.
El 60 % del peso corporal es agua, la que depende de la edad: 62 % en el lactante, 83 % en el recién nacido de pretérmino y 79 % en el recién nacido de término.
Los líquidos corporales se distribuyen en dos grandes espacios. Dos tercios son fluidos intracelulares y un tercio es líquido extracelular, que a su vez está constituido por el espacio intravascular y el intersticial. Hay que considerar que la variación en el volumen de agua secundario a la edad será mayor en el recién nacido y el lactante, en favor del extracelular.
Otro aspecto importante a considerar del compartimento extracelular es la cuantificación del volumen intravascular o volemia, ya que éste también refleja variaciones en términos de la edad. A partir de los tres meses, los volúmenes sanguíneos totales por kilo de peso pasan a ser prácticamente iguales a los de un adulto.
Estimación de volumen sanguíneo.
- RNPretérmino 85-100 ml/kg.
- RNTérmino 85 ml/kg.
- 1-3 meses 75 ml/kg.
- 3 meses-adulto 70 ml/kg.
El lactante tiene una mayor necesidad de agua porque:
- Tiene una mayor superficie cutánea en relación al peso.
- Presenta taquipnea por lo que hay un aumento de agua por la respiración.
- Presenta mayor actividad metabólica.
- Tiene menor capacidad de concentración renal. El niño no ha desarrollado totalmente su capacidad de producir orina concentrada, necesitando más cantidad de agua para disolver las sustancias que se eliminan por orina que el adulto.
- Presenta un activo crecimiento.
El requerimiento de agua es la suma de:
- Pérdida de agua por evaporación (piel y pulmones): en lactantes sanos de término no expuestos a situaciones ambientales extremas, el agua excretada por piel y pulmones representan la mayor proporción del requerimiento de agua: 30 a 70 ml/kg/día. Al ser sometidos a altas temperaturas estas pérdidas pueden aumentar en 50 a 100 %, 10 % por cada grado de temperatura por sobre lo normal.
- Pérdida de agua por heces: la pérdida de agua en lactantes es igual a 10 ml./kg./día o 13 % del requerimiento total. En caso de diarrea, las pérdidas pueden aumentar 5 a 6 veces. Otra situación que puede determinar incremento en las pérdidas fecales es la osmolaridad de la fórmula, que generará una presión osmótica que provocará salida de agua del medio interno al intestino. La osmolaridad viene dada por el número de moléculas presentes en ella.
- Agua requerida para crecer: representa alrededor del 2 % de las pérdidas. El proceso de crecimiento exige un determinado consumo de agua, a pesar de la gran velocidad de crecimiento, sobre todo en los primeros meses de vida, la cantidad de agua que se exige es pequeña.
- Pérdidas urinarias: son pérdidas obligadas que permiten disolver los productos del metabolismo normal. El agua renal representa el 50 % de las pérdidas. La cantidad de agua excretada por orina está determinada por la carga renal de solutos y la capacidad renal de concentración. Pueden modificarse en función de ellos.
La carga renal de solutos, está representada por los solutos que deben ser excretados por el riñón, y determinada por los componentes dietéticos no metabolizables: electrolitos en exceso(minerales) y componentes nitrogenados(proteínas).
Es importante considerar la carga renal de solutos cuando:
- Disminuye la ingestión de líquidos, incluyendo la administración de dietas de alta concentración calórica.
- Aumento de las pérdidas de agua extra renal por fiebre, diarrea, hiperventilación, aumento de la temperatura ambiental.
- Deterioro de la capacidad de concentración renal, en casos de desnutrición proteica y calórica, y diabetes insípida.
La capacidad renal de concentración es muy pequeña en la primera época de la vida, aumentando significativamente hasta el año de edad. Por ello, el lactante en su primera época para una determinada carga renal de solutos, necesita mucha más agua para la eliminación renal.
Por lo tanto, es importante conocer la relación que existe entre la carga renal de solutos, la capacidad de concentración renal y el equilibrio hídrico, ya que estos tres aspectos pueden ser esenciales para conservar el estado de salud del lactante.
Cuando las pérdidas extra renales de agua son grandes y hay limitaciones en la capacidad del riñón para concentrar orina, la selección del tipo de alimento y por lo tanto la carga renal de solutos, se transforma en un elemento crítico en el balance acuoso, esto reviste mayor importancia cuando la ingesta total de agua no se adecua a los requerimientos.
Un litro de leche materna, libera aproximadamente 75 m Osm. Fórmulas no maternizadas, basadas en leche de vaca 184 y 248 m Osm/lt., dependiendo de su contenido proteico.
Cálculo simplificado de necesidades de agua:
- 1° semestre 50 ml/kg/día.
- 2° semestre 130 ml/kg/día.
- 2 a 6 años 110 a 100 ml/kg/día.
- 7 años y más 80 a 50 ml/kg/día.
Los requerimientos de agua de los recién nacidos se relacionan con el consumo calórico, la temperatura ambiental, la actividad y la tasa de crecimiento.
El lactante requiere en promedio el 15 % de su peso en agua. Fórmula práctica es 1kcal = 1,1 a 1,3 ml. El agua que necesita el lactante proviene fundamentalmente de la que contiene la leche materna o biberón.
C. Tipos de lactancia
La tendencia actual es la recomendación de lactancia materna exclusiva (pecho, biberón o sonda nasogástrica) hasta los 6 meses de vida (OMS).
Dependiendo de las situaciones particulares podemos encontrar además:
- Lactancia mixta (lactancia materna combinada con tomas de lactancia artificial) o
- Lactancia artificial (no hay aporte de leche materna).
D. Lactancia artificial. Concepto. Alimentación con fórmulas lácteas
La composición y formas de administración han sido establecidos por organismos científicos:
- Comité de Nutrición de la Sociedad Europea de Gastroenterología, Hepatología y Nutrición pediátrica (ESPGHAN)
- Comité de Nutrición de la AAP (American Academy of Pediatrics)
- Comité de Nutrición y de Lactancia Materna de la Asociación Española de Pediatría (AEP), así como con normativas oficiales para su cumplimiento (Código de Comercialización de sucedáneos de leche materna).
La indicación de sustitutos de leche materna ha de ser hecha por el pediatra, valorando antes la posibilidad o no de lactar. Las Fórmulas de Inicio (FI) pueden sustituir a la leche materna cuando ésta no es posible, han de cubrir las necesidades del RN con peso mayor de 2.500 g. al nacer hasta los 4-6 meses.
Las Fórmulas de Bajo Peso cubren las necesidades de los niños de bajo peso hasta la edad de a término aproximadamente, para lograr un crecimiento semejante al intrauterino, aportando nutrientes condicionalmente esenciales en el prematuro (aminoácidos, nucleótidos, LC-PUFA w3-w6, oligosacáridos, etc.) y mayores aportes de proteínas, calorías y minerales. Ambos tipos de leche se administran inicialmente tras confirmar tolerancia con una toma de agua, suero glucosado 5 % o leche diluida al medio, con biberones cada 3 horas, 6-8 tomas al día, (no hay evidencia científica que permita recomendar una u otra de estas pautas adoptadas por diferentes centros).
Se comienza con unos 50 ml /kg/día y aumentando unos 10-20 ml /kg/día hasta alcanzar los 150 ml -170 /kg/día (120 -130 Kcal/kg/día) hacia los 8-10 días, para seguir así los primeros meses. Las leches artificiales se prepararán con agua libre de gérmenes y pobre en minerales, inicialmente aguas envasadas o aguas potables del grifo si la composición lo permite por niveles de sales y de nitritos. En estos casos se recomienda la ebullición del agua durante un minuto desde que comienza a hervir. No es necesario más tiempo porque concentra las sales en el agua.
Suplementos: Las FI están suplementadas con vitaminas y minerales de manera que cubren las necesidades cuando se aportan los 500 ml al día.
E. Técnicas de la lactancia artificial
A pesar de las reconocidas ventajas de la lactancia natural, se dan algunos casos en los que ésta no es posible. Cuando se dan esos casos, la madre puede optar por alimentar al lactante con preparados de fórmula.
a. Clasificación de las fórmulas, según ESPGHAN
Fórmulas de inicio:
Son aquellas que cubren por sí solas todas las necesidades nutritivas del lactante sano nacido a término, durante los seis primeros meses de vida; no obstante, pueden ser utilizadas conjuntamente con otros alimentos desde los seis a los doce meses.
- Fórmulas de continuación:
Destinadas a ser utilizadas a partir de los seis meses conjuntamente con otros alimentos. Según las recomendaciones de la ESPGHAN, su administración puede prolongarse hasta los tres años con ventaja sobre la leche de vaca.
b. Recomendaciones en la preparación de la toma
Después de lavarse cuidadosamente las manos, tomar la tetina y el biberón previamente desinfectados. Se empleará agua mineral sin gas. Es conveniente preparar los biberones antes de cada toma. Si se prepara más de uno deberán conservarse en frío hasta su utilización hasta un máximo de 24 horas.
1 cacito de leche por cada 30 ml de agua.
c. Técnica de la lactancia artificial
En cuanto a las precauciones que se deben tomar: un entorno tranquilo, el niño cómodo, semiincorporado con la cabeza apoyada en el brazo y el cuerpo mantenido por el antebrazo, son similares a las recomendaciones en la lactancia materna.
No dar nunca biberón a un bebé que permanece acostado por el peligro de aspiración.
Cuando se ofrezca el biberón, nos aseguraremos que la tetina esté siempre llena de leche y no de aire. Nunca hay que obligarle a que se lo termine si él no quiere. Concluida la toma, que aproximadamente durará 15-20 minutos, se le incorporará nuevamente y con unos suaves golpecitos en la espalda para favorecer la expulsión de gases.
Determinación del volumen de las tomas.
La distribución horaria deberá ser ajustada por el pediatra a las necesidades particulares de cada niño. Las ingestas señaladas por el fabricante para cada edad son sólo orientativas.
Por regla general, durante las primeras 2 semanas el bebé puede ingerir 8 tomas de 60 cc Entre la segunda y la octava semana se recomiendan 7 tomas con 90 cc Durante el segundo y tercer mes puede disminuirse el número de tomas a cinco diarias, atendiendo a las necesidades del lactante, siendo el profesional el que ajustará las pautas.

d. Signos de alerta que debemos identificar para prevenir déficits en la alimentación del RN
- Pérdida ponderal más de 3-4 días o incremento lento: no recuperación a los 14 días.
- Signos de deshidratación.
- Lactante hiperalerta, hambriento o letárgico e indiferente.
- Queda dormido tras escasas succiones al pecho.
- Disminuye la diuresis y el volumen de las heces.
- Signos de mala posición: boca muy cerrada, alejado del pecho, pezón dañado o niño que succiona muy rápido, mucho tiempo sin llegar a saciarse o sin aumento de peso.
Lactantes de riesgo:
- Recién nacidos de 35 a 37 semanas que no ingresan y se van de alta con la madre en las primeras 48-72 horas. Disfunción en la succión: mala posición, incoordinación, succión mordiente o poco vigorosa. Problemas neurológicos. Niños sedados por medicación en el parto o tratamientos maternos.
- Niños que han recibido suplementos en el hospital. Durante unos días, además de mayor ayuda para la puesta al pecho, la madre deberá extraerse la leche para que la secreción no disminuya, por lo que habrá que explicar los métodos de extracción y conservación de la LM. Administrarla al niño con jeringa o cuchara hasta recuperar el peso o lograr una buena succión.
Madres que podemos catalogar de riesgo:
- Adolescentes
- Fumadoras
- Sin pareja
- Sin ayudas familiares y bajo nivel socio-cultural
- Medicaciones en la madre
- Niños que han sido separados de su madre y
- Madres que no tengan una decisión firme de lactar
Estas madres necesitan apoyo físico y psíquico casi diario inicialmente. Otras madres pueden ayudarles. Por ello es importante crear grupos de apoyo a la lactancia en los centros de salud.
Un 75 a 90 % de las madres en España, inician sus lactancias en el hospital. Múltiples factores sociales, educacionales, laborales, rutinas hospitalarias, el marketing comercial y en especial la pérdida de cultura de la lactancia entre familiares y amigos, junto con la falta de apoyo práctico de los profesionales a los que las madres piden asesoramiento, hacen que muchas madres que intentan lactar no logren sus objetivos, cerrándose un círculo de desconfianza en su capacidad de lactar. Es por ello, que resulta imprescindible que los profesionales reciban cursos de sensibilización y formación en materia de lactancia.
Asesoramiento al alta. Importancia del asesoramiento a los padres en el alta del recién nacido. Pruebas de cribaje. Signos de salud/enfermedad. Vacunaciones: calendario. Prevención de los accidentes neonatales. Programa de seguimiento del niño sano
A. Asesoramiento al alta. Importancia del asesoramiento a los padres en el alta del recién nacido
La educación sanitaria es fundamental para la difícil aventura de cuidar al neonato en el domicilio, nuestras recomendaciones sobre alimentación, signos de alerta, cuidados generales del RN (baño, cordón, etc..), así como prevención de infecciones en las primeras semanas (contacto con personas que puedan transmitirlas), factores de riesgo (principalmente hábito tabáquico).
Asímismo, se debe hacer especial hincapié en el seguimiento del RN en los programas sanitarios, tanto control del niño sano, como programa de vacunación de su comunidad.
B. Pruebas de cribaje
a. Hipoacusia
La detección precoz, mediante el cribado neonatal, permite un rápido diagnóstico y tratamiento. Actualmente existen dos técnicas comercializadas y de aprobada fiabilidad, utilizadas en distintos países, nos referimos a las Otoemisiones Acústicas Evocadas (OEA) y a los Potenciales Auditivos Evocados de Tronco Cerebral Automatizados (PEATC-a). Las OEA es una prueba que consiste en recoger la respuesta de las células ciliadas externas mediante un receptor colocado en el conducto auditivo externo (CAE), tras la estimulación sonora mediante un clic, emitido por un micrófono colocado en CAE. Esta técnica sencilla y rápida, reproducible, objetiva, inocua y fiable: sensibilidad: 80-100 % y especificidad: 90 %. Tiene el inconveniente que precisa de la combinación de los PEATC-a, ya que sólo exploran la vía auditiva hasta la cóclea (células ciliadas externas).
Hay que destacar la posibilidad de aparición tardía de hipoacusia en las siguientes situaciones:
- Antecedentes familiares de hipocausia
- Síndrome, cromosomopatías, enfermedades neurodegenerativas
- Infecciones gestacionales tipo TORCH:
- Toxoplasmosis
- Sífilis
- Rubeola
- Citomegalovirus
- Herpes
- HIV
- Encefalopatías hipóxico-isquémicas graves
b. Cribado de enfermedades metabólicas
Se basa en la determinación en sangre del RN de la existencia de determinadas enfermedades denominadas “raras” que, debido a su trascendencia, debemos hacer especial hincapié en la información a los padres para la captación del 100 % de los RN… El momento de la toma de muestra será desde el tercer día (a partir de las 48 horas de vida) hasta el quinto día, siendo preferible la determinación en el tercer día. Las pruebas se consideran de urgencia, con lo que se facilitarán por parte de todos los profesionales, tanto en Atención Primaria como en Especializada. En caso de detectar problema social en el núcleo familiar, se procederá a la toma de muestra incluso antes del tercer día, antes del alta hospitalaria.
En los casos que se detallan a continuación es necesario tomar una segunda muestra:
- De manera rutinaria para confirmar los resultados de la prueba de
hipotiroidismo:
- A las dos semanas (15 días) de vida en caso de:
- Recién nacido de bajo peso (igual o menor de 2.500 g)
- Edad gestacional inferior a 37 semanas
- Neonatos de partos múltiples
- Neonatos cons Síndrome de Down
En todos estos casos deberá especificarse en la historia clínica la necesidad de esta muestra adicional a los 15 días, si el niño o niña está ingresado en el Servicio de Neonatología, o figurar en el informe de alta si se va al domicilio y comunicárselo verbalmente a la familia.
- Nueva muestra para cribado neonatal al alta hospitalaria en caso de:
- Gran prematuro (<31 semanas).
- Muy bajo peso (<1.500 g).
- A los 3 meses de vida en caso de recién nacidos politrasfundidos.
- A petición del laboratorio de referencia.
- Por muestra inadecuada.
- Resultado de la primera muestra dudoso o fuera de los intervalos de referencia establecidos.
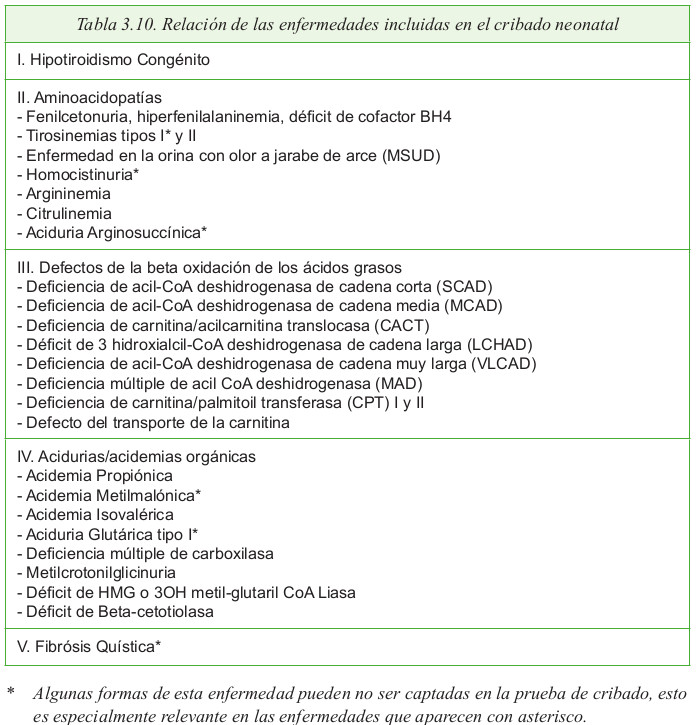
C. Signos de salud/enfermedad
Debemos instruir a la familia en la valoración de signos de alerta y que son necesarios consultar inmediatamente con un profesional, como son:
- Aparición de petequias.
- Temperatura por encima de los 38 ºC.
- Convulsiones.
- Letargia, que suele asociarse a pérdida de apetito (más de 8 horas sin realizar tomas).
- Cianosis, generalmente asociada a episodios de apnea.
- Vómitos insistentes (que generalmente se acompaña de pérdida de peso).
- Pérdida de peso.
- No emisión de orina.
- Heces diarreicas (insistir en las características normales de las heces del neonato, informaremos del riesgo de las heces acuosas).
Datos que indican una buena alimentación y bienestar del RN:
- Pérdida fisiológica de 3-4 días, de 6-10 % que recupera hacia el 10-14 día y con aumento posterior de más de 20 g. día. Los desnutridos al nacer deberían no perder o tener pérdida mínima.
- Niño activo, succión vigorosa y relajado al finalizar.
- Tras succión rápida inicial, la succión se enlentece y se observa al RN deglutir, la madre nota que sale leche, sensación de reflejo activo y pecho más vacío.
- Succionan vigorosos desde pocos minutos a 10-15 min. Cada RN tiene su forma de tomar.
- Moja 4-6 pañales al día a partir del 4º día. Deposiciones blandas 5-6 por día o espaciadas cada 2-3 días pero abundantes.
D. Vacunaciones: calendario
En el año 2014 la Asociación Española de Pediatría ha consensuado un calendario vacunal unificado para todas las comunidades en un intento de disminuir la variabilidad existente, de entre los principales cambios existentes, tenemos los siguientes:
- La primera dosis de las vacunas: triple vírica (TV) y de la varicela se recomiendan a los 12 meses.
- La segunda dosis de las vacunas TV y de la varicela se recomienda entre los 2 y 3 años, con preferencia a los 2 años.
- Se cambia la pauta de vacunación frente al meningococo C, pasando de un esquema 2+1 a un esquema 1 o 2+1+1: una dosis a los 2 y 4 meses o solo a los 4 meses (según preparado vacunal), otra a los 12 meses y una tercera, en la adolescencia, a los 12 años de edad.
- Dada la duración limitada de la inmunidad frente a la tos ferina, se vuelve a recomendar la vacuna combinada de alta carga antigénica frente al tétanos, la difteria y la tosferina (DTPa) o la vacuna combinada de baja carga antigénica frente al tétanos, la difteria y la tosferina (Tdpa) a los 4-6 años y la Tdpa a los 11-12 años. Ya que la mayoría de las CC.AA. utilizan la Tdpa a los 4-6 años, se recomienda que vaya obligatoriamente seguida de otra dosis de Tdpa a los 11-12 años.
- La vacuna frente al meningococo B se recomienda actualmente para el control de brotes epidémicos, y se insiste en la necesidad de que sea comercializada libremente en las oficinas de farmacia.
Fuera del calendario infantil, se recomienda la vacunación con Tdpa a la embarazada a partir de la 27 semana de gestación, y a los miembros del entorno familiar de los recién nacidos (especialmente de la madre, no previamente vacunada en el embarazo, en el puerperio inmediato).
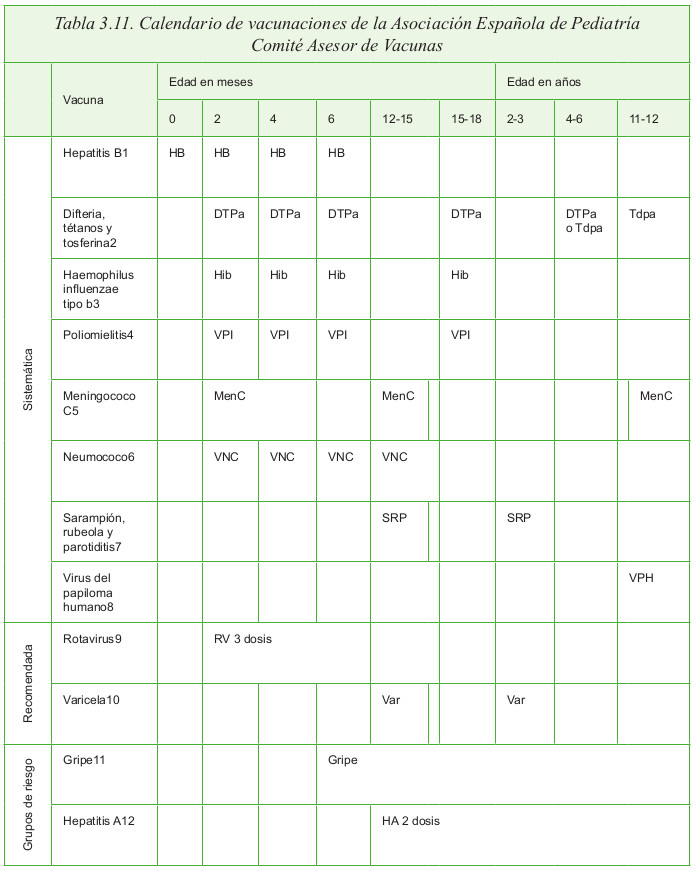
E. Prevención de los accidentes neonatales
a. Síndrome de la Muerte Súbita del Lactante (SMSL)
Dentro de la prevención de accidentes en el neonato, las intervenciones van encaminadas fundamentalmente, al control del Síndrome de la Muerte Súbita del Lactante (SMSL), que se define como la muerte súbita de un niño menor de un año de edad, a la cual no se encuentra explicación después de una investigación minuciosa del caso, incluyendo la realización de una autopsia completa, el examen de la escena del fallecimiento y la revisión de la historia clínica.
Es la principal causa de muerte en niños de un mes a un año de edad en los países desarrollados (40-50 % de dicha mortalidad). En España se estima una frecuencia de 2 por mil nacidos vivos.
Es más frecuente en varones (3:2).
Su máxima incidencia ocurre entre el 2º y 4º mes de edad, siendo poco frecuentes los casos antes de las dos semanas y después de los seis meses de vida.
La mayoría de los casos ocurren entre la medianoche y las nueve de la mañana, por lo que se supone que se producen durante el sueño. También hay una mayor incidencia en los meses fríos y húmedos.
Factores de riesgo asociados al SMSL
Factores relacionados con la madre:
- Tabaquismo durante y después del embarazo. En la actualidad es el mayor factor de riesgo (50 % de los casos de SMSL) desde la generalización del consejo de dormir en decúbito supino.
- Lactancia artificial.
- Madres jóvenes, solteras, distocia social.
- Drogas y alcohol.
- Multíparas con periodos muy cortos entre embarazos.
Factores relacionados con el niño:
- Antecedente de hermano fallecido por SMSL. El riesgo de recurrencia es de 2-10 veces mayor. En caso de gemelos o trillizos es hasta 40 veces mayor en las primeras 24 horas tras el fallecimiento del hermano.
- Prematuridad y bajo peso al nacer.
- Displasia broncopulmonar, apneas sintomáticas.
- Lactantes que presentaron un episodio aparentemente letal (EAL). Este se define como una apnea brusca con cambios de la coloración (cianosis o palidez), del tono muscular (hipotonía, hipertonía) y con sensación de muerte inminente (muerte súbita abortada).
- Niños con dificultades en la ingesta de alimentos (malformaciones faciales).
- Aumento del tono vagal (apnea o bradicardia refleja).
Factores ambientales:
- Postura del lactante en la cuna en decúbito prono (boca abajo), es posiblemente el mayor factor de riesgo. También presenta mayor riesgo el decúbito lateral (más de seis veces que el decúbito supino) ya que es inestable y muchos de los niños colocados así acaban en decúbito prono.
- Arropamiento excesivo y sobrecalentamiento en la cuna.
- Colchones blandos.
- Compartir la cama con un adulto, sobre todo con madres fumadoras.
- Bajo nivel socioeconómico.
Recomendaciones de la AEP
Para lactantes menores de 6 meses, posición para dormir, decúbito supino (disminuye en más de un 50 % la posibilidad de SMSL).
La lactancia materna es un factor de protección frente a la MSL.
El colecho, aunque favorecedor de la lactancia materna, tiene una serie de consideraciones especiales, por lo que no debe recomendarse en:
- Lactantes menores de 3 meses de edad.
- Prematuridad y bajo peso al nacimiento.
- Padres que consuman tabaco, alcohol, drogas o fármacos sedantes.
- Situaciones de cansancio extremo en los padres.
- Colecho sobre superficies blandas.
- Compartir la cama con otros familiares, con otros niños o múltiples
personas.
- Se puede optar por colocar la cuna junto a la cama de los padres (modelo sidecar) para favorecer las tomas de lactancia.
- El uso de chupete, tras los primeros meses de vida, previene el SMSL.
La población de alto riesgo debe ser incluida en un programa de monitorización domiciliaria. Los monitores registran el movimiento respiratorio y la actividad eléctrica del corazón. En la mayoría de los casos esta monitorización puede suspenderse entre los seis y nueve meses, si en los dos meses previos no hubo apneas reales. En los hermanos de víctimas del SMSL se retirará siempre al menos un mes después de la edad a la que falleció el hermano.
b. Recomendaciones de uso de cabestrillos portabebés
La AEP se hace eco de la comunicación de más de 20 accidentes mortales neonatales asociados al mal uso de estos dispositivos en los últimos 20 años, en diferentes países, por lo que hace las siguientes recomendaciones por parte de su propio comité de seguridad y prevención de lesiones infantiles:
- Evitar la compresión de la nariz o boca del neonato por el cuerpo del adulto que lo sostiene.
- Evitar la flexión de la cabeza del RN, ya que puede provocar un episodio de asfixia y no podrá llorar, con lo que el adulto que lo porta no se dará cuenta del hecho.
- Evitar tapar la cabeza del bebé, para que pueda respirar convenientemente.
- Los portabebés son especialmente peligrosos si se usan en el siguiente
contexto:
- Niños menores de 4 meses
- Gemelos
- Prematuros
- Niños de bajo peso al nacimiento
- Niños con infecciones de vías respiratorias
c. Evitar prendas y objetos que puedan obstruir la vía aérea o que se desprendan y obstruyan la misma
F. Programa de seguimiento del niño sano
Aunque se pueden dar diferencias según en qué CC.AA. nos encontremos, en general se pueden recomendar los siguientes controles para el seguimiento del control del niño sano:

a. Revisión del recién nacido
Debe llevarse a cabo entre el 5º-10º día de vida. Es aconsejable que la realice el pediatra y el profesional de enfermería conjuntamente para establecer el primer contacto con los padres del niño.
Es fundamental la captación activa de los recién nacidos informando a las mujeres embarazadas en las consultas de medicina, enfermería y matrona, de la necesidad de realizar una primera visita en esos días.
Apertura de la historia clínica:
- Antecedentes obstétricos maternos: GAV (gestaciones, abortos, nacidos vivos).
- Historia del embarazo: deseado o no, controles, feto único o no, patología, fármacos, hábitos tóxicos…
- Factores de riesgo psicosocial: familias monoparentales, situación laboral, ocupación, inmigración, drogadicción, enfermedades mentales…
- Antecedentes familiares: consanguinidad, enfermedades (diabetes mellitus, HTA, dislipemias…) y hábitos tóxicos.
- Antecedentes perinatales: edad gestacional, tipo de parto, test de Apgar, reanimación, peso, talla y perímetro cefálico, peso al alta hospitalaria, pH y grupo sanguíneo, emisión de meconio y diuresis, ictericia, ingreso neonatal…
Anamnesis:
- Informarnos sobre hábitos de descanso y posición para dormir del RN (prevención SMSL).
- Dudas surgidas en los primeros días, valoración de la adaptación de los padres a su nueva situación.
- Actitud ante la lactancia: tipo de lactancia, habilidades, conocimientos y dudas.
- Entorno socioeconómico del RN.
- Vómitos y/o regurgitaciones.
- Características de las micciones (número y cantidad, así como información sobre el chorro miccional, en varones, y/o coloración de las mismas) y de las deposiciones.
- Cuidados higiénicos: cuidados del cordón, baño, genitales, piel, ropa…
Exploración física:
- Somatometría: peso, talla y perímetro cefálico con percentiles y registro en las gráficas correspondientes.
- Fenotipo.
- Coloración de piel y mucosas: ictericia, palidez, perfusión, angiomas, nevus…
- Cráneo: morfotipo, cefalohematoma, caput sucedaneum, fontanela y suturas.
- Boca: labio leporino, fisura palatina, muguet, dientes…
- Ojos: inspección descartando malformaciones del cristalino, iris, córnea, párpados. Valorar motilidad ocular, reactividad pupilar y reflejo rojo retiniano.
- Audición: posición de los pabellones auriculares, apéndices cutáneos, pruebas subjetivas de audición…
- Cuello: masas, movilidad, tortícolis congénita. Clavículas.
- Palpación de pulsos periféricos.
- Tórax: morfología, auscultación cardiopulmonar, inspección de las mamas…
- Abdomen: morfología, palpación de masas y visceromegalias, inspección del ombligo, descartar hernias…
- Genitales:
- Niños: pene (tamaño y morfología), meato uretral (hipospadias, epispadias u otras malformaciones), escroto (situación de testes, hidrocele…).
- Niñas: himen imperforado, sinequias vulvares, hipertrofia de clítoris…
- Ano y recto: descartar fosa, fístula o quiste pilonidal.
- Aparato locomotor: caderas y extremidades.
- Neurológico: respuestas neurológicas del recién nacido, tono muscular…
Valoración de la necesidad de realización de pruebas metabólicas (cribado neonatal de metabolopatías congénitas). Se debe confirmar que se ha realizado en el hospital la primera extracción de sangre para el despistaje de metabolopatías.
En general, recomendaciones sobre alimentación, cuidados, higiene, ropa y prevención de accidentes, así como intentar detectar debilidades en los cuidadores para poder reforzar los cuidados necesarios.
b. Revisión al mes de vida
Además de la entrevista a los padres en busca de datos que nos puedan hacer sospechar de alguna desviación de la normalidad (alimentación, hábitos reposo/ sueño, deposiciones y micción, etc..) o nos puede servir para poder resolver dudas de los cuidadores, realizaremos las siguientes valoraciones.
Se realizará exploración física completa con especial atención a:
- Estado general.
- Somatometría: peso, talla y perímetro cefálico indicando los percentiles y registrándolos en las gráficas correspondientes.
- Coloración de piel y mucosas: perfusión, hidratación, ictericia, palidez, angiomas, nevus… Dermatitis.
- Cabeza: fontanelas, suturas, deformidad de la cabeza por decúbito…
- Cuello: masas, movilidad (tortícolis congénita)…
- Boca: muguet…
- Ojos: inspección descartando malformaciones del cristalino, iris, córnea, párpados… Valorar motilidad ocular completa al giro pasivo de la cabeza, reactividad pupilar, reflejo rojo retiniano y comportamiento visual (es capaz de seguir la cara de su madre).
- Exploración subjetiva de la audición con anamnesis dirigida a los padres.
- Auscultación cardiopulmonar y palpación de pulsos periféricos.
- Abdomen: masas, visceromegalias, hernias…
- Locomotor: caderas (abducción y simetrías), pies…
- Genitales: testes (situación, hidrocele), sinequias vulvares.
- Ano.
- Dermatitis del pañal.
- Neurológico: actitud, tono, movilidad y reflejos.
- Valoración del desarrollo psicomotor: mantiene la cabeza, sigue una luz, reacciona a los sonidos…
- Signos de negligencia, maltrato o abuso del niño.
Los controles posteriores van encaminados a realizar una valoración general del lactante y su entorno familiar para poder identificar problemas o negligencias y reforzar en las conductas adecuadas en el cuidado del menor.
Iremos añadiendo recomendaciones sobre alimentación a partir del 6º mes de vida, valoración de caderas, relacionar persistencia de reflejos con posibles patologías (p.ej. reflejo de Moro persistente tras 7º mes), recomendaciones en prevención de accidentes adaptadas a la edad del niño.
c. Recomendaciones de valoraciones complementarias
0-2 años; pueden realizarse las siguientes escalas de valoración:
- Test de desarrollo de Gessell: desde 4 semanas a 5 años. Explora conducta motora, adaptativa, lenguaje, personal y social. Mide edad y cociente de desarrollo en cada área y global.
- Escala de Brunet-Lezine: de 1 a 30 meses. Cuatro sectores del desarrollo: motor-postural, coordinación óculo-motriz, verbal y social. Cociente de desarrollo para cada una de estas áreas (información sobre el ritmo de desarrollo de ese niño en relación con los de su misma edad).
- Escala de desarrollo de Bailey: de 2 a 30 meses. Escala mental que proporciona un índice de desarrollo mental del niño y una escala motriz que proporciona un índice de desarrollo psicomotor.
- Inventario de desarrollo Battelle: de 0 a 8 años. Explora conducta motora, adaptativa, comunicación, personal y social y cognitiva.
- Escalas McCarthy: de 2½ a 8½ años. Índice cognoscitivo general (equivalente a CI).
3-5 años. El estudio se centra en el cribado de problemas de salud mental:
- Hitos evolutivos del niño. Examen del Desarrollo Infantil de la Población de Denver (EDIPD). De 0 a 6 años.
- Nivel socio-emocional. ASQ-SE. Cuestionario para padres. De 6 meses a 5 años.
- Sospecha TDAH: Escala abreviada de Conners para padres y profesores (20 items). De 3 a 17 años.
- Sospecha oposicionismo. Cuestionario de capacidades y dificultades (SDQCas). De 4 a 17 años. Para padres y profesores.
- Childhood Asperger Syndrome Test. De 4 a 11 años. Cuestionario para padres y profesores.