Cribado
Concepto y objetivos
El cribado es una actividad de la práctica médica. La Organización Mundial de la Salud (OMS) lo define como «la identificación presuntiva, con la ayuda de pruebas, exámenes u otras técnicas susceptibles de aplicación rápida, de los sujetos afectados por una enfermedad o por una anomalía que hasta entonces había pasado desapercibida». El cribado es una medida de prevención secundaria; su finalidad básica es disminuir la incidencia de complicaciones derivadas de una enfermedad (ej. ceguera en la retinopatía diabética), disminuir la mortalidad por un proceso (ej. cáncer colorrectal) o aumentar la calidad de vida de las personas afectadas por una determinada patología.
Puesto que el cribado se dirige a la población «sana» (sin noción de enfermedad), sus requisitos éticos son más estrictos que los exigibles a las pruebas diagnósticas que se aplican cuando es la población —y no el médico— quien toma la iniciativa de buscar la atención clínica por notarse unos síntomas atribuibles a un problema de salud. Esto se debe principalmente al hecho de que el uso de pruebas diagnósticas no está exento de riesgos y efectos colaterales, que en el caso del cribado serían completamente prevenibles si no se realizase éste. A los riesgos derivados del uso de pruebas diagnósticas hay que añadir los secundarios a la ansiedad injustificadamente generada y a los tratamientos aplicados cuando el resultado del cribado es un falso positivo.
En el profesional sanitario existe la creencia errónea pero muy arraigada de que diagnosticar precozmente un proceso es «siempre» mejor, porque el tratamiento aplicado en las fases iniciales de la enfermedad tiene mayores posibilidades de éxito. Sin embargo, en cada caso debe demostrarse que, efectivamente, tratar antes de la fase clínica es mejor que hacerlo cuando se manifiesta abiertamente la enfermedad. Los sanitarios deben conocer los factores que contradicen la supuesta «lógica» de los beneficios del tratamiento en la fase asintomática.
Cuando el tratamiento aplicado tras la detección precoz de una determinada enfermedad es curativo, y además tiene una mayor efectividad si se aplica precozmente que si se hace tras la manifestación natural de la enfermedad, se observará una disminución de la prevalencia y de la mortalidad por dicha enfermedad, si éste es el efecto que hay que prevenir. Si el tratamiento es paliativo, pero prolonga la vida de forma real (y no de forma artificial, por el tiempo sobreañadido de enfermedad debido al adelanto diagnóstico como efecto del cribado), se producirá un aumento de la expectativa de vida de los enfermos y un aumento de la prevalencia.
Inicialmente se observará un descenso de la mortalidad, que luego se equilibra por su desplazamiento a edades más avanzadas. Este aumento de la expectativa de vida se traduce en una disminución de la letalidad y un aumento de la prevalencia de la enfermedad. En un programa de cribado, al ser el diagnóstico más precoz, la incidencia se desplazará a edades más jóvenes, lo que implica que se prolonga el período entre la edad de diagnóstico y la de muerte.
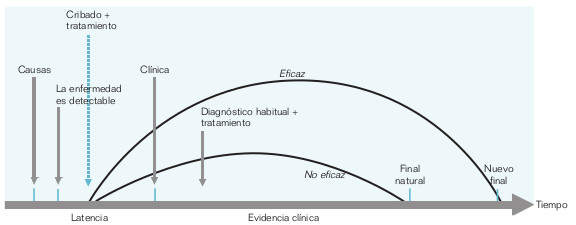
Para comprender los efectos del cribado sobre la frecuencia e impacto de una enfermedad, hay que recordar la historia natural de ésta, es decir, la evolución que sigue la enfermedad en ausencia de intervención. Este proceso se resume en la figura 16-1. Tal y como se aprecia en esta figura, existen dos fases: una etapa en la que la enfermedad no se detecta clínicamente (etapa subclínica o preclínica o fase de latencia), y una etapa clínica, en la que aparece la sintomatología, pues los síntomas sobrepasan el umbral de detección (el horizonte clínico, variable según las personas) y se hace aparente la enfermedad.
El período de detección durante la fase de latencia (sojourn time) es el que se extiende desde que la enfermedad es detectable hasta la aparición de la clínica. El período de adelanto diagnóstico (lead time) es el que abarca entre el diagnóstico determinado por el cribado y el comienzo de la fase clínica.
Características de la enfermedad, población y prueba del cribado
Es preciso diferenciar la búsqueda oportunista o cribado ocasional que puede realizar un médico en su práctica clínica habitual de los programas universales de cribado. Lo que sigue se refiere fundamentalmente al establecimiento de cribados universales para ciertos estratos de edad y sexo de la población. Antes de implantar un programa de cribado universal, es necesario responder a las siguientes preguntas: ¿qué condiciones debe cumplir una enfermedad susceptible de entrar en el programa de cribado?, ¿a quiénes (población) debe dirigirse el programa?, ¿cómo debe llevarse a cabo el programa (con qué medios o pruebas diagnósticas)?, ¿se dispone de los recursos necesarios?
En primer lugar, una enfermedad susceptible de entrar en un programa de cribado debe cumplir las siguientes condiciones:
- Debe ser frecuente y grave, para que su valor predictivo sea alto y, además, sea percibida como un problema socialmente prioritario, de modo que la población también acepte el programa.
- Debe ser claramente diferenciable de la normalidad. Su curso clínico debe ser conocido y su estadio presintomático estar claramente definido.
- El tratamiento en el estadio presintomático tiene que reducir la mortalidad o las complicaciones graves (si éste es el efecto) de manera más eficaz que el tratamiento tras la aparición de los síntomas. Si dicho tratamiento no reduce la mortalidad o la gravedad, al menos debe mejorar la calidad de vida del enfermo. Pero si no hay tratamiento, ¿para qué diagnosticar antes? Por ejemplo, un diagnóstico precoz no tendría sentido en el caso de enfermedad de Alzheimer mientras no se disponga de un tratamiento eficaz frente a esta enfermedad.
- Debe ser una enfermedad tratable y controlable como fenómeno de masas.
Por su parte, la población susceptible de incorporarse a un programa de cribado tiene que cumplir los siguientes requisitos:
- Debe tener riesgo elevado para la enfermedad, es decir, una prevalencia alta.
- Debe ser población con buenas relaciones comunitarias y actitud cooperativa.
- Se debe contar con datos demográficos de dicha población, con el fin de que se puedan planificar correctamente los recursos necesarios para ejecutar el programa de cribado.
Por su parte, la prueba diagnóstica que vaya a utilizarse en el cribado difiere en una serie de características de las pruebas empleadas rutinariamente en el diagnóstico asistencial (tabla 16-1) y debe reunir las siguientes características:
- Debe ser aceptable por la población, para que no dificulte la participación.
- Debe ser reproducible y válida; en orden lógico, primero debe ser reproducible, es decir, proporcionar los mismos resultados en condiciones similares, si no difícilmente se podría estimar su validez.
| Prueba diagnóstica de cribado | Prueba diagnóstica asistencial |
|---|---|
| Aplicada a personas con buen estado de salud aparente | Aplicada a personas con problemas definidos |
| Para un colectivo | Individualizada |
| Menos precisa | Más precisa |
| Más barata | Más cara |
| No constituye base para un tratamiento | Sí constituye base para un tratamiento |
| Clasifica en baja o alta probabilidad de estar enfermos | Clasifica en exentos de la enfermedad/enfermos |
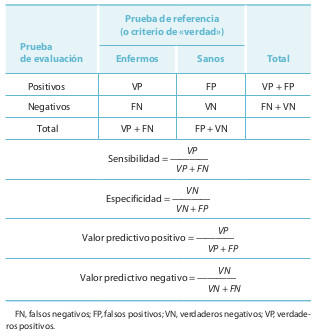
En la tabla 16-2 se presentan los parámetros para evaluar la validez de una prueba diagnóstica. El parámetro más importante es el valor predictivo positivo, que debe ser elevado. Para ello se requieren dos condiciones esenciales: alta sensibilidad (elevada frecuencia de verdaderos positivos) y alta prevalencia de la enfermedad que hay que diagnosticar. Se puede pensar que una especificidad elevada también sería necesaria para disminuir los falsos positivos en relación con los verdaderos negativos, pero la sensibilidad y la especificidad suelen ir contrapuestas: cuando aumenta la una, se sacrifica la otra. Además, las pruebas muy específicas suelen ser costosas, y no suele haber recursos para aplicarlas en poblaciones amplias.
Si se tiene en cuenta que una prueba de cribado inicia un proceso diagnóstico, que luego se verifica mediante otras pruebas de confirmación, lo más importante en una enfermedad grave es que no queden casos sin un diagnóstico de presunción, es decir, que inicialmente no haya falsos negativos. Por lo tanto, es más importante la sensibilidad que la especificidad. El valor predictivo positivo aumenta en las poblaciones con mayor prevalencia de enfermedad. No es lo mismo un valor predictivo positivo del 2% que uno del 10%.
En el primer caso, por cada 100 personas remitidas a la prueba de confirmación sólo 2 resultarán enfermas, mientras que en el segundo caso, por cada 100 personas en el programa 10 presentarían la enfermedad. La rentabilidad del cribado es mayor en la segunda situación que en la primera, pues con el mismo esfuerzo de cribado se han detectado cinco veces más casos.
Por último, en relación con los recursos que tienen que utilizarse en un programa de cribado es preciso considerar las siguientes condiciones:
- Se debe contar con todos los recursos de diagnóstico y tratamiento de los sujetos positivos en la prueba. Es necesario asegurarse de que hay recursos para el seguimiento y la realización de pruebas confirmatorias de alta especificidad para quienes tuvieron un test de cribado positivo.
- Sólo se iniciará el programa una vez que se hayan examinado las restantes prioridades sanitarias cuya realización entrañaría un coste idéntico al del programa.
Clasificación de los cribados
Los cribados se pueden clasificar en función de diferentes características:
- Cribado simple (para una enfermedad) o múltiple (para varias enfermedades). Lo más usual es que el cribado de población sana se dedique a una sola enfermedad.
- Cribado monofásico (de una etapa) o multifásico (de varias etapas). Las pruebas que normalmente se utilizan son presuntivas, lo cual implica que los positivos dados por la prueba de cribado deben confirmarse. La mayoría de los cribados son multifásicos.
- Cribado ocasional u oportunista (aprovechando que un paciente acude por otro motivo al servicio sanitario) o sistemático (dirigido al conjunto de la población).
- Cribado no selectivo (dirigido a toda la población) o selectivo (dirigido a grupos de riesgo elevado). Este último se realiza cuando no se ha demostrado la rentabilidad universal de un cribado.
- Cribado precoz (búsqueda de la enfermedad en su estadio inicial) o tardío (búsqueda de casos «olvidados» en la población). La mayor parte de los cribados intentan ser precoces.
Un cribado puede clasificarse con cualquier combinación de los tipos anteriores. Las peculiaridades de cada programa de cribado dependerán de las características de la enfermedad buscada, de la economía de los medios y de la complejidad del trabajo en la comunidad diana.
Evaluación de los programas de cribado
Sesgos que afectan a la evaluación
A la hora de evaluar la utilidad de un programa de cribado hay que tener en cuenta el efecto de una serie de errores o sesgos que se describen a continuación.
Sesgo de adelanto diagnóstico (lead time bias)
El cribado permite el diagnóstico previo a los síntomas, es decir, en la fase de latencia. En ausencia de una mayor eficacia del tratamiento precoz frente al tratamiento en fase clínica, el efecto es que aumenta la duración media de la enfermedad; dicho de otra forma, el intervalo entre el diagnóstico tras los síntomas y el final natural de la enfermedad es inferior al existente entre el diagnóstico precoz por cribado en fase asintomática y el final natural. Si se compara cándidamente la duración media de la enfermedad en quienes fueron diagnosticados por cribado y quienes lo fueron por sus síntomas, tal duración (tiempo de supervivencia) será superior en los diagnosticados por cribado, simplemente porque en ellos se adelantó artificialmente el momento del diagnóstico de la enfermedad, y no porque se les prolongase la vida.
Existen varias opciones para contrarrestar este sesgo:
- Se puede comparar la mortalidad antes y después de desarrollar un programa de cribado (comparación prepost) ajustando por los diferentes estadios de la enfermedad: en los casos detectados mediante el cribado hay un mayor predominio de estadios tempranos, en los que el tiempo de supervivencia es mayor (el estadio se comporta en este caso como un factor de confusión).
Las comparaciones pre-post, sin embargo, no evitan el efecto de otros factores. En primer lugar, el denominado fenómeno de Will Rogers, que se refiere al hecho de que con el tiempo las pruebas diagnósticas mejoran (es decir, aumenta su sensibilidad) y se etiquetan más y mejor los estadios precoces, que tienen menor mortalidad. En segundo lugar, puede también influir el hecho de que el curso natural de una enfermedad sea un continuo y, por lo tanto, la categorización en estadios suponga una pérdida de información. Así, es posible que los sujetos, aun perteneciendo al mismo estadio, difieran en pronóstico porque los casos detectados por el cribado por término medio estén más próximos al comienzo que al final del estadio (comienzo del siguiente estadio). - Comparar las edades medias de ocurrencia (diagnóstico) de la enfermedad y de fallecimiento. Un cribado eficaz normalmente rebajará la primera y retrasará la segunda. El problema es que para poder determinar si esa diferencia refleja realmente un aumento del tiempo de vida, hay que tener en cuenta todos los fenómenos que pueden retrasar la edad de mortalidad, como cambios en los estilos de vida y otros. Los estudios de observación, incluyendo las comparaciones pre-post en las mismas poblaciones, no proporcionan información suficiente para controlar este efecto.
- Ensayos aleatorizados. Si se conoce la duración de cada fase en el curso natural de la enfermedad, el sesgo de adelanto diagnóstico es controlable con cualquier diseño. En caso contrario (lo más habitual) se puede realizar un ensayo clínico aleatorizado, en el que el resultado será la mortalidad (y no la incidencia) o la calidad de vida. En el caso de cribado de cáncer, la valoración del tiempo de adelanto diagnóstico puede hacerse comparando la incidencia de la enfermedad en el grupo sometido a cribado tras un cribado negativo (cánceres producidos en el intervalo) con la incidencia esperada que sería la observada en el grupo control no sometido a programa de cribado. Conforme va aumentando el tiempo tras el momento de realización del cribado, el beneficio de éste desaparece, ya que no se detectan más casos en fase de latencia: la detección precoz de estos casos provoca una disminución inicial de la incidencia, que con el paso del tiempo desaparece y la tasa de incidencia del grupo inicialmente sometido a un cribado llega a hacerse igual a la del no cribado.
Un método aproximado para estimar el tiempo de adelanto diagnóstico debido al cribado es calcular el tiempo de seguimiento necesario para que la incidencia acumulada de casos en la población no cribada llegue al número de casos detectados en la población cribada. El tiempo de adelanto diagnóstico se relaciona con el tiempo de detección clínica o período durante el cual una lesión asintomática puede sacarse a la luz, que, a su vez, puede estimarse de dos maneras: multiplicando por 2 el tiempo de adelanto diagnóstico, o, de manera aproximada, con el cociente que resulta de dividir la prevalencia en el momento del cribado por la tasa de incidencia de la enfermedad en la población.
Por último, el tiempo de adelanto diagnóstico es útil para establecer la periodicidad del cribado en una población, por la relación que mantiene con el tiempo de detección clínica.
Si se asume que el tiempo de adelanto diagnóstico es constante y que la distribución de los estadios de la enfermedad en la población no cambia en el tiempo, la periodicidad del cribado debe ser el doble del tiempo de adelanto diagnóstico (o, lo que es lo mismo, igual al tiempo de detección clínica).
Sesgo por duración de la enfermedad (length bias)
Este error está muy relacionado con la falacia de Neyman. El cribado es en esencia un estudio transversal y, por ello, tiene mayor probabilidad de seleccionar los casos de enfermedad con duración más larga (menos letales), que tienen mejor pronóstico que el resto y, por este motivo, están presentes durante más tiempo en la población. Si el pronóstico es mejor, el cribado seleccionará a una población con un pronóstico por término medio mejor, en la que podría darse el caso de que un tratamiento inútil pareciera eficaz.
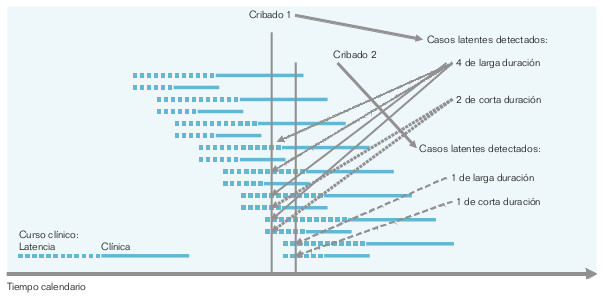
Por ejemplo, supóngase que una enfermedad se compone de dos tipos de casos: el 50% de la incidencia son casos de evolución clínica más larga (4 años de latencia y 4 años con sintomatología clínica) y el resto, por casos de evolución más corta (2 años de latencia y 2 años con sintomatología clínica) (fig. 16-2). Esto supone que la fase sintomática clínica dura 3 años por término medio. Si se hace un cribado, se seleccionarán dos casos de evolución larga por cada caso de evolución corta debido a la desigual duración de unos y otros. Si se asume que el diagnóstico se realiza en la mitad de la fase de latencia (es decir, al año en los casos de duración corta y a los 2 años en los de duración larga), a los que hay que sumar la duración habitual de la fase de clínica (2 años en los casos de duración corta y 4 años en los otros), esto dará un tiempo medio de supervivencia de enfermedad de 5 años:
$$5 = \frac{1 \times 3 + 2 \times 6}{3}$$
Si se controla la fase de latencia (el adelanto diagnóstico), la duración media de la fase clínica será de 3,3 años:
$$3,3 = \frac{1 \times 2 + 2 \times 4}{3}$$
Este valor de 3,3 años es superior a la media real.
Para neutralizar este tipo de error sería necesario evaluar la eficacia del cribado en cribados subsiguientes al primero, es decir, una vez se han eliminado de la población diana los casos detectados en el primer cribado. En el ejemplo de la figura 16-2, si se realiza un nuevo cribado un año después del primero, la proporción de casos de evolución larga y corta en la población será la adecuada, es decir, del 50%. Cuanto más se retrase el segundo cribado con respecto al primero, más probable será que el sesgo por duración de la enfermedad se vuelva a presentar.
En el ejemplo anterior se asume que la sensibilidad de la prueba diagnóstica es del 100%. Si esto no es así, como suele ser lo habitual, una cierta proporción de casos pasarán desapercibidos en el primer cribado y serán proporcionalmente detectados en el siguiente. La probabilidad de que el sesgo por duración de la enfermedad se presente será inversamente proporcional al valor de la sensibilidad. Tampoco debe olvidarse que normalmente la sensibilidad de una prueba diagnóstica muestra una relación directa con la historia natural de la enfermedad (la sensibilidad aumenta conforme la enfermedad progresa hacia fases más avanzadas).
Las condiciones de intervalo de cribado adecuado y la alta sensibilidad de la prueba diagnóstica no siempre se cumplen y, por lo tanto, el sesgo de duración de la enfermedad es una amenaza muy presente. La sensibilidad depende de las características de la prueba, pero el cumplimiento del intervalo de cribado depende de la población y no todos sus individuos siguen adecuadamente el protocolo del programa. Así suele suceder incluso en los ensayos aleatorizados, que son sobre población sana en la comunidad (ensayos de campo). La posibilidad de evitar el sesgo de duración es inversamente proporcional al cumplimiento del protocolo del intervalo entre cribados: si los cribados no se realizan con la suficiente periodicidad (tardan más en realizarse de lo establecido), se pueden acumular en la población los casos de evolución lenta (duran más tiempo), que son los que más fácilmente se detectan por el cribado, y, por consiguiente, el sesgo de duración será mayor.
Sesgo del voluntario sano
Un programa de cribado es un programa de prevención que implica una preocupación de los participantes por la propia salud. Se ha comprobado reiteradamente que los que acuden a los programas de prevención presentan menor riesgo de estar enfermos que los que no lo hacen. Por este motivo, cabe esperar que el programa sea evaluado artificialmente como más beneficioso de lo que es. Este sesgo es muy difícil de evitar, es un sesgo de selección. El análisis de las características de la población participante en otros programas de prevención y de las posibles razones que puedan influir en la participación puede servir para valorar de forma aproximada el impacto de este sesgo en la evaluación de los resultados de un programa de cribado.
Exceso de diagnóstico
Si hay variabilidad en los pacientes en la duración de la fase clínica, hay que asumir que dicha variabilidad también tiene lugar en la fase preclínica. Por lo tanto, es perfectamente factible que haya casos en los que su evolución sea tan pausada que nunca lleguen a la fase clínica. Estos casos pueden salir a la luz con el cribado, dando lugar a dicho efecto de exceso de diagnóstico. De hecho, uno de los principales factores de riesgo para ser diagnosticado de cáncer de próstata es hacerse una determinación del antígeno prostático (PSA, prostate-specific antigen). Muchos pacientes con este cáncer mueren de otra causa sin haberse enterado de que lo tenían.
Si se hubiese determinado el PSA, habrían sido etiquetados de cáncer, pero esto no hubiese mejorado su pronóstico.
Tipos de estudios para la evaluación
La evaluación de un programa de cribado se puede realizar de manera indirecta basándose en tres elementos fundamentales: la frecuencia de la enfermedad, la capacidad del cribado para identificar la lesión y la mejora inducida por el tratamiento en la fase asintomática. Por ejemplo, para valorar la eficacia del cribado de retinopatía en diabéticos se pueden valorar los siguientes datos:
- Prevalencia de retinopatía en diabéticos.
- Capacidad del cribado en diabéticos para identificar anomalías que sean predictores robustos de desarrollar ceguera.
- Efectos del tratamiento con fotocoagulación por láser en los casos detectados por el cribado sobre la incidencia del deterioro visual grave.
La información más difícil de obtener se refiere al tercer aspecto: determinar si el tratamiento en la fase preclínica conduce a un mejor pronóstico que en la fase clínica. Por ello a veces resulta necesario diseñar estudios específicos que intenten valorar estos tres elementos.
Ensayo clínico comunitario
Es el diseño ideal, que puede neutralizar, si está realizado correctamente, los sesgos mencionados en el apartado anterior. Se puede aleatorizar individualmente a la población en el estudio, pero es más frecuente la aleatorización de comunidades por razones de factibilidad.
En un estudio experimental, la aleatorización intenta garantizar que los grupos (en este caso, cribado y no cribado) sean comparables. El sesgo del voluntario (participante) en este tipo de estudios produciría dos consecuencias. En primer lugar, disminuiría la validez externa del estudio: no es posible saber si el cribado será eficaz en poblaciones con características diferentes a las de los participantes en el estudio.
Se debe recordar también que el análisis por intención de tratar (es decir, manteniendo a cada individuo en el grupo al que fue originalmente asignado, con independencia de que se le haya realizado o no el cribado) garantiza la comparabilidad de los grupos y que el sesgo de selección no se presente. Otro problema es que la no participación reduce la probabilidad de encontrar una diferencia estadísticamente significativa, ya que el tamaño muestral final del ensayo es menor.
Si la eficacia del cribado radica en una reducción de la mortalidad, lo que se compara es la mortalidad en el grupo cribado frente a la del grupo no cribado.
Estudio de cohortes
El cribado se implanta en una población y ésta configura una cohorte de individuos cribados. Los resultados se comparan con los observados en otra población no cribada.
Dado que no se ha utilizado la aleatorización para repartir por igual los otros factores pronósticos (posibles factores de confusión), este tipo de diseños es más débil. Hay que realizar análisis multivariable ajustando por las diferencias existentes al inicio entre los grupos que se comparan. Los sujetos que rechazan el cribado tienen tasas de mortalidad diferentes de los que lo aceptan, y esto puede introducir errores de difícil cuantificación.
Estudio de casos y controles
En la valoración del cribado se suelen utilizar estudios de casos y controles emparejados por la edad a la que ocurre el efecto que debe evitarse (la edad de fallecimiento si es la muerte). Si lo que se quiere evaluar es la eficacia del cribado en el cáncer de colon, los casos serán los fallecidos por cáncer de colon.
Los controles deben ser comparables a los casos justo en el momento en que la enfermedad se haya detectado. Los controles se suelen emparejar por la edad a la que ocurre el acontecimiento de interés en los casos. Tener la enfermedad no supone un criterio de exclusión en los controles, con la condición de que no se haya diagnosticado la enfermedad antes en el control que en el caso. No se deben elegir exclusivamente controles con un estadio precoz de la enfermedad en un estudio de casos y controles sobre la eficacia del cribado, porque en ellos se realiza con mayor frecuencia el cribado (y éste se comportará falsamente como un factor protector); en todo caso, los controles deberían representar los estadios precoces de la enfermedad con la misma frecuencia que existen en la población. Tampoco es una elección acertada elegir controles fallecidos, con la finalidad de favorecer la comparabilidad de la información con la de los casos (también fallecidos). Es preciso señalar también que el estudio de casos y controles no sirve para establecer la periodicidad con la que debe establecerse un cribado.
En la valoración de la exposición hay que definir bien el marco temporal en el que se considerará si el individuo ha sido o no cribado. En los controles, el límite superior de la ventana temporal viene determinada por la fecha de diagnóstico del caso emparejado, mientras que para los casos detectados por el cribado, este límite es la fecha de cribado.
El límite inferior del cribado se sitúa en función de la historia natural de la enfermedad que se estudia. Las situaciones en las que la prueba de cribado se hace como consecuencia del proceso diagnóstico, ante la presencia de clínica, deberían considerarse como no cribados. La realización del cribado se debería clasificar en tres grupos: la realizada en sujetos completamente asintomáticos, la realizada como consecuencia de otra prueba diagnóstica que ha sido positiva y la realizada en pacientes con una clínica parecida a la enfermedad problema (sin padecerla). A veces no es fácil atribuir el cribado a uno de estos grupos. Un paciente puede tener molestias atribuibles a un proceso que es factor de riesgo de la enfermedad diana (ej. la hipertrofia benigna de próstata para el cáncer de próstata), que, por similitud con la enfermedad, se juzgan como síntomas. De esta manera, el cribado realizado en estos pacientes se considerará consecuencia del diagnóstico de la enfermedad y no un auténtico cribado, y se reducirá el posible beneficio atribuible a éste.
En los estudios de casos y controles conviene ajustar por las variables que se relacionan con el efecto que se valora (enfermedad grave, muerte) y que se relacionan con participar en el cribado. Por ejemplo, en el cáncer de mama, si un peor nivel educativo se asocia con diagnóstico tardío de la enfermedad y, además, influye en el cribado, en el análisis estadístico habría que ajustar por esa variable.
Si la mortalidad en las personas (invitadas) que no acuden al programa de cribado es mayor que en los sujetos que no lo realizan por no haber sido invitados, un estudio de casos y controles sobrestimará el beneficio del cribado. Sucederá lo opuesto cuando la mortalidad sea menor. Un problema relacionado con el anterior es la presencia de comorbilidades. Por definición, los casos son fallecidos y en ellos es más probable que se presenten otros procesos que son causas competitivas de muerte y éstos pueden estar asociados a un menor uso de la prueba de cribado. De esta manera se sobrestima el beneficio del cribado. Por otra parte, la inclusión de casos con probable mala evolución es un error que se produce especialmente en los estudios de casos y controles.
En resumen, en los estudios de casos y controles pueden existir sesgos si no se cumplen las tres condiciones siguientes:
- Que se alcance una tasa de respuesta muy elevada a la entrevista o al cuestionario, ya que hay que incluir a los sujetos con peor nivel de salud, donde es más probable que no se haya hecho el cribado. Su no inclusión puede aumentar espuriamente la frecuencia de cribado en los casos.
- Que haya una gran exactitud en el momento y las razones de realización del cribado en los casos y los controles, especificando claramente la presencia y ausencia de síntomas relacionados con el cáncer.
- Que el seguimiento de los casos incidentes se produzca durante un período lo suficientemente largo para detectar una metástasis o la muerte, si no se producirá el sesgo por adelanto diagnóstico en caso de que no haya un tratamiento eficaz. El seguimiento debería prolongarse hasta que no haya diferencias en la mortalidad entre los sujetos que presentan cáncer y los sujetos de la población general de la misma edad y sexo.
Estudios ecológicos
Los estudios ecológicos están sometidos a la falacia ecológica y son diseños débiles. No obstante, si se dan ciertas condiciones, pueden ofrecer una estimación de la eficacia del cribado:
- Si en los períodos o áreas geográficas que se comparan hay cambios bruscos en la frecuencia del cribado (ej. del 80%).
- Si hay datos válidos de la frecuencia del efecto que hay que evitar durante el período o en las áreas de estudio.
- Si el tamaño de la población es suficiente.
- Si hay datos de que, en ausencia de cribado, la frecuencia del efecto no desciende.
- Si la reducción del efecto en el período o área cribada se reduce de manera tal que es poco verosímil que otras variables no medidas, diferentes del cribado, puedan ser responsables del descenso.
Indicadores
Para calcular los indicadores necesarios para evaluar la utilidad de un cribado se necesita un buen sistema de información. La evaluación de un cribado normalmente dura mucho y, por ello, desde el principio es necesario prever una monitorización del desarrollo del programa de cribado (lo cual, si no se tiene en cuenta, puede hacer fracasar al programa). En la tabla 16-3 se presentan las características de los indicadores utilizados para la evaluación de la efectividad de un programa de cribado de cáncer, aplicables también al cribado de otros procesos. El único indicador directo de la eficacia de un cribado es la reducción del efecto que se intenta prevenir, todos los demás son indirectos. Se describen a continuación los distintos indicadores.
| Tipo de medida | Indicador | Parámetro estimado |
|---|---|---|
| Observación básica | Tasas de participación por edad y tiempo Tasas de detección por edad, tamaño, estadio y grado de malignidad Incidencia de cáncer en el intervalo por edad y tiempo desde el último cribado Tasas de cáncer en los que acuden y no al cribado por edad, tamaño, estadio y grado de malignidad | Aceptación por la población Sensibilidad según la fase de desarrollo del tumor Eficacia de la detección precoz Beneficio posible teniendo en cuenta el sesgo de selección |
| Modelización | Tiempo de detección, tiempo de adelanto, sensibilidad de la prueba y del programa, por edad y tiempo Prevalencia esperada según el tiempo de detección y sensibilidad, y prevalencia observada en el primer cribado y siguientes Incidencia observada en la población cribada e incidencia esperada en ausencia de cribado, por histología y otros atributos del tumor Mortalidad observada según tamaño, estadio y grado de malignidad de los tumores detectados, comparada con la esperada en ausencia de cribado | Eficacia de la detección precoz, identificación de las causas de deficiencias Sobrediagnóstico Sobrediagnóstico de tipos específicos de tumores Beneficio en la mortalidad |
| Indicadores directos | Proyección de la incidencia anticipada de tumores avanzados si el cribado no se hubiera introducido con respecto a la incidencia observada desde el comienzo del cribado Proyección de la mortalidad anticipada si el cribado no se hubiera introducido con respecto a la mortalidad observada desde el comienzo del cribado Exceso de mortalidad de cáncer antes y después del comienzo del programa | Beneficio en la mortalidad - confundida por sesgos de valoración Beneficio en la mortalidad – confundida por cambios en la terapia y sesgos de valoración Beneficio en la mortalidad – confundida por cambios en la terapia |
La tasa de participación indica el grado de aceptabilidad del cribado por parte de la población. Una baja tasa de cribado indica que la medida no ha calado en la población.
Las tasas de detección por estadio y tamaño son un indicador indirecto de la sensibilidad del cribado: la frecuencia de estadios precoces debería ser mayor. Una estimación simple de la sensibilidad del cribado requiere algo más. Los cánceres que surgen en una población cribada son de dos tipos: los perdidos en el primer cribado y los nuevos que se originan, que no se pueden distinguir clínicamente, pero en los que sería razonable asumir que los detectados en un tiempo breve tras el cribado (siendo definido este tiempo en función de lo que se conoce sobre la historia natural del proceso que se criba) son pérdidas del cribado (falsos negativos). Por lo tanto:
$$Sensibilidad = \frac{CDC}{CDC + CDP}$$
donde CDC es “Casos detectados en el cribado” y CDP es “Casos detectados clínicamente tras un período definido después de un cribado negativo”.
La fórmula anterior es muy simplista e implica asunciones que pueden no ser verdad. Otros procedimientos más complicados, como las cadenas de Markov, pueden ofrecer estimaciones más realistas.
La incidencia de cáncer en el intervalo entre cribados debe ser reducida. Lo cual indica que el cribado ha detectado tumores preclínicos.
La comparación de tasas de la enfermedad entre los que acuden o no al cribado, teniendo en cuenta el estadio y el grado de malignidad, ofrece un indicador indirecto de la eficacia potencial del programa. Es posible que las personas que acuden al programa sean distintas de las que no acuden, y tengan un menor riesgo general de mortalidad, por lo que con este procedimiento no se puede descartar la influencia de un sesgo de selección. También hay que tener en cuenta los sesgos de adelanto diagnóstico y de duración de la enfermedad que operan en la misma dirección de exagerar el efecto beneficioso del cribado.
Hay una serie de parámetros que no son directamente medibles tras la implantación de un programa de cribado y que se conocen generalmente en los ensayos clínicos que preceden a la aplicación del cribado. Son el de tiempo de adelanto diagnóstico, el período de detección, etc. Estos parámetros deben tenerse en cuenta cuando se valora la eficacia de un cribado sobre el terreno.
Con la sensibilidad del cribado (conocida normalmente en el cribado) y el intervalo entre cribados se puede estimar una prevalencia esperada de la enfermedad que se compara con la prevalencia observada en el cribado: si esta última es mayor, habrá que valorar si se está diagnosticando en exceso.
La comparación de la incidencia observada durante el cribado con la esperada en ausencia del cribado (ej. la existente con anterioridad al cribado o la resultante de un modelo matemático en función del perfil de riesgo de la población) puede indicar también si se están diagnosticando en exceso ciertos tipos específicos del proceso.
La distribución por estadios y grado de malignidad que se observa en el cribado puede dar una idea indirecta del beneficio del cribado, ya que se puede estimar cuál será la mortalidad esperada tras el proceso cribado.
La reducción en la incidencia de estadios avanzados con respecto a lo que sería esperado en ausencia del cribado constituye ya un indicador directo del beneficio en la mortalidad.
Hay que resaltar que este indicador puede verse influido por problemas en la estimación de lo esperado.
La comparación de la mortalidad observada en la población cribada con la que sería esperable en ausencia del cribado (ej. la existente con anterioridad, o la que sería resultante con el tratamiento actual y la distribución por estadios en ausencia del cribado) da una idea directa del beneficio del cribado. No obstante, esta comparación puede dificultarse debido a problemas en la valoración de la mortalidad esperada. Adicionalmente, aunque la disminución de la mortalidad tras la implantación del programa de cribado es la medida principal de eficacia, esta comparación puede verse también confundida por cambios en el tratamiento.
La periodicidad con que se realizará el cribado dependerá de la prevalencia de la enfermedad de interés (cuanto más elevada sea dicha prevalencia, menor debe ser la periodicidad), de la duración de la fase de latencia (ídem), de su rentabilidad económica, etc.
Establecimiento de prioridades de cribado
El cribado es una práctica clínica. Para establecer las prioridades de cribado en una población, es necesario valorar en ésta la carga de enfermedad prevenible y el análisis coste-eficacia del programa. La carga de enfermedad prevenible se refiere a la proporción de enfermedad que se puede evitar por el cribado si se aplicara al 100% de la población a los intervalos recomendados. Esta carga prevenible es el producto de la carga de enfermedad (ej. prevalencia) por la eficacia de la intervención (porcentaje de carga reducido). Cuando se comparan diferentes intervenciones (incluyendo el cribado) con la finalidad de prevenir diferentes enfermedades o problemas, suele utilizarse un único indicador, habitualmente los QALY (QualityAdjusted Life Years, años de vida ajustados por calidad) añadidos.
Se puede asignar a la carga de enfermedad prevenible una puntuación de 1 a 5 en función del quintil que ocupan los diferentes problemas que deben priorizarse. Conforme más elevada sea la carga de enfermedad prevenible, más alta será su puntuación.
El análisis coste-eficacia se mide como el coste-neto de la práctica preventiva dividida por el QALY añadido:
$$RC - eficacia = \frac{CP - CE}{QALY\ ahorrado}$$
donde RC es “Razón coste”, CP es “Coste de la prevención”, y CE es “Costes evitados”.
La escala de la razón coste-eficacia se mueve al contrario que la de carga de enfermedad prevenible: conforme más baja sea esta razón, más conveniente es la práctica preventiva. Por ello se ordenan de manera ascendente y el quintil que tiene el coste-eficacia más bajo recibe 5 puntos, y así sucesivamente hasta que el quintil con la razón coste-eficacia más elevada recibe 1 punto.
La suma de las puntuaciones para carga de enfermedad prevenible y razón coste-eficacia permite establecer prioridades para las diferentes prácticas de prevención.
En la tabla 16-4 se presentan estos cálculos de priorización para población de Estados Unidos. Estos datos no son directamente extrapolables a otros países debido a las diferencias en las tasas de enfermedad y en los costes asociados.
| Práctica | CEP | CE | Total |
|---|---|---|---|
| Vacunación infantil | 5 | 5 | 10 |
| Valoración del tabaquismo en adultos y consejo | 5 | 4 | 9 |
| Cribado del deterioro visual en >64 años | 4 | 5 | 9 |
| Cribado del cáncer cervical en mujeres sexualmente activas >17 años | 5 | 3 | 8 |
| Cribado del cáncer colorrectal mediante sangre oculta en heces y/o sigmoidoscopia en >49 años | 5 | 3 | 8 |
| Cribado de hemoglobinopatías, fenilcetonuria e hipotiroidismo en recién nacidos | 3 | 5 | 8 |
| Cribado de hipertensión a todos los adultos | 5 | 3 | 8 |
| Cribado de Chlamydia en mujeres de 15 a 24 años | 3 | 4 | 7 |
| Cribado de hipercolesterolemia en hombres de 35-65 y mujeres de 45-65 años | 5 | 2 | 7 |
| Cribado de problemas con el alcohol y consejo | 4 | 3 | 7 |
| Cribado de cáncer de mama a mujeres de 50 a 69 años | 4 | 2 | 6 |
| Cribado de deterioro visual a las edades de 3-4 años | 2 | 4 | 6 |
| Cribado de deterioro auditivo en >64 años | 2 | 2 | 4 |
Cribados reconocidos como eficaces
La tabla 16-4 presenta algunos de los cribados reconocidos como eficaces. Adicionalmente, en la tabla 16-5 se muestra un resumen de tales cribados. A este listado se podrían añadir los cribados recomendados en la mujer embarazada: bacteriuria asintomática para la prevención del parto pretérmino, cribado del VIH, preeclampsia y factor Rh.
| Cribados | Población diana | Nivel |
|---|---|---|
| Tuberculosis: prueba de tuberculina | Personas de alto riesgo | A |
| Hipotiroidismo, fenilcetonuria | Recién nacidos | A |
| Factor Rh: análisis de sangre | Embarazadas | A |
| Bacteriuria asintomática: cultivo de orina | Embarazadas | A |
| Hipertensión arterial: presión arterial | Personas >20 años | A |
| Preeclampsia: presión arterial | Embarazadas | B |
| Virus VIH: ELISA y PCR en los (+) | Sujetos de alto riesgo | A |
| Obesidad: medición de altura y peso | Tras observación | B |
| Hipercolesterolemia: colesterol total en sangre/suero | Hombres de 35-65 años, cada 5 años Mujeres de 45-65 años, cada 5 años | B B |
| Alcoholismo: detección del bebedor problemático | Rutinario | B |
| Cáncer de colon: sangre oculta en heces Sigmoidoscopia | Anual, de 50 a 80 años Cada 5 años, de 50 a 80 años | A B |
| Cáncer de mama: mamografía | Mujeres de 50-74 años, cada 1-2 años Mujeres de 40-49 años, cada 2 años Mujeres >74 años, cada 2 años | A B C |
| Cáncer de cuello uterino: citología cervical | Mujeres sexualmente activas de 24-65 años, cada 1-3 años Mujeres >65 años, si son sexualmente activas y tienen un factor de riesgo de cáncer de cérvix | A C |
| Trastornos de la visión: agudeza visual | Personas mayores | B |
| Audición: preguntas sobre la agudeza auditiva | Periódicamente en adultos mayores | B |
La lista de cribados de diferentes tipos de cánceres está sometida a discusión. En 2003, el Consejo de la Unión Europea (UE) emitió una serie de recomendaciones sobre los cribados de cáncer que había que realizar en el ámbito de la UE:
- Cribado de citología cervicovaginal para los precursores de cáncer del cuello del útero, que debe empezar en mujeres sexualmente activas no antes de los 20 años de edad y, a más tardar, a los 30 años.
- Cribado de mamografía para el cáncer de mama en mujeres de 50 a 69 años, de acuerdo con las «Directrices europeas de garantía de calidad del screening mamográfico».
- Cribado de sangre oculta en heces para el cáncer colorrectal en hombres y mujeres de 50 a 74 años.
Se trata de un listado no exento de controversia, ya que hay directrices de sociedades científicas que extienden el cribado de cáncer de mama a mujeres más jóvenes, plantean la eficacia de la sigmoidocolonoscopia en el cáncer colorrectal (que no difiere de la sangre oculta en heces) y limitan la edad superior a la que los cánceres de cuello uterino pueden ser detectados precozmente.